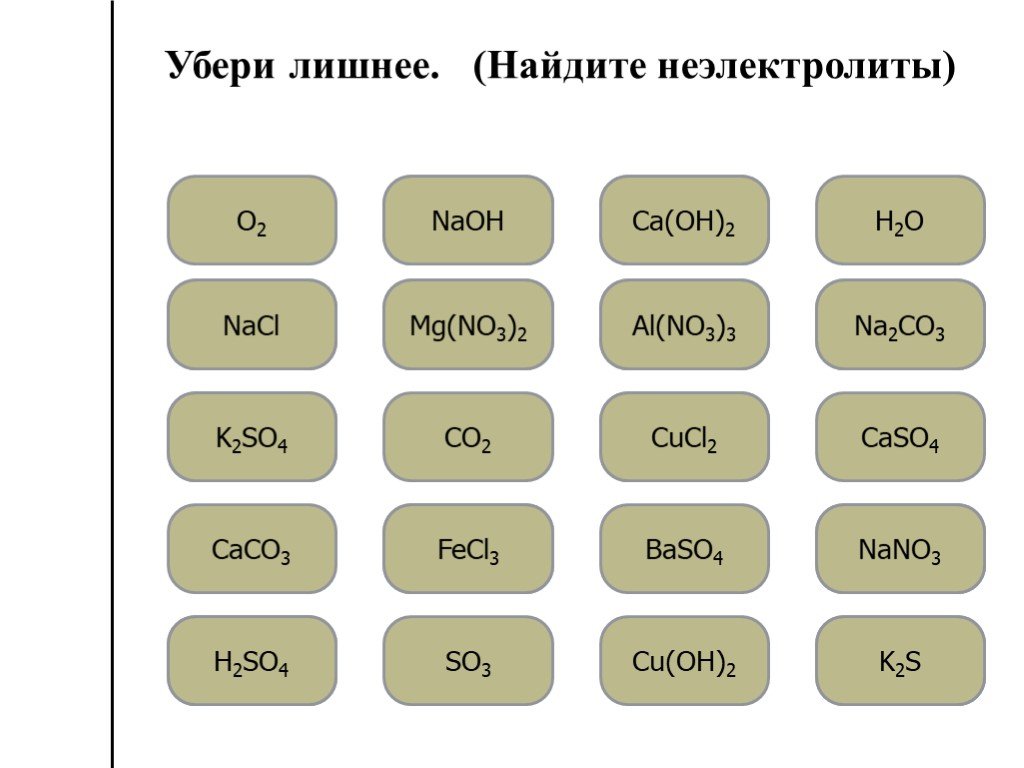
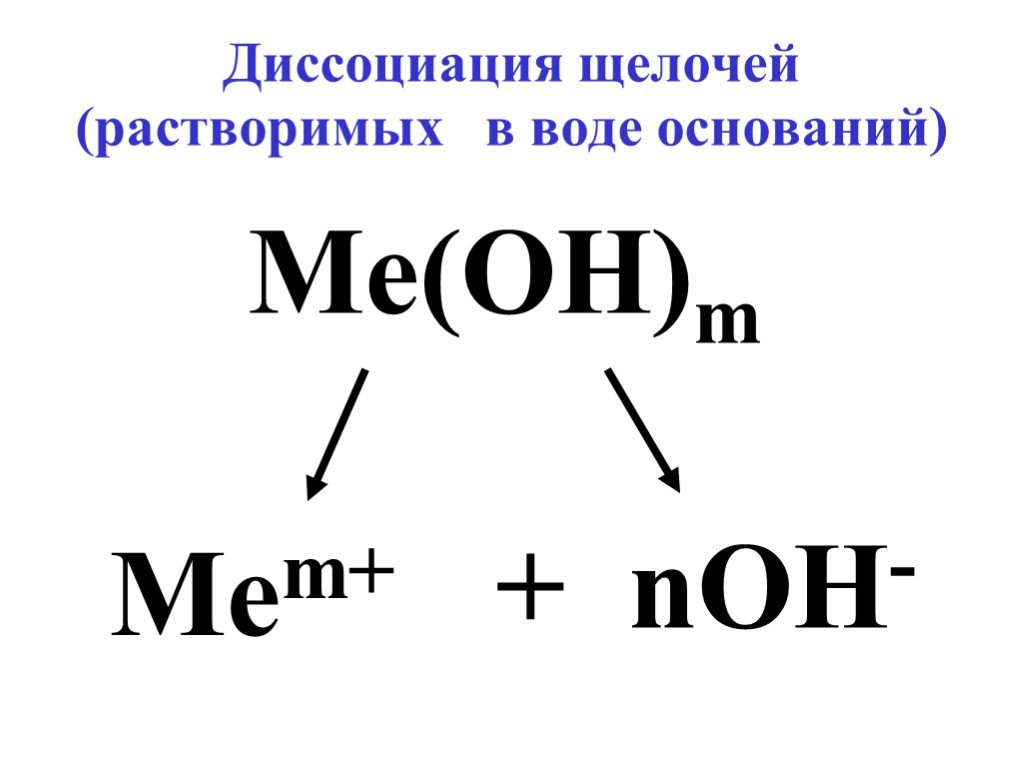
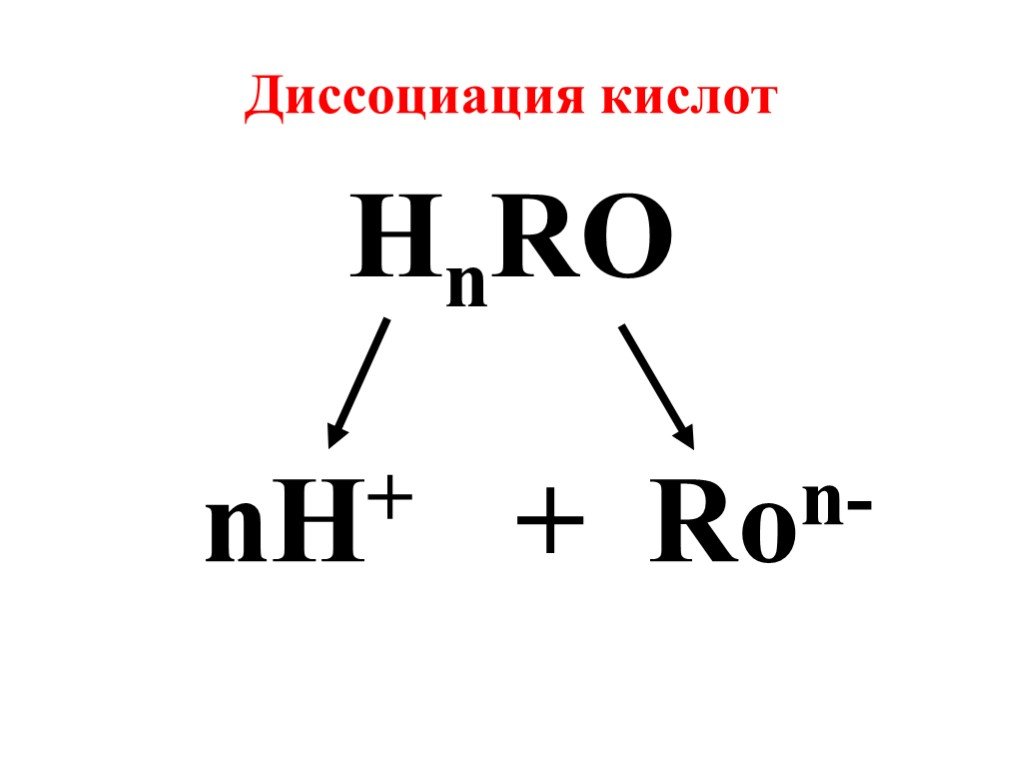
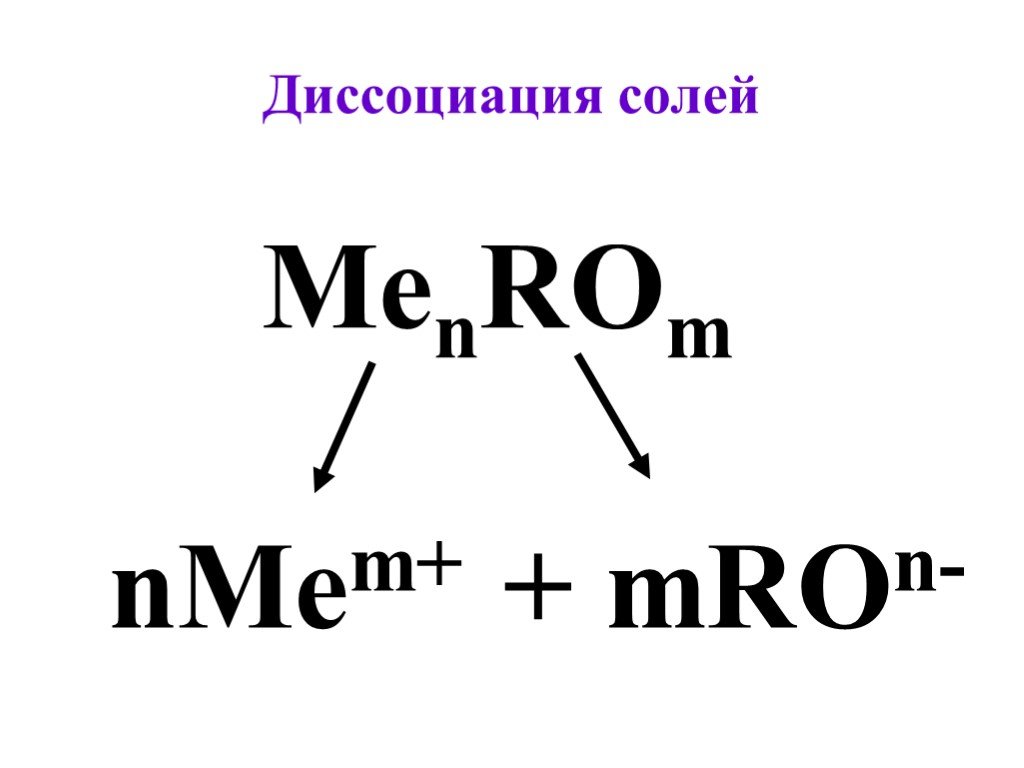
Презентация "Реакции ионного обмена" по химии – проект, доклад
Презентацию на тему "Реакции ионного обмена" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 28 слайд(ов).
Слайды презентации
Список похожих презентаций
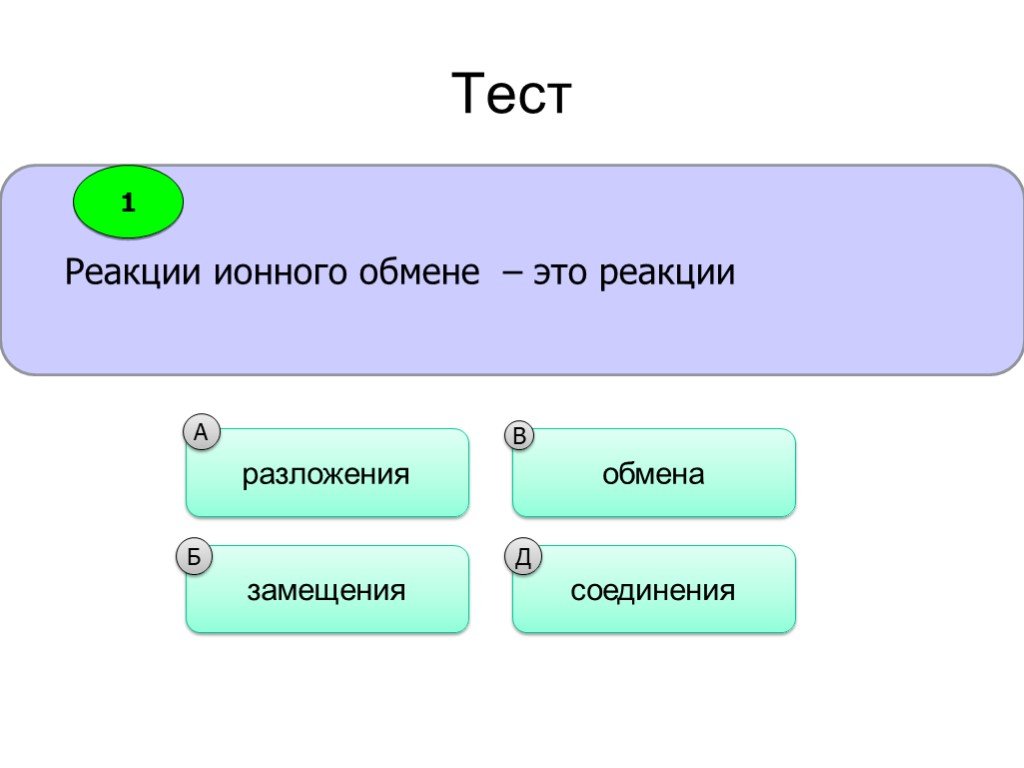
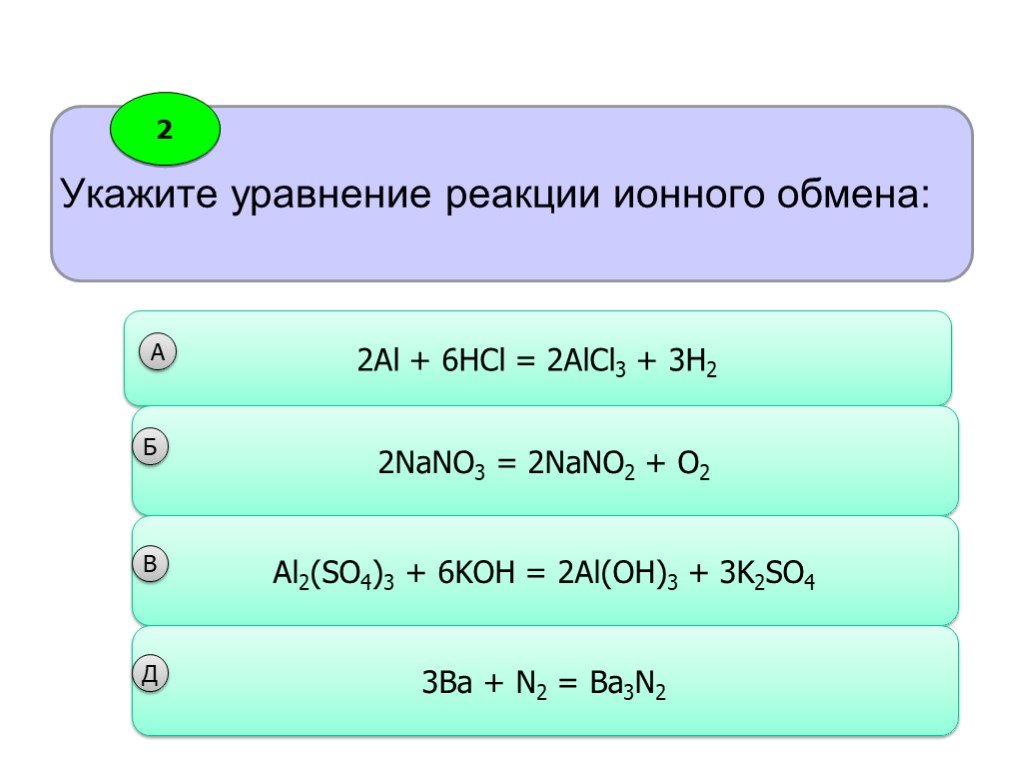
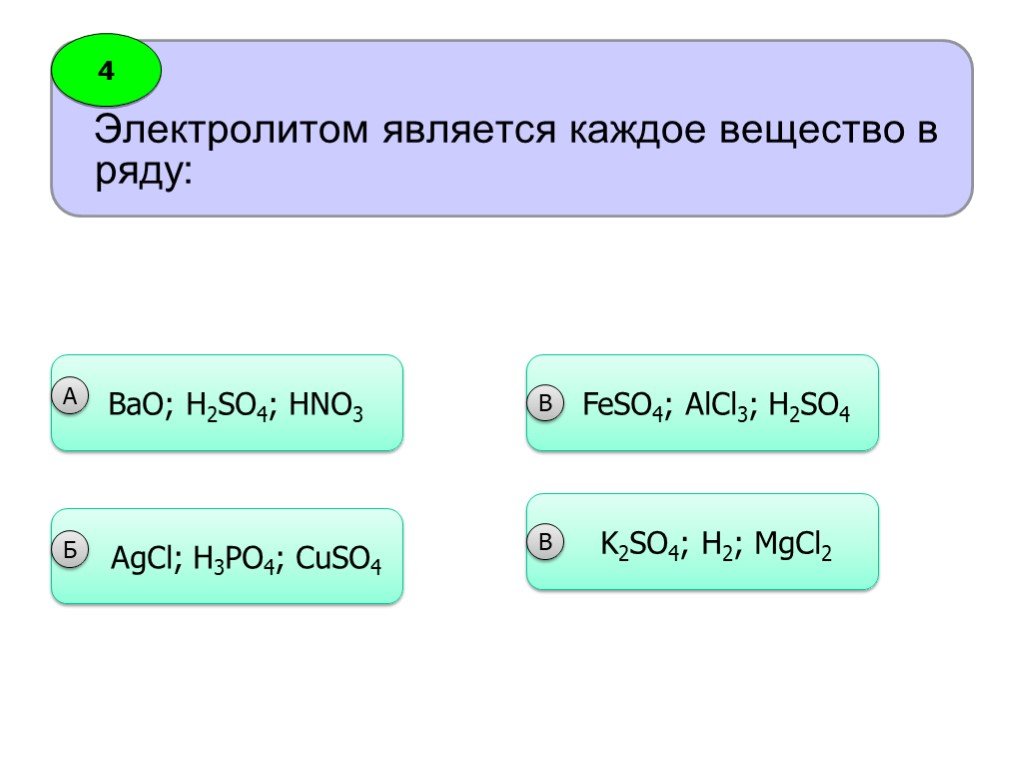
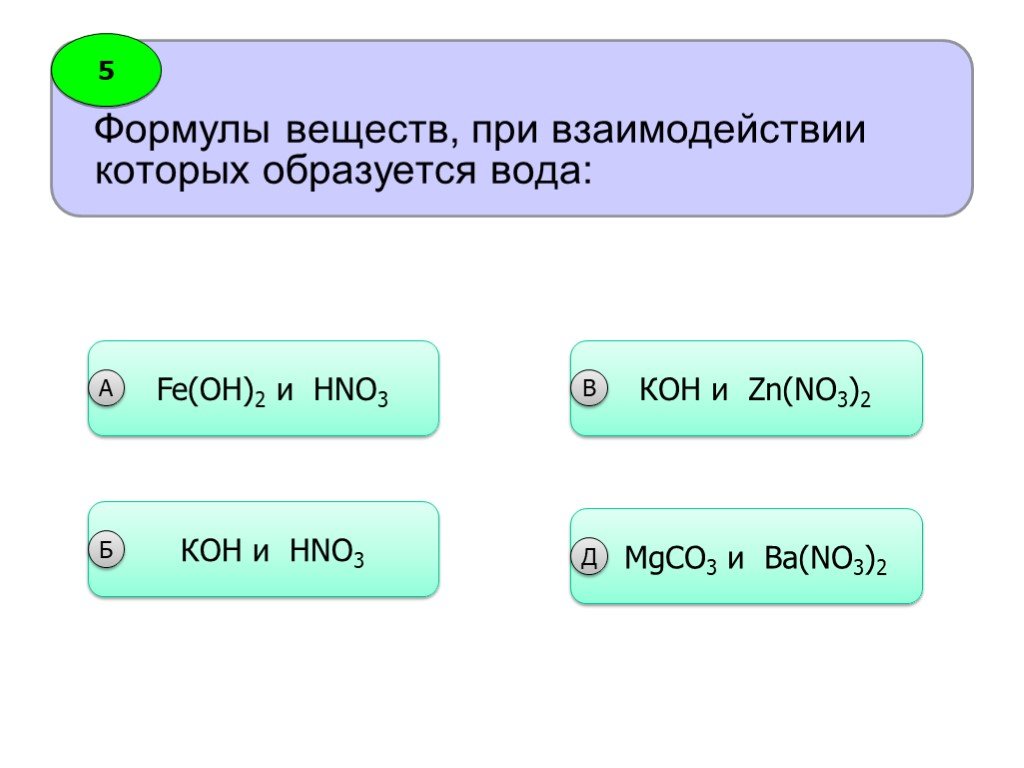
Реакции ионного обмена
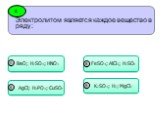
Получение гидроксида меди (II). I группа: CuCl2 + 2KOH = Cu(OH)2 + 2KCl 2 группа: CuBr2 + Ba(OH)2 = Cu(OH)2 + BaBr2 3 группа: Cu(NO3)2 + 2NaOH = Cu(OH)2 ...Электролитическая диссоциация веществ. Реакции ионного обмена и условия их протекания
1. Веществом, при диссоциации которого образуются катионы металла и анионы кислотного остатка, является. А. NH4NO3 Б. HNO3 В. NaOH Г. Na2SO4. 2. К ...Реакции ионного обмена
ЦЕЛЬ урока: сформировать понятие о реакциях ионного обмена. ЗАДАЧИ: Образовательные: познакомить учащихся с реакциями ионного обмена и условиями их ..."Реакции ионного обмена"
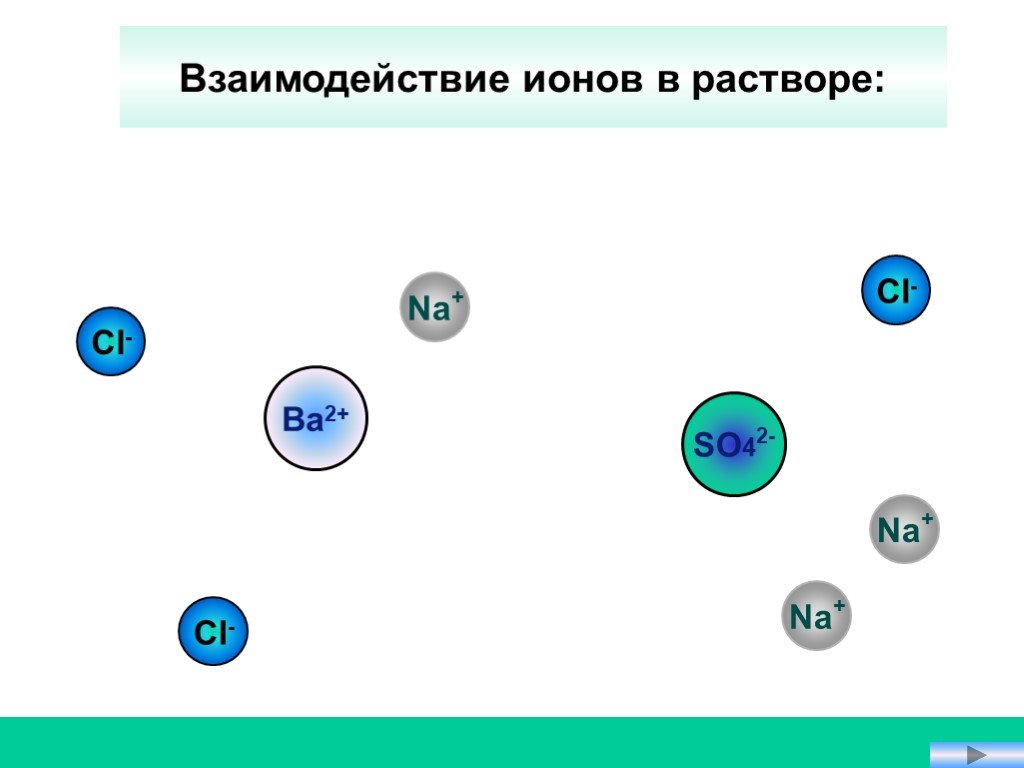
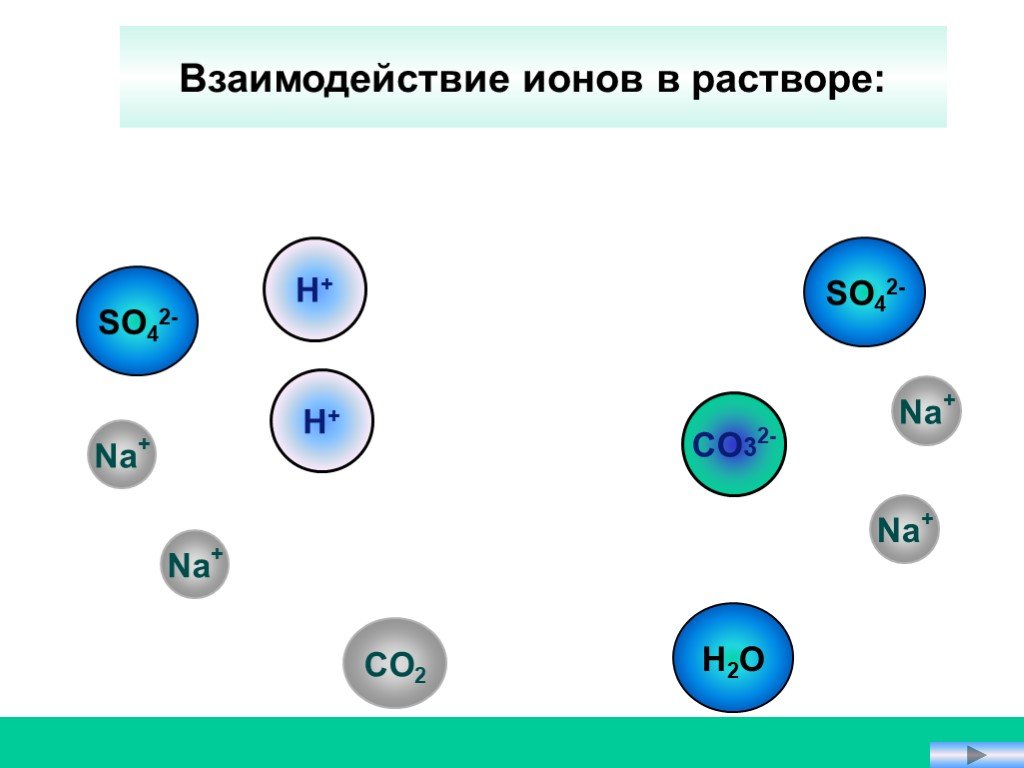
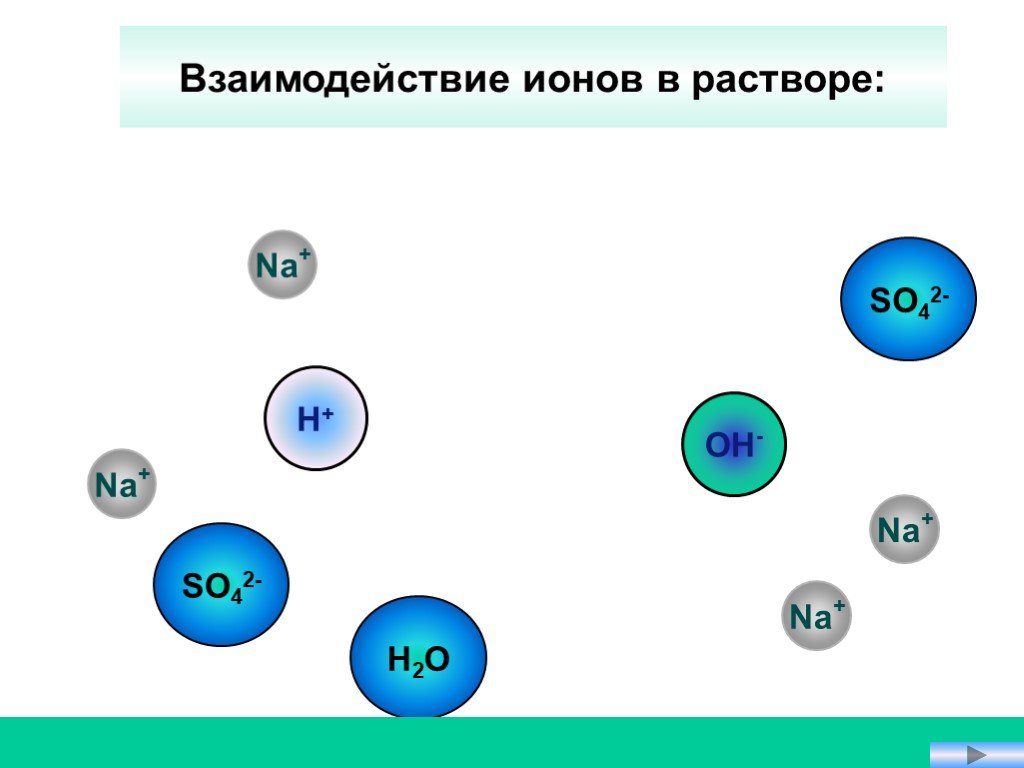
Реакции обмена протекают между ионами, поэтому они называются реакциями ионного обмена Реакции ионного обмена идут до конца в трех случаях. Если образуется ...Реакции ионного обмена. Ионные уравнения
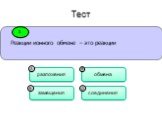
Определите тип данной реакции по числу и составу веществ вступивших и образующихся в реакции AqNO3 + HCl = AqCl + HNO3. реакция обмена. Технологическая ...Уравнения реакций ионного обмена
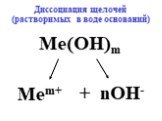
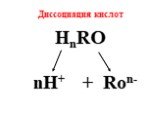
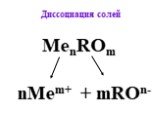
Реакции ионного обмена-. это реакции в водных растворах электролитов между ионами. Уравнения. реакций ионного обмена называют ионными уравнениями. ...Реакции обмена в водных растворах электролитов. Ионные реакции и уравнения
Ионные реакции – реакции протекающие между ионами в растворе. Порядок составления ионных уравнений реакции. 1. Записывают молекулярное уравнение реакции ...Химические уравнения. Реакции обмена
24.05.2019 Лебедева Л.В.Повторим изученный материал.
Какое слово зашифровано в таблице?
2Na+2HCl=2NaCl +H2↑ 2Al + 3S = Al2S3 Al(OH)3 = Al2O3 + ...
Реакции электрофильного замещения в ароматическом ряду
Реакции электрофильного замещения в ароматическом ряду. Ароматические соединения. Характерны реакции замещения, в первую очередь электрофильного, ...Реакции соединения
Карточка № 1. Явления. 1. При нагревании вода превращается в пар (физическое) 2. При сильном измельчении кусочек мела превращается в белый порошок ...Реакции разложения
Химическими реакциями называют такие превращения веществ, в результате которых образуются новые соединения и при этом не происходит образования новых ...Реакции окисления и восстановления органических соединений
Реакции окисления-восстановления реакции, в ходе которых происходит изменение степени окисления одного или нескольких атомов углерода. 4 (3)+(+1)= ...Патофизиология водно-солевого обмена
План лекции Содержание воды в организме. Распределение воды по секторам. Понятие о водном балансе организма. Формы нарушения водного баланса. Обезвоживание ...Взаимосвязь путей обмена веществ
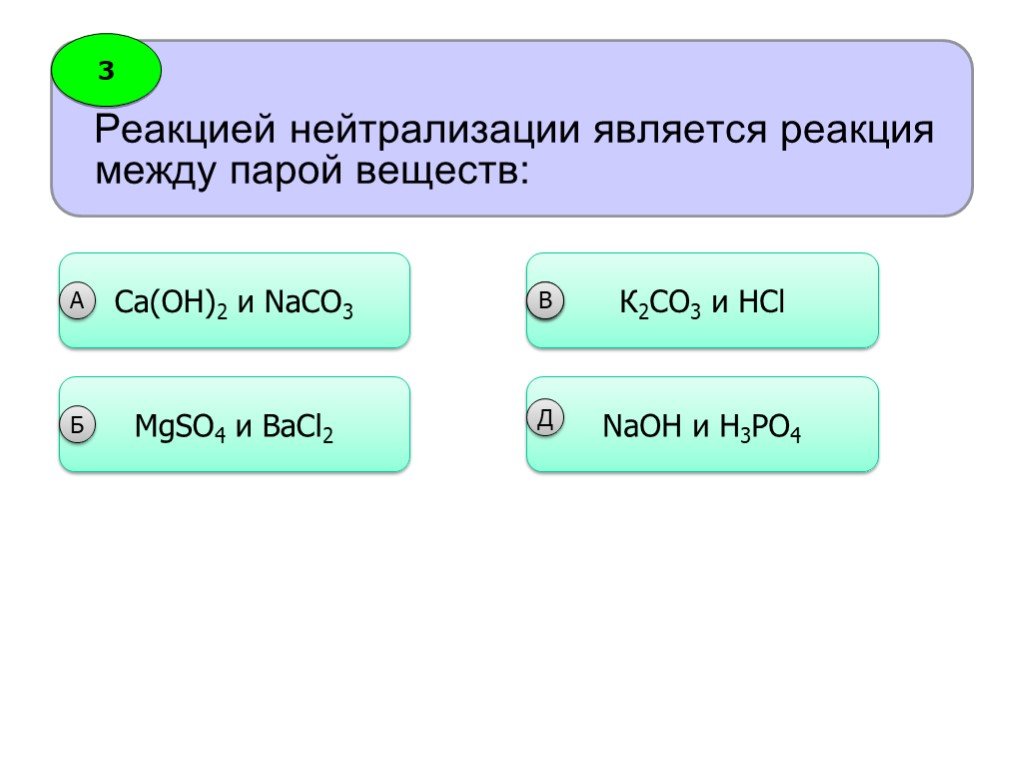
Включение безазотистого остатка аминокислот в общий путь катаболизма. Взаимосвязь гликолиза и гликонеогенеза. Гликонеогенез из липидов. дегидро-геназа. ..."Реакции нейтрализации"
Заполните таблицу. mв(NaCl) mp(NaCl) m(H2O) ω(NaCl) 20 г 80 г 100 г 120 г 200 г 40 % 15 г 135 г 150 г 10 % 01.11.2018. Ким Е.П., урок химии (УМК В.В. ...Реакции замещения. Электрохимический ряд напряжений.
Цель урока:. I. Дать понятие о реакциях замещения. II. Познакомить с: 1) электрохимическим рядом напряжений металлов; 2) условиями взаимодействия ...Реакции веществ
Цель создания данной работы – показать возможности использования мультимедийных технологий и интерактивной доски на уроках химии. Фрагменты презентаций ...Реакции в органической химии
Важнейшие реакции в органической химии. Типы химических реакций по числу и составу реагирующих веществ. . Виды органических реакций. . . . . . ...Реакции ароматического нуклеофильного замещения
Реакции ароматического нуклеофильного замещения. Реакции SNAr Ar-B + C- ArC + B-. Ароматические соединения. Характерны реакции замещения, в первую ...Пути обмена отдельных аминокислот
Фенилаланин – незаменимая аминокислота, так как в клетках животных не синтезируется ее бензольное кольцо, гликокетогенная. Тирозин – условнозаменимая ...Конспекты
Реакции ионного обмена и условия их протекания
Дата ______________ Класс_______________. Тема: Реакции ионного обмена и условия их протекания. Цели урока:. познакомить учащихся с ионными уравнениями ...Реакции ионного обмена и условия их протекания
Дата ______________ Класс_______________. Тема: Реакции ионного обмена и условия их протекания. Цели урока:. продолжить формирование навыков составления ...Реакции ионного обмена и условия их протекания
Тема урока:. Реакции ионного обмена и условия их протекания. Тип урока. : Урок новых знаний. Вид урока:. Проблемно – исследовательский. ...Реакции ионного обмена
. УРОК-ИССЛЕДОВАНИЕ ПО ТЕМЕ. . «Реакции ионного обмена» 9 класс. . Образовательные цели:. . Дать первоначальные знания о реакции ионного ...Реакции ионного обмена
Реакции ионного обмена. Цели урока:. обучающая. . – раскрыть суть протекания химических реакций в растворах электролитов; сформировать умение предвидеть ...Реакции обмена
МБОУ Ясенецкая СОШ. Павловский район. Нижегородская область. . Конспект урока. . Предмет : химия. Программа :. . О.С. Габриелян « ...Реакции обмена
Урок химии, 8 класс (базовый уровень). Учитель : Серебрякова Елена Васильевна. МОУ СОШ № 9,г.Георгиевска. Тема урока: Реакции обмена. Задачи:. ...Реакции обмена
Ф.И.О. автора. –. Желовникова Оксана Викторовна. . . Место работы - ГБОУ СОШ п. Комсомольский м.р. Кинельский Самарской области. Должность- ...Реакции обмена
Урок по химии для 8 класса по теме:. «Реакции обмена». Составлен учителем химии. МОУ «СОШ №5 г. Кировска». Зудковой Верой Сергеевной. Цель ...Реакции обмена. Реакция нейтрализации
Урок химии в 8 классе. по теме: «Реакции обмена. Реакция нейтрализации». Максимова Светлана Юрьевна, учитель химии. Цель урока:. . повторить ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:18 сентября 2018
Категория:Химия
Содержит:28 слайд(ов)
Поделись с друзьями:
Скачать презентацию