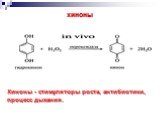
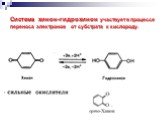
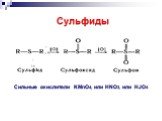
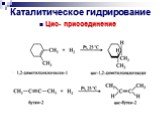
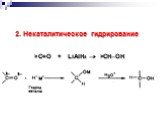
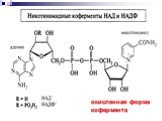
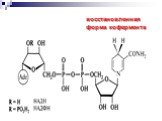
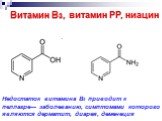
Презентация "Реакции окисления и восстановления органических соединений" по химии – проект, доклад
Презентацию на тему "Реакции окисления и восстановления органических соединений" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 76 слайд(ов).
Слайды презентации
Список похожих презентаций
Основные классы неорганических соединений. Генетическая связь между классами неорганических соединений
«ТРЕТИЙ ЛИШНИЙ». Поместите здесь ваш текст. Дайте название веществам и определите класс соединения:. Na OH SO2 Ca SO4 HCl. Проверка:. Классы неорганических ...Основные классы органических соединений организма человека
3 основные группы: (от количества составляющих мономеров). МОНОСАХАРИДЫ производные многоатомных спиртов, содержащие кроме гидроксильных групп, функциональную ...Важнейшие классы неорганических соединений
Оксид - сложное вещество, состоящее из атомов двух элементов, один из которых - кислород. Э Ме неМе + О2 ЭО-2. Гидроксиды — соединения оксидов химических ...Важнейшие классы неорганических соединений
Цели урока:. ВОСпитывающая. Формирование интереса к умению, создание положительной атмосферы, воспитание взаимного уважения между учащимися, для раскрытия ...Основные классы неорганических соединений. Генетическая связь между классами неорганических соединений
Девиз урока! Все знать, изведать, испытать! Путешествие на подводной лодке «Генезис". соляндия. основайские острова. кислотостан оксидония. Работа ...Химические раскопки по классам неорганических соединений
Раскопки по холмам. Холм Знаний Холм Умений Холм Творчества Холм Памяти. Цель урока:. 1) повторить и систематизировать имеющиеся у вас знания об основных ...Генетические связи между важнейшими классами неорганических соединений
Тема. Генетические связи между важнейшими классами неорганических соединений. А. С. Макаренко: «Теория и практика неотъемлемы». . SO2 HCl H3PO4 H2O ...Взаимосвязь между классами неорганических соединений
19.02.2019 Оськина Т.А. Даны схемы превращений. Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. ...Основные классы неорганических соединений. Генетическая связь между классами неорганических соединений
Девиз урока! Думай, работай, ищи, трудно будет -не пищи! Путешествие на подводной лодке «Генезис". соляндия основайские оксидония кислотостан. Работа ...Теория строения органических соединений
Например: Сбраживая виноградный сок, получали вино, а при его перегонке - спирт; Нагревая жир с содой, получали мыло; Из цветов извлекали эфирные ...Теория строения строения органических соединений
Первые теории строения органических соединений. Органическая химия в начале XIX века: Ученые определяли количественный и качественный состав вещества. ...Теория строения органических соединений А.М. Бутлерова
Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма). В состав органических веществ входят радикалы;. Радикалы всегда постоянны, не подвергаются ...Классификация и номенклатура неорганических соединений
ОТВЕТИТЬ НА ПРЕДЛОЖЕННЫЕ ВОПРОСЫ В ПОРЯДКЕ ИХ ПОСТАНОВКИ. Вариант 1 Основания – это… Кислотные оксиды – это … С водой реагирую только оксиды металлов ...Теория строения органических соединений А. М. Бутлерова
Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма). В состав органических веществ входят радикалы;. Радикалы всегда постоянны, не подвергаются ...Строение органических соединений А.М. Бутлерова
Биография А.М.Бутлерова Теория химического строения органических веществ Предпосылки создания теории Теории до Бутлерова Основные положения теории ...Классы неорганических соединений
Оксиды. Образованы двумя химическими элементами Один из элементов кислород, имеющий степень окисления -2 Примеры: MgO, H2O. Оксидами являются оба ...Классы неорганических соединений
Чем объединены и чем отличаются перечисленные соединения:. Na SO ВаCl Cu(NO ) K PO K S CaSiO 3 4. Cоли – это сложные вещества, состоящие из атомов ...Классификация органических соединений
Органическая химия – химия углеводородов и их функциональных производных. органические вещества. углеводороды. функциональные производные углеводородов. ...Классы неорганических соединений
Почему у фруктов кислый вкус? Вы любите фрукты? Что такое КИСЛОТА? Какие бывают КИСЛОТЫ? Кислоты. Состав и классификация. урок по химии 8 класс. Цель ...Классификация органических соединений
Классификация. Органические вещества. Углеводороды СхНу. Кислородсодержащие. Азотсодержащие Углеводы предельные непредельные Алканы СnH2n+2 Алкины ...Конспекты
Качественные реакции кислородсодержащих органических соединений
Практическая работа. Тема: «Качественные реакции кислородсодержащих органических соединений». Цели:. . обучающая. : закрепить знания о кислородсодержащих ...Степень окисления. Реакции окисления – восстановления
Урок- упражнение , 8 класс. Степень окисления. Реакции окисления – восстановления. . . Цели урока:. Образовательные:. - повторить основные ...Основные классы неорганических соединений
План-конспект учебного занятия по химии. Автор:. Серова Елена Петровна. Класс:. 8. Тема:. Основные классы неорганических соединений. Форма ...Основные классы неорганических соединений
Урок в 8 классе. Тема:. «Основные классы неорганических соединений». Цель урока:. систематизация и обобщение знаний учащихся об основных классах ...Важнейшие классы неорганических соединений
ГБОУ СОШ пос. Сургут муниципального района Сергиевский Самарской области . . ПЛАН-КОНСПЕКТ УРОКА. . по химии в 8 классе Важнейшие ...Важнейшие классы неорганических соединений
МОУ Кинель – Черкасская средняя общеобразовательная школа № 1. «Образовательный центр». Конспект. . открытого урока по химии в 8 ...Важнейшие классы неорганических соединений
Урок – игра по теме: «Важнейшие классы неорганических соединений». Класс: 8. ФИО: Тимохина Алёна Владимировна. Должность: Учитель Химии. Место ...Теория строения органических соединений
тест Теория строения органических соединений. 1. Верны ли следующие суждения о понятиях «химическое строение» и «изомерия»? А. Химическое ...Основные классы неорганических соединений
Урок-повторение по теме. «Основные классы неорганических соединений». Цель урока:. систематизировать знания учащихся по теме «Основные классы ...Теория химического строения органических соединений А. М. Бутлерова
МАВ(С)ОУ вечерняя (сменная) общеобразовательная школа № 13 города тюмени. . . Теория химического строения органических соединений А. М. Бутлерова. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:9 ноября 2018
Категория:Химия
Содержит:76 слайд(ов)
Поделись с друзьями:
Скачать презентацию








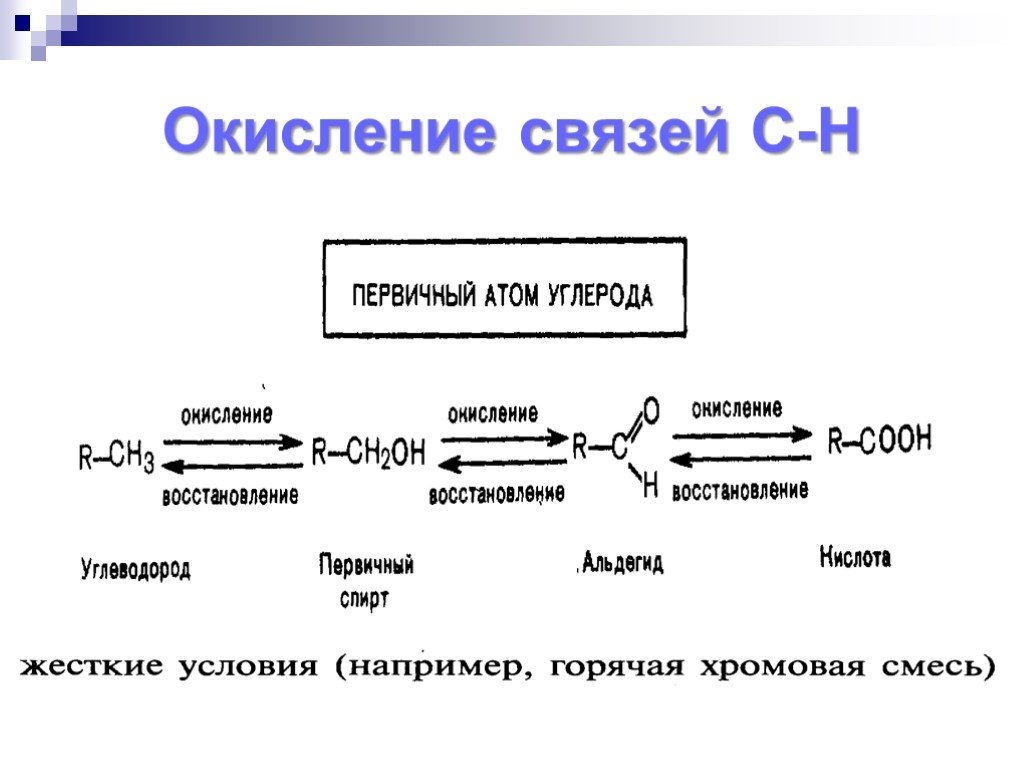
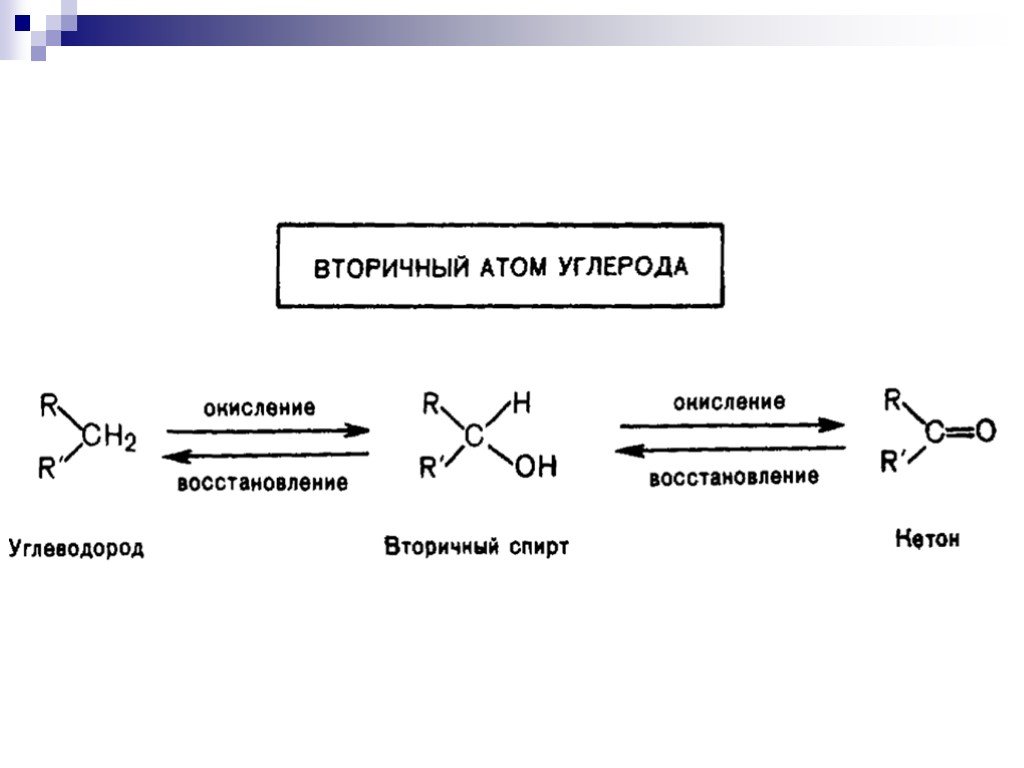
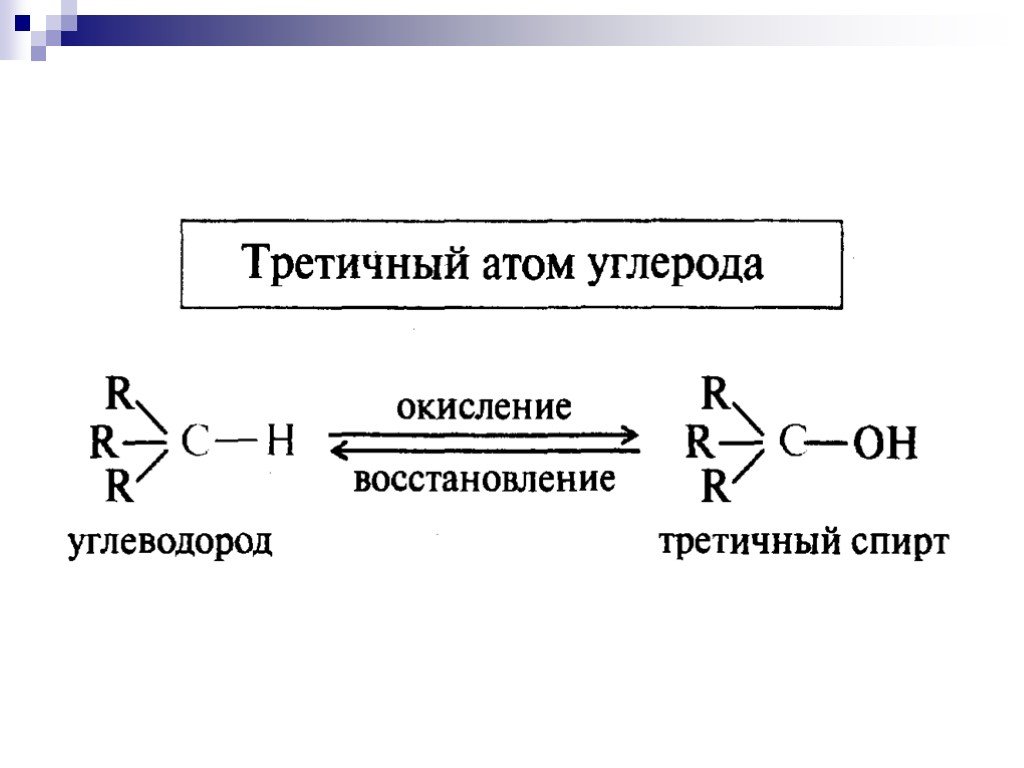
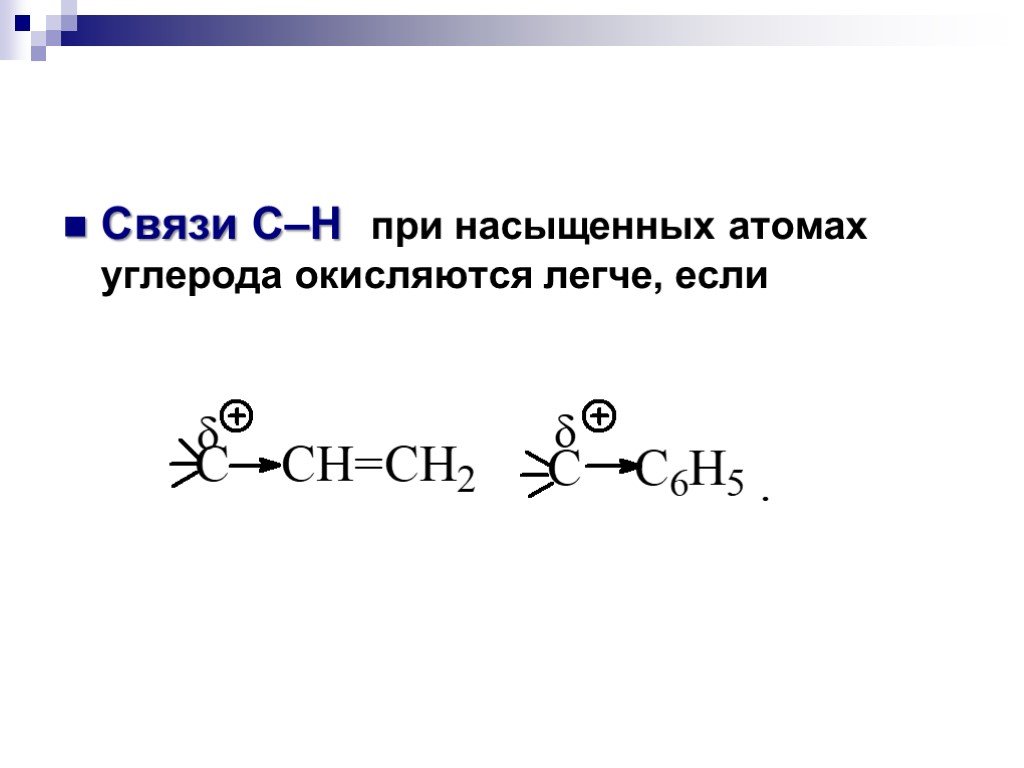


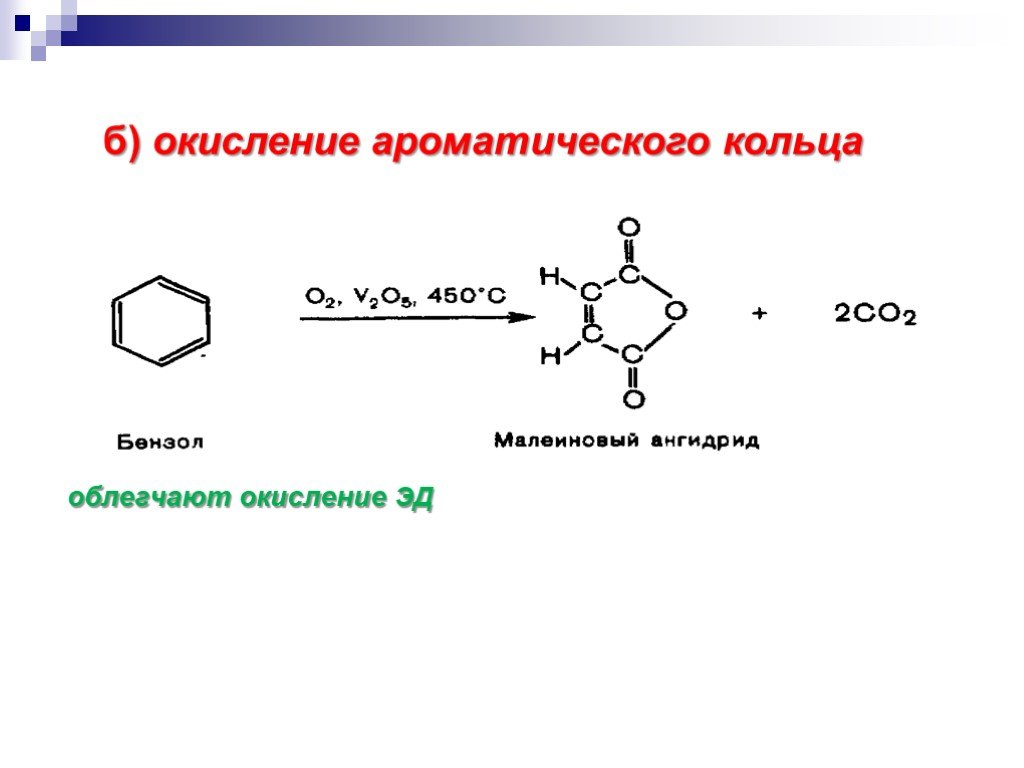
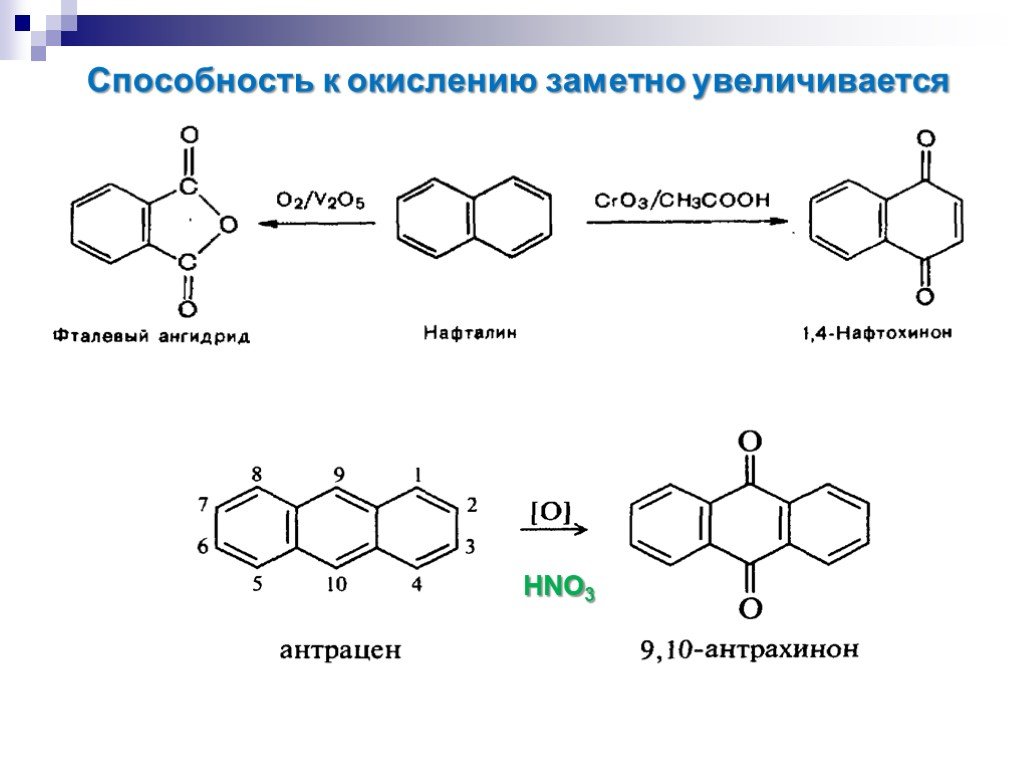
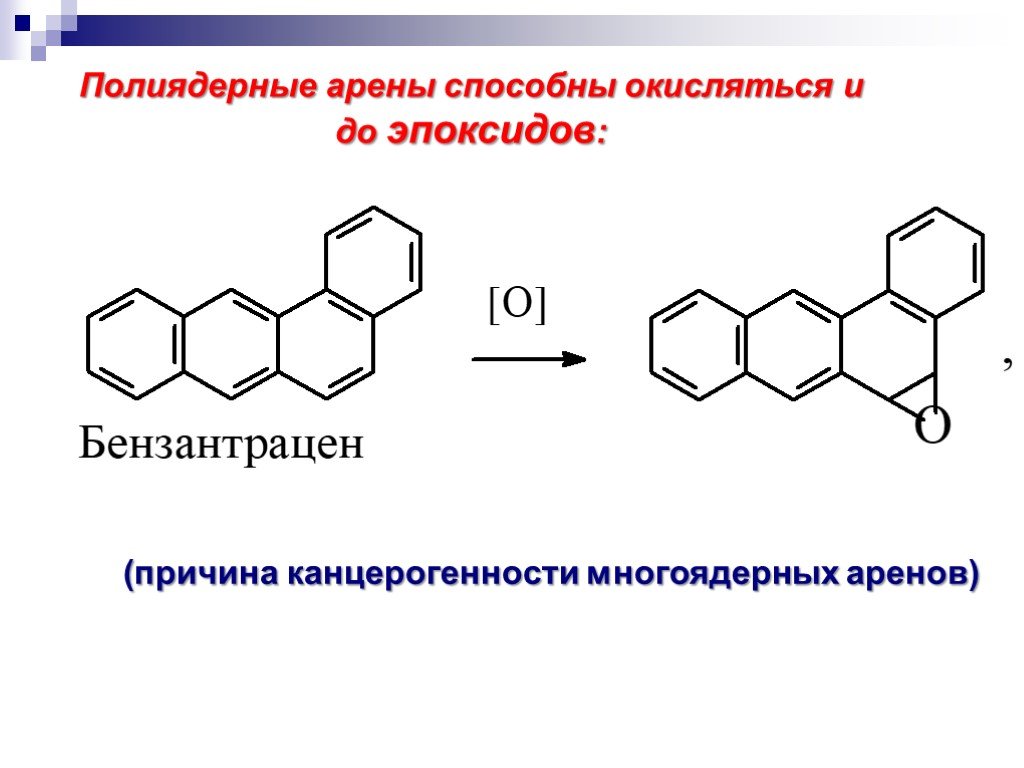
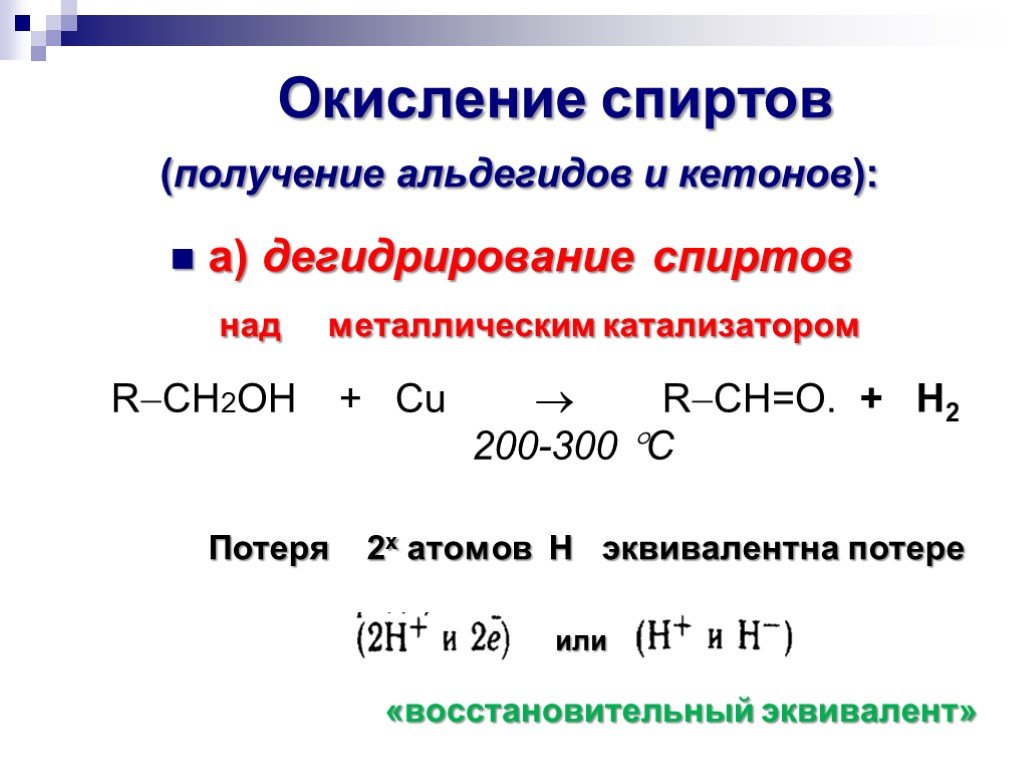

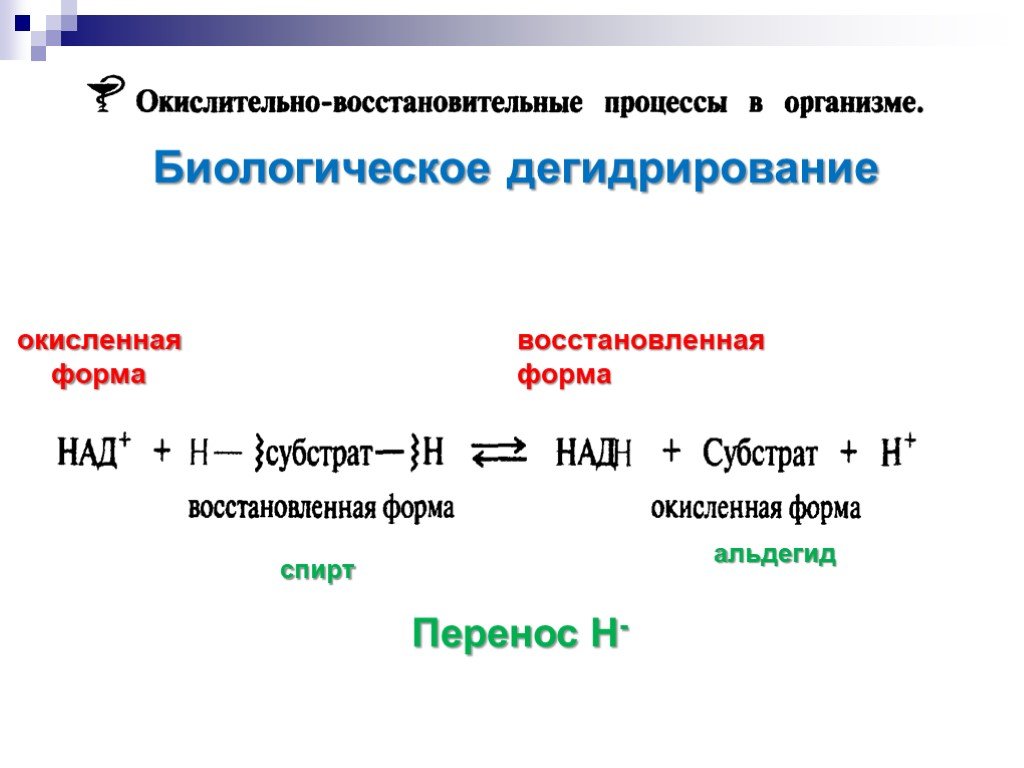
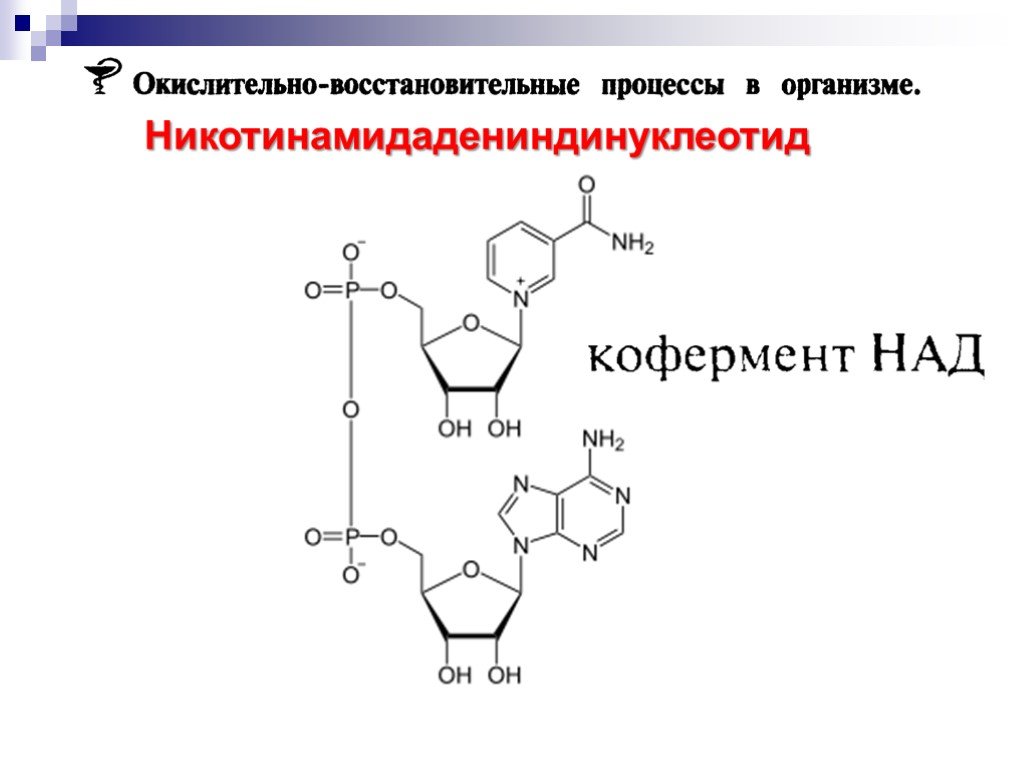
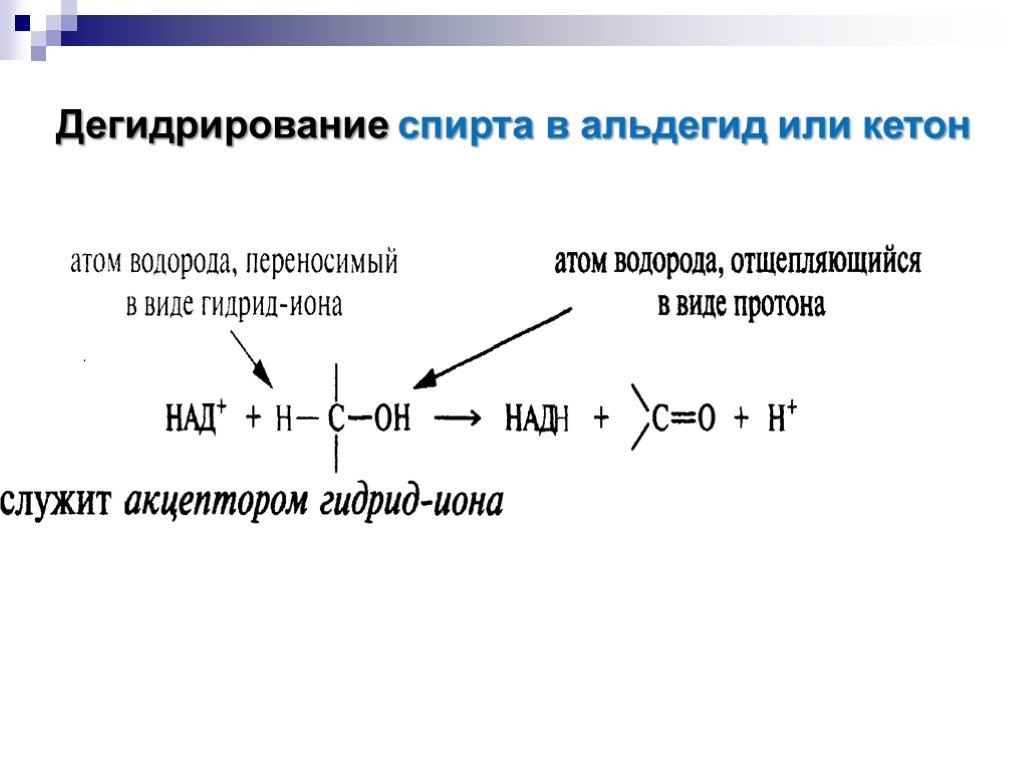

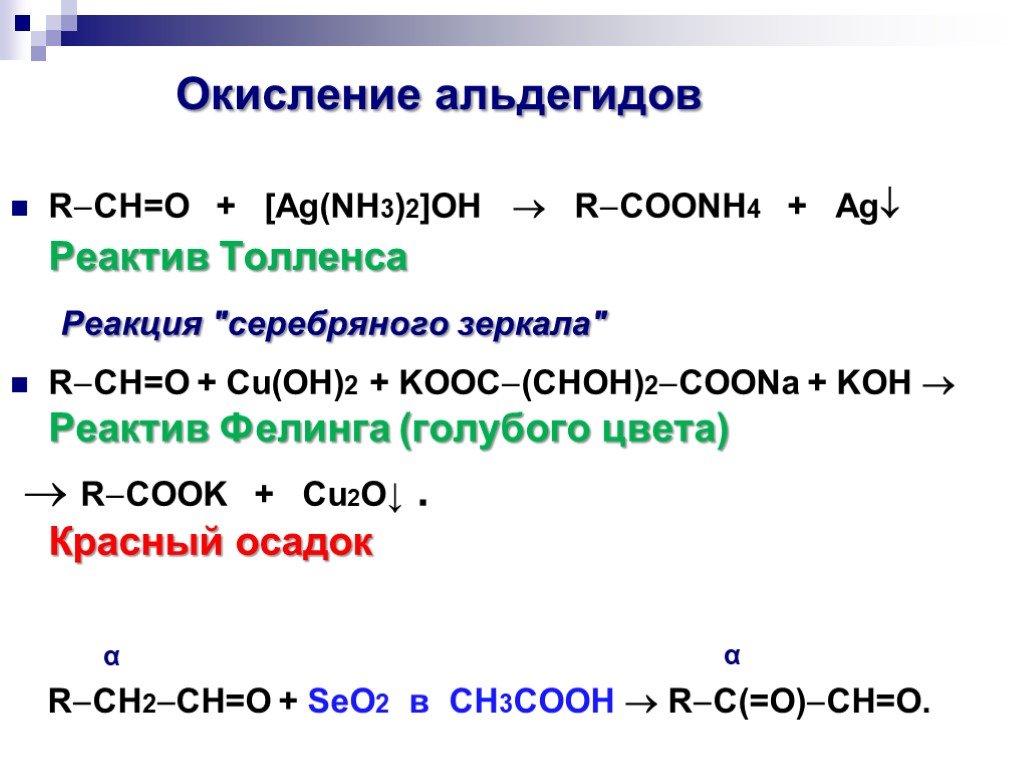

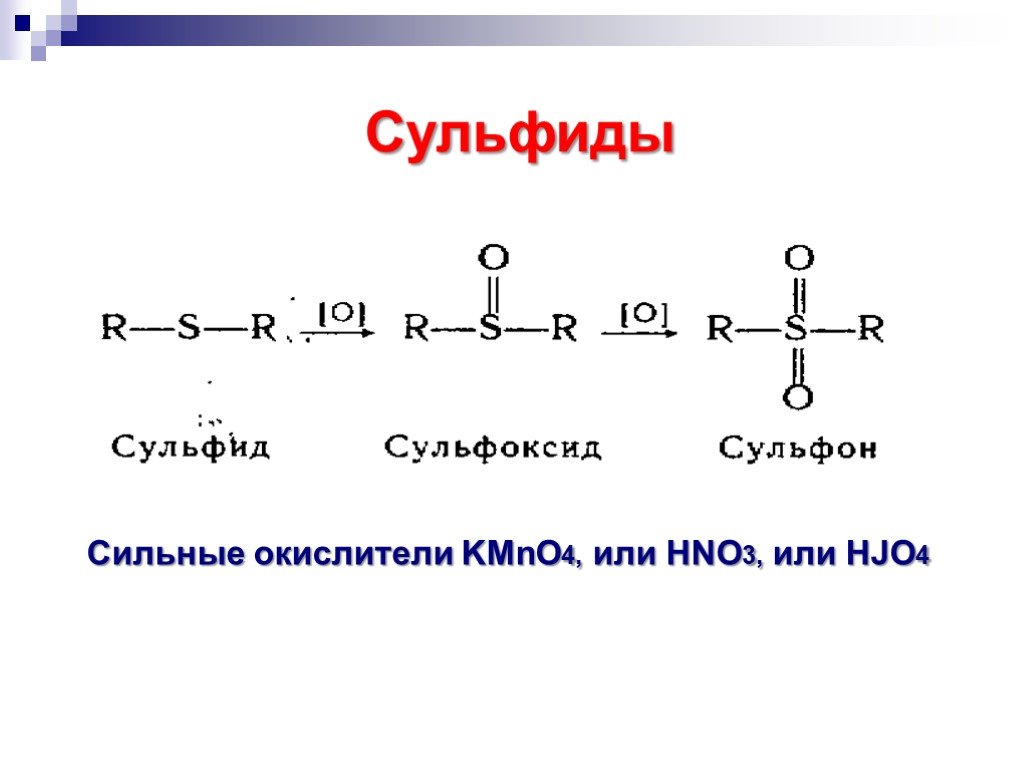

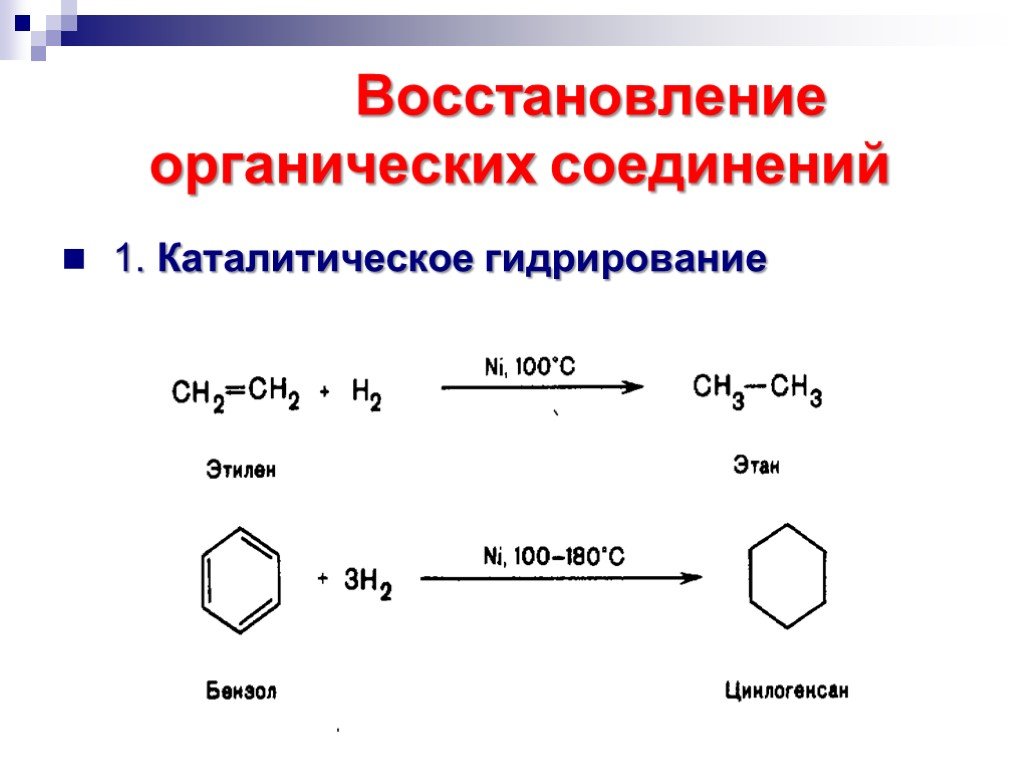
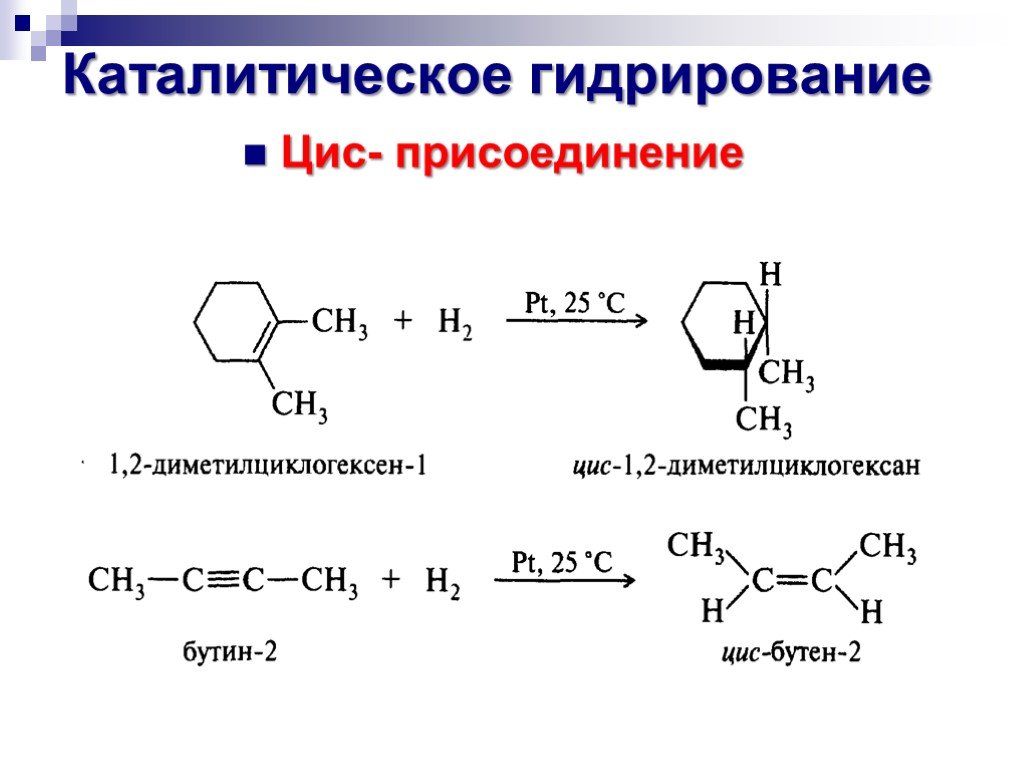
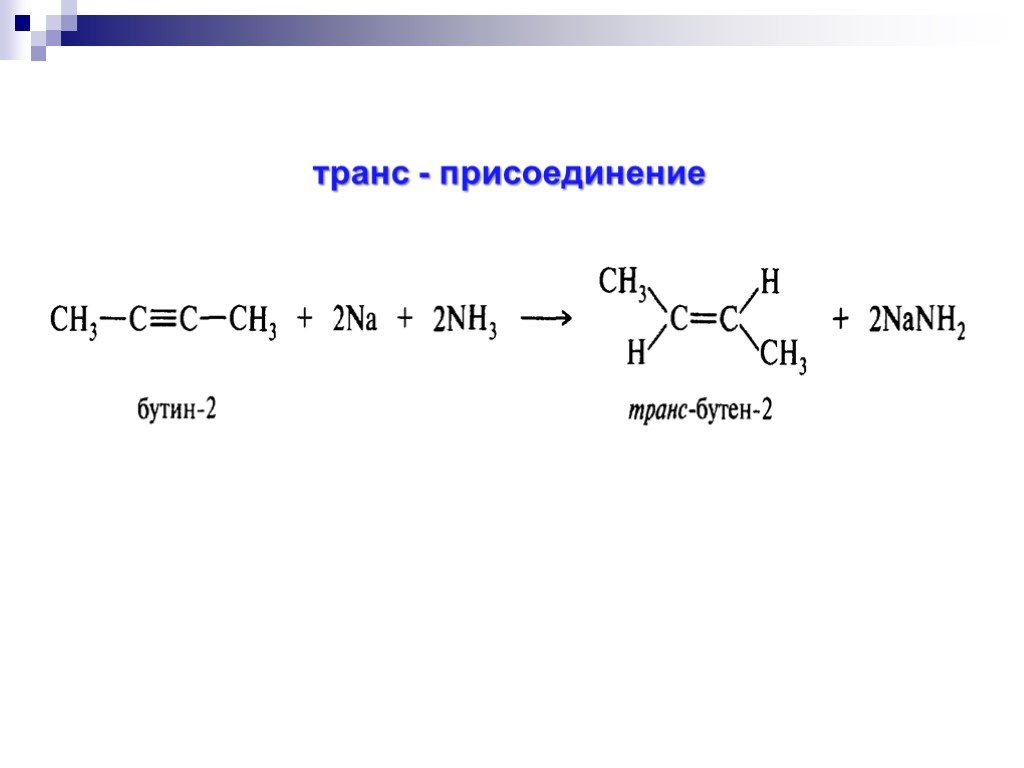
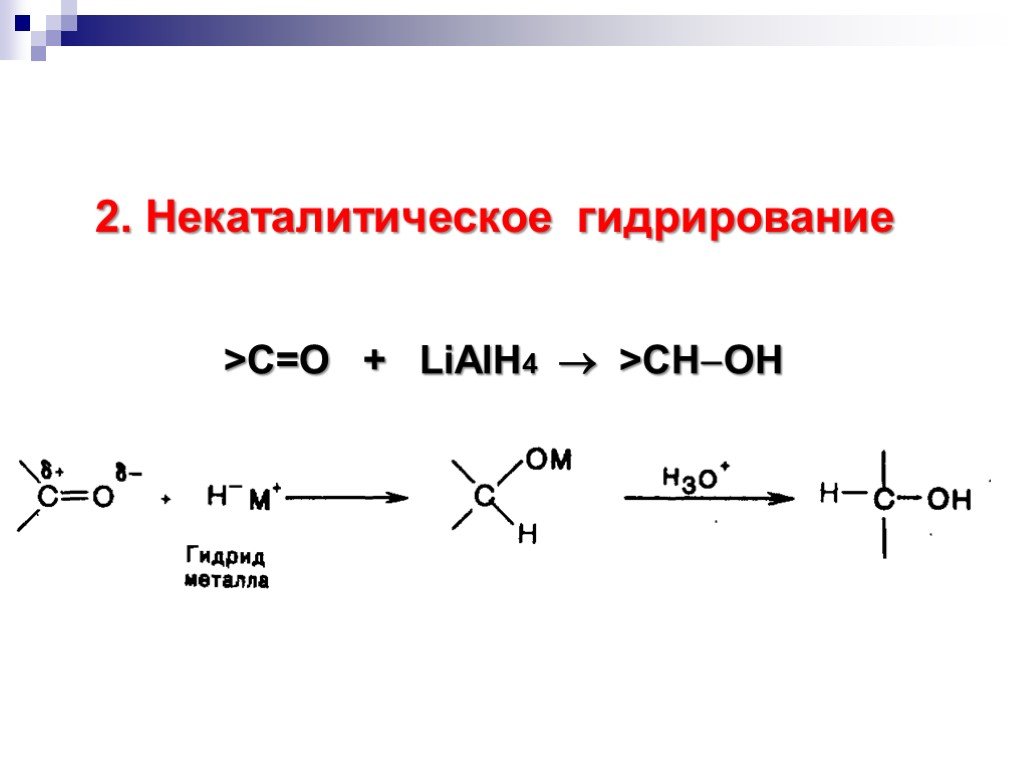
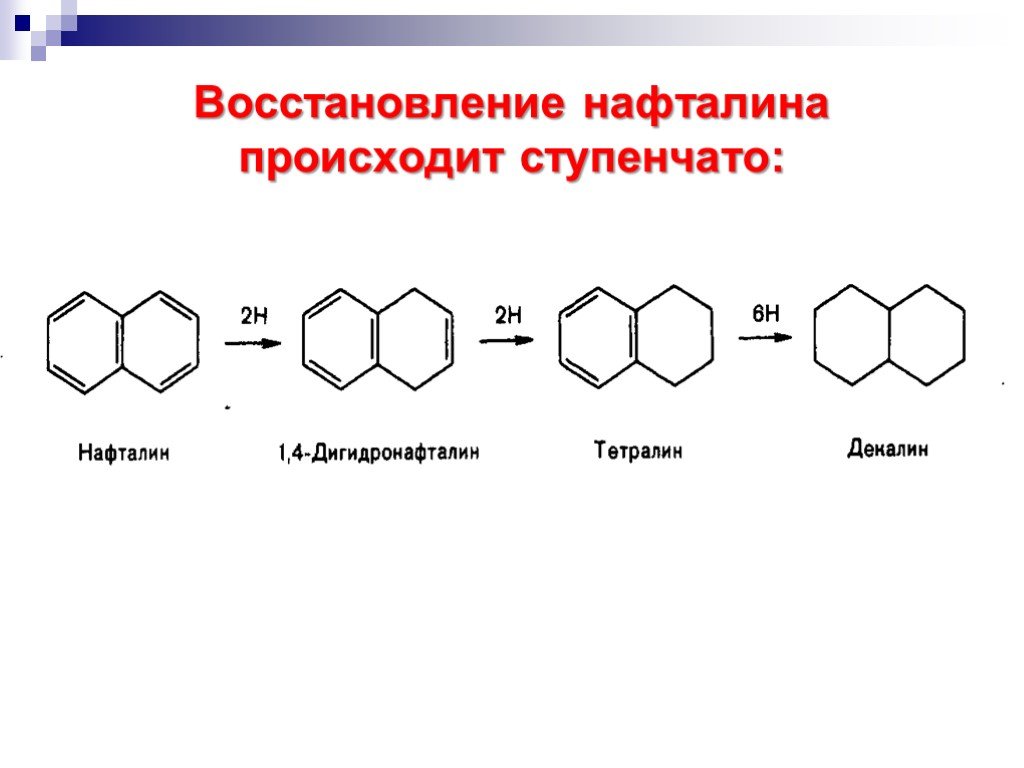
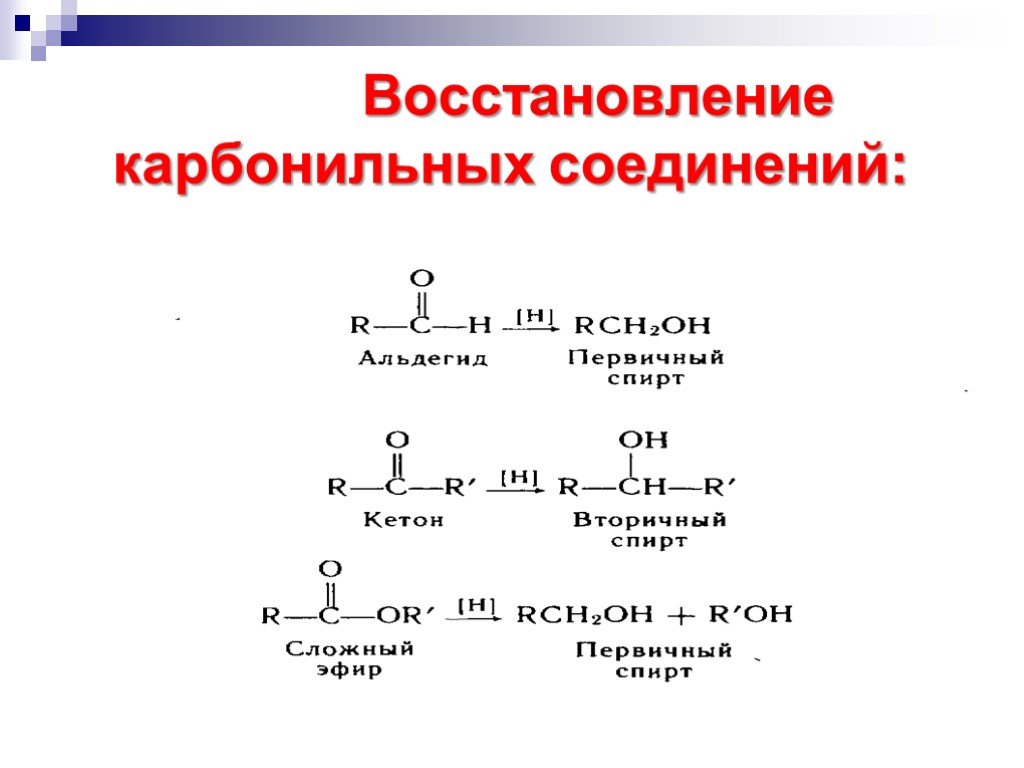
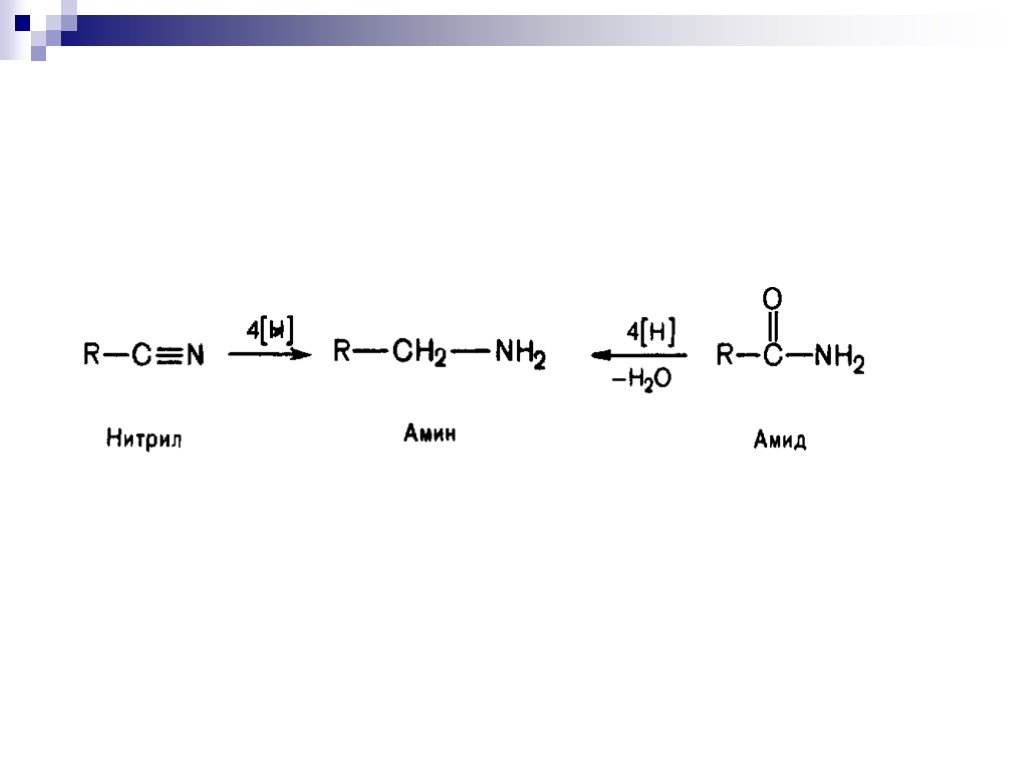
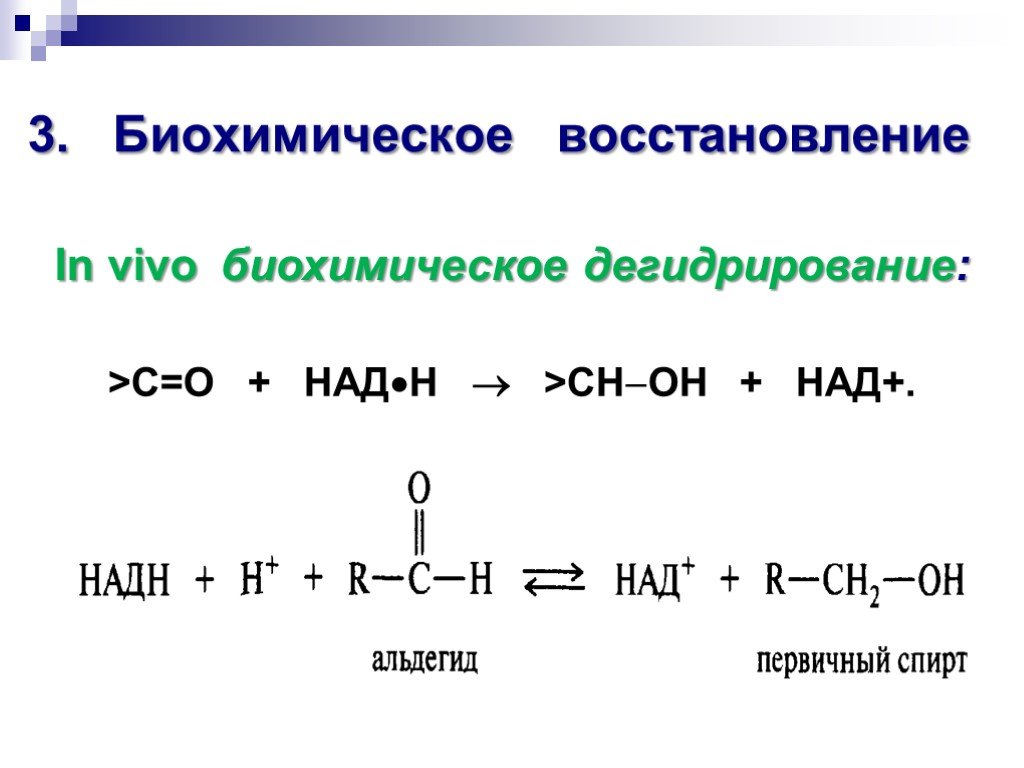


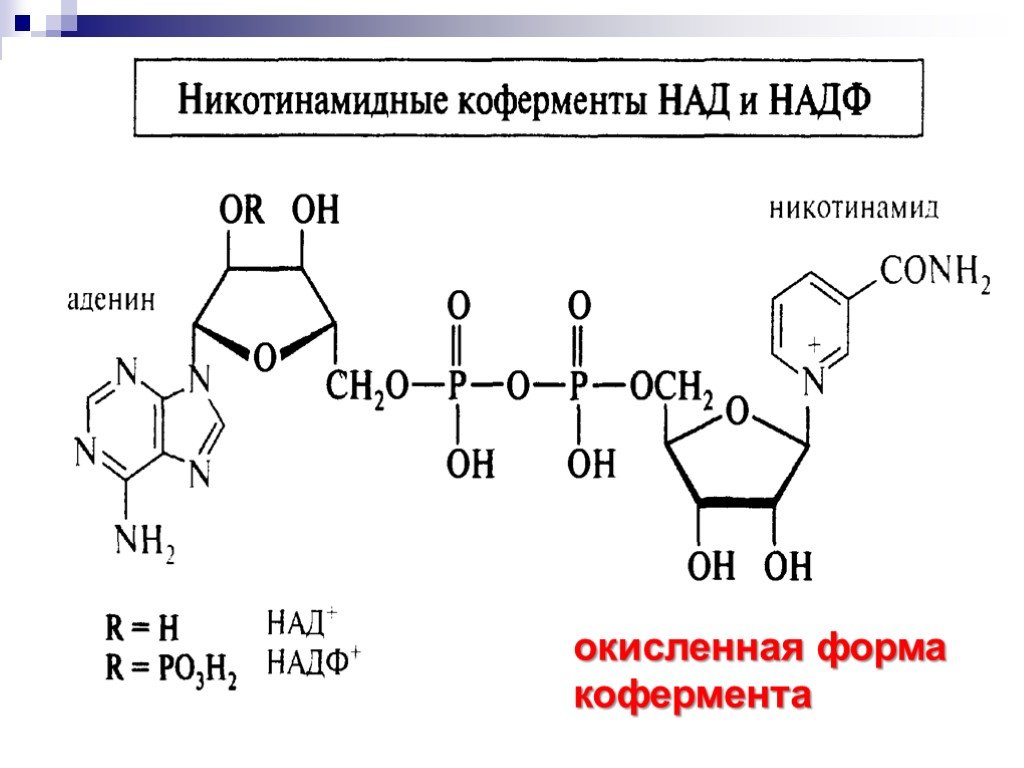
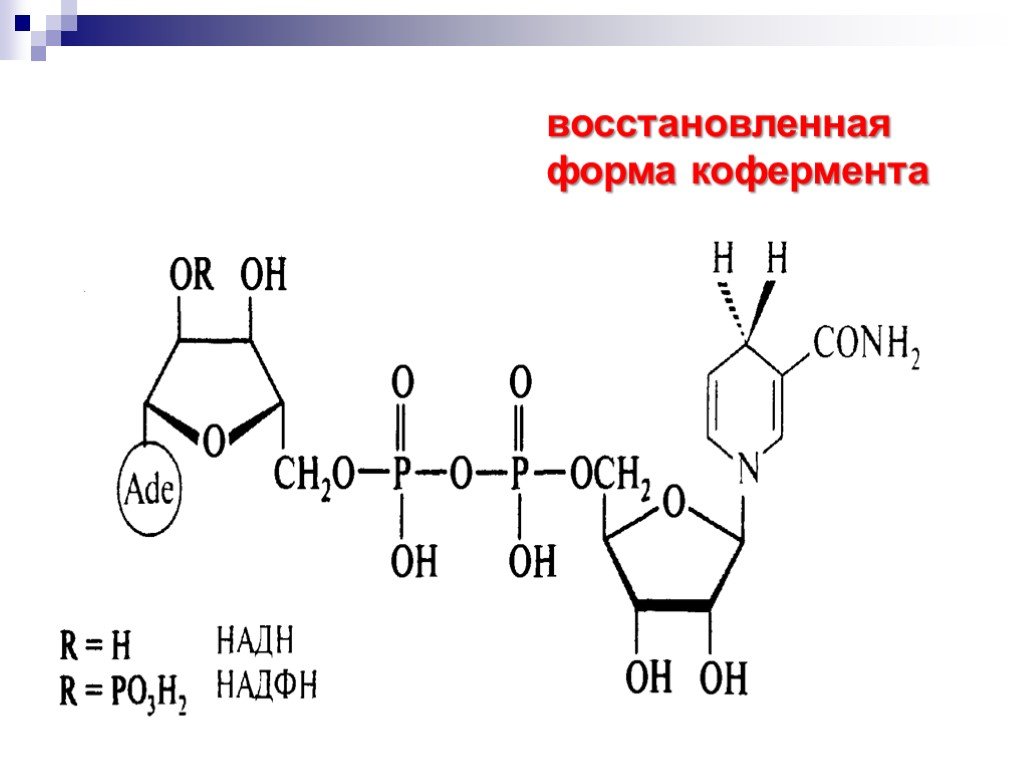
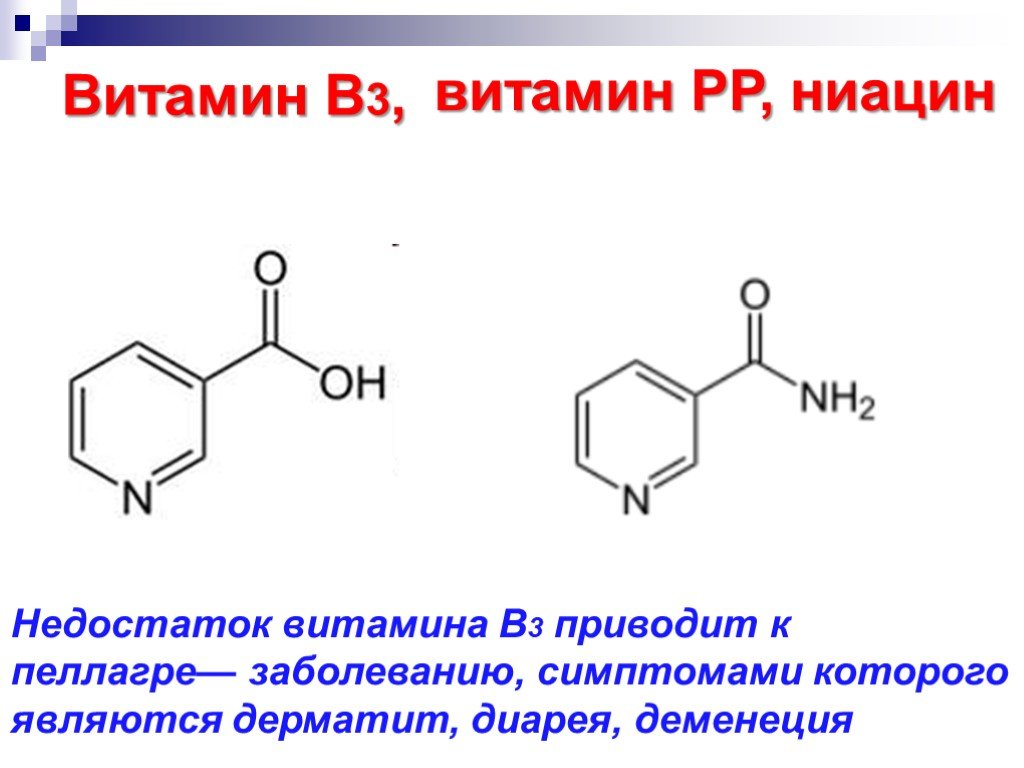
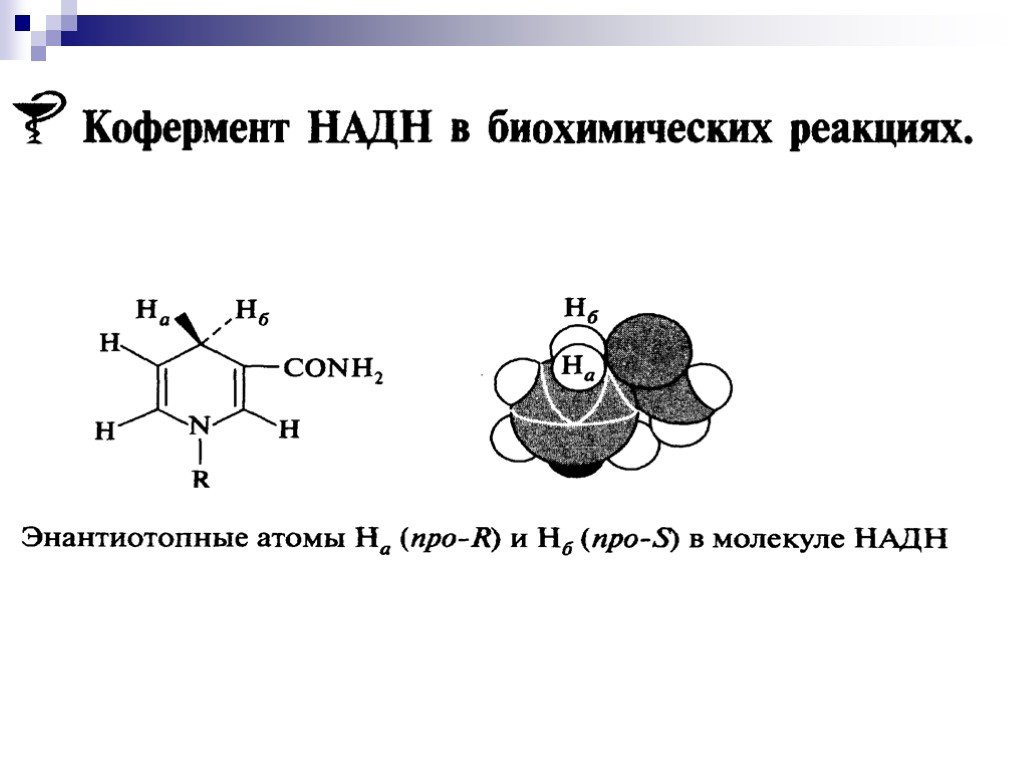
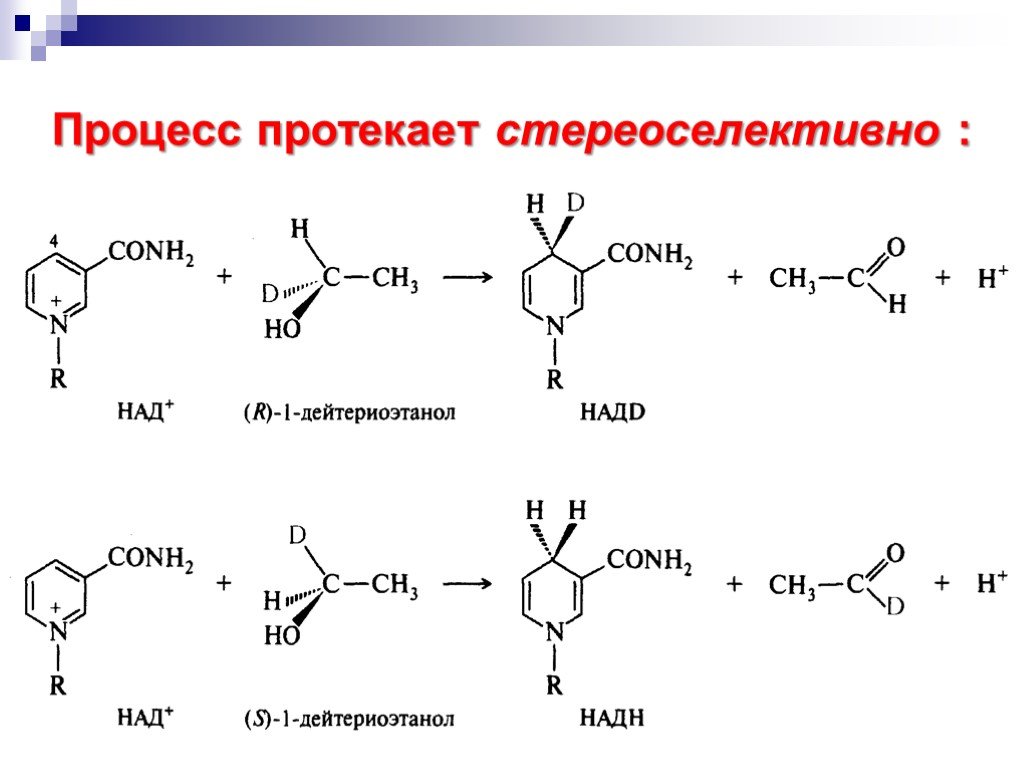
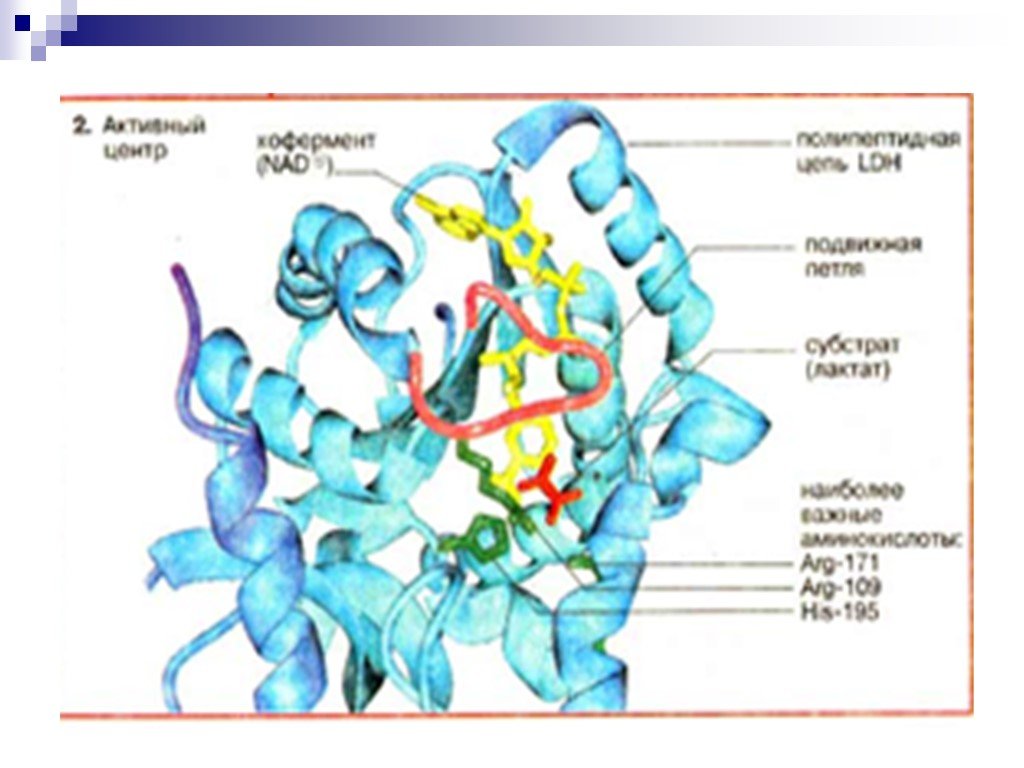
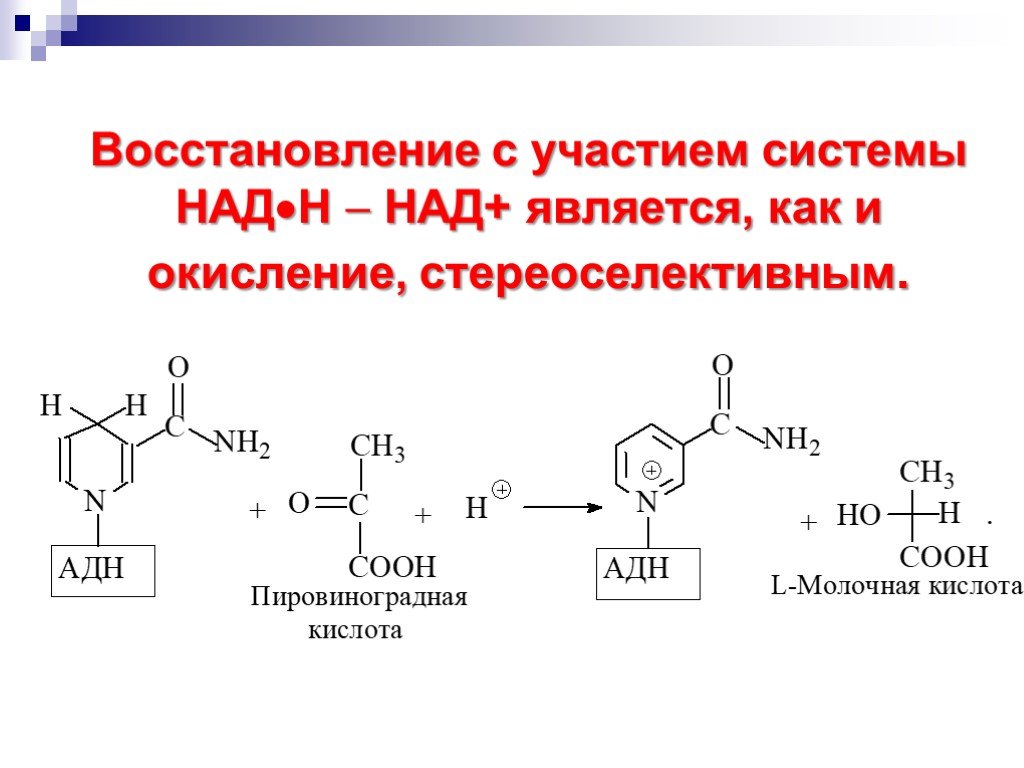






























![Окисление альдегидов. RCH=O + [Ag(NH3)2]OH RCOONH4 + Ag Реактив Толленса Реакция "серебряного зеркала" RCH=O + Cu(OH)2 + KOOC(CHOH)2COONa + KOH Реактив Фелинга (голубого цвета) RCOOK + Cu2O↓ . Красный осадок. RCH2CH=O + SeO2 в CH3COOH RC(=O)CH=O. α Окисление альдегидов. RCH=O + [Ag(NH3)2]OH RCOONH4 + Ag Реактив Толленса Реакция "серебряного зеркала" RCH=O + Cu(OH)2 + KOOC(CHOH)2COONa + KOH Реактив Фелинга (голубого цвета) RCOOK + Cu2O↓ . Красный осадок. RCH2CH=O + SeO2 в CH3COOH RC(=O)CH=O. α](https://prezentacii.org/upload/cloud/18/11/98609/images/thumbs/screen33.jpg)

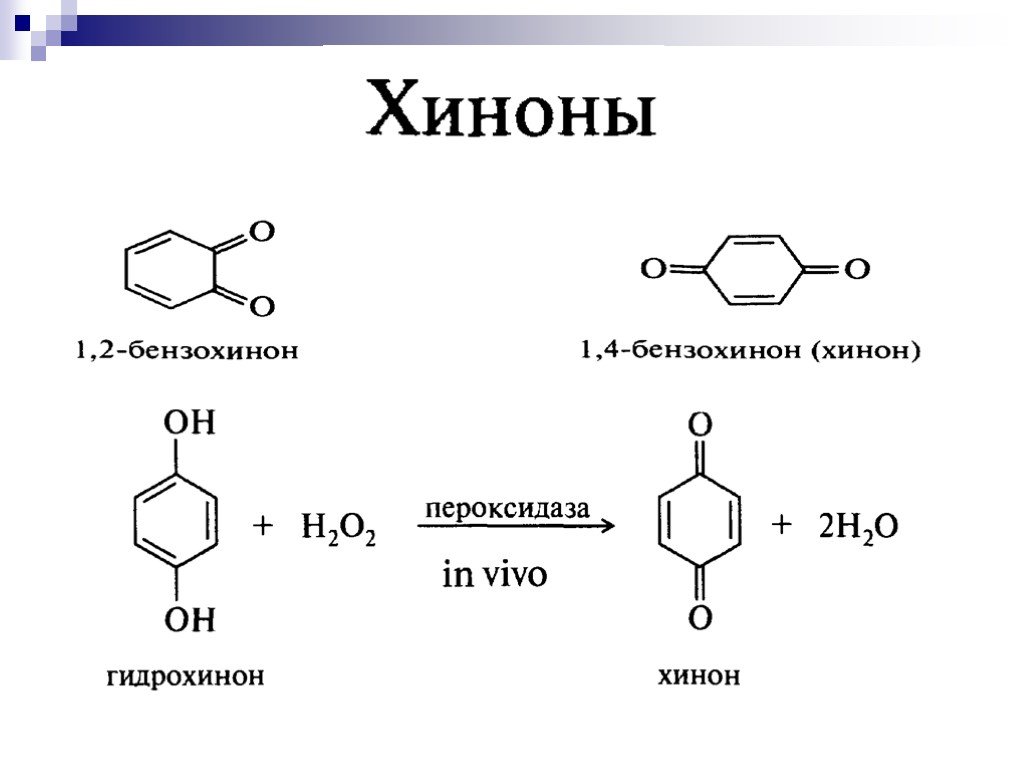
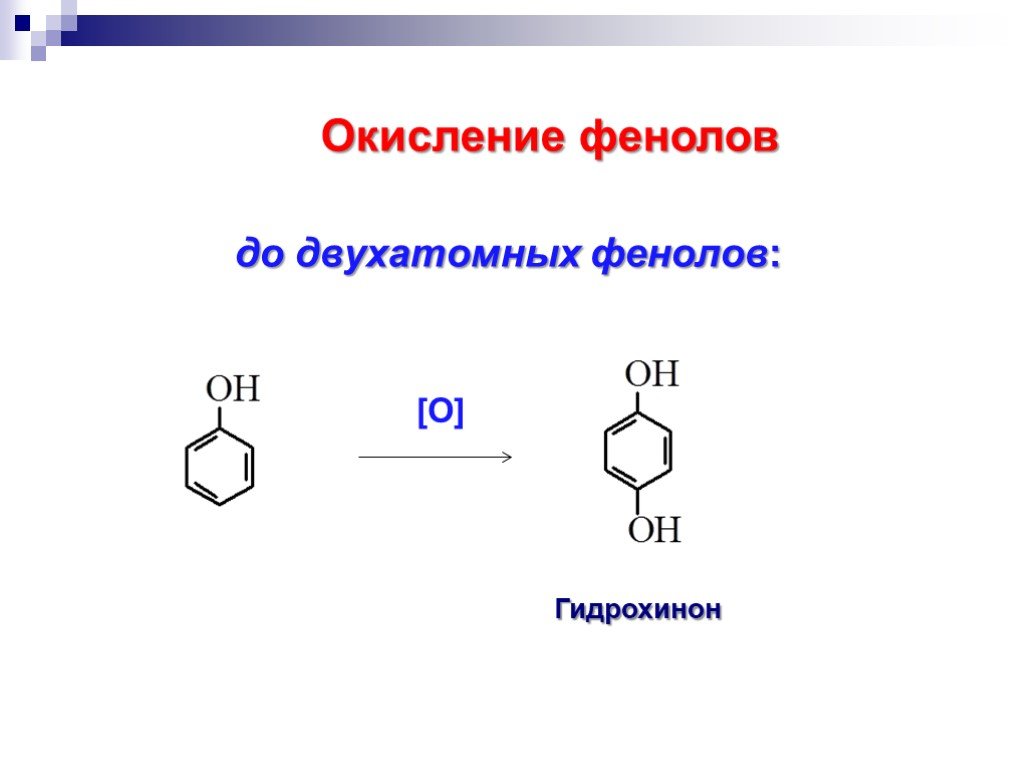
![до двухатомных фенолов: Гидрохинон. Окисление фенолов. [O] до двухатомных фенолов: Гидрохинон. Окисление фенолов. [O]](https://prezentacii.org/upload/cloud/18/11/98609/images/thumbs/screen35.jpg)