Презентация "Теория строения органических соединений А.М. Бутлерова" по химии – проект, доклад
Презентацию на тему "Теория строения органических соединений А.М. Бутлерова" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 18 слайд(ов).
Слайды презентации
Список похожих презентаций
Теория химического строения органических веществ А.М. Бутлерова
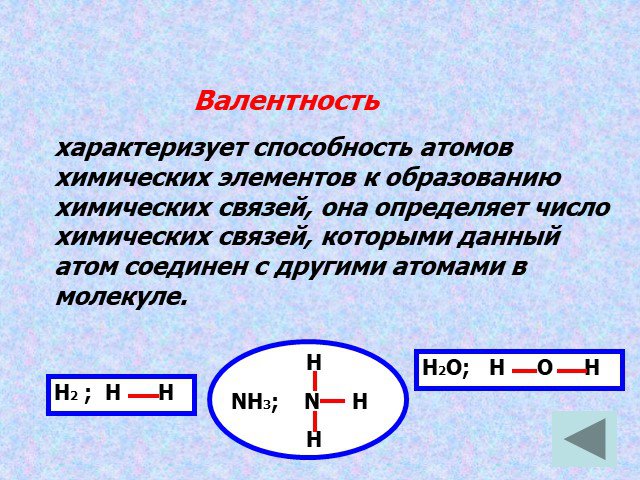
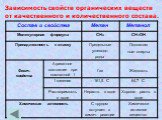
Важнейшем открытием в органической химии в середине 19 века явилось то, что углерод, как правило, четырёхвалентен (1857 г.), были известны СН4, С2Н2, ...Теория строения химических соединений А.М.Бутлерова
Бутлеров Александр Михайлович (1828-1886). Русский химик, академик Петербургской АН (с 1874 г.). Окончил Казанский университет (1849 г.). Работал ...Теория строения химических соединений А.М. Бутлерова
Оглавление Биография А.М. Бутлерова; Основные положения теории строения химических соединений; Первое положение; Второе положение; Третье положение; ...Теория строения органических соединений А. М. Бутлерова
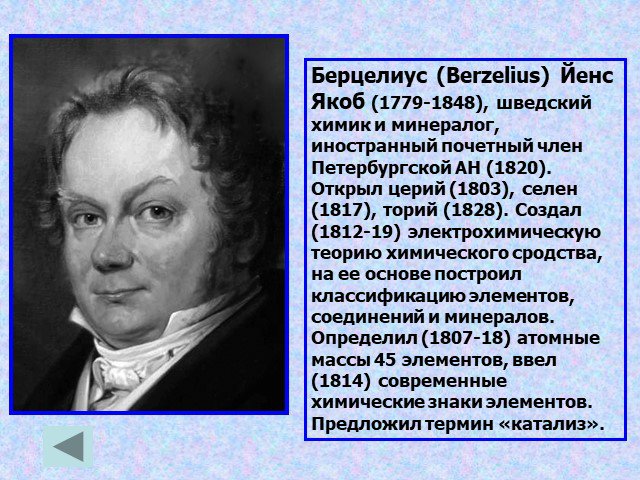
Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма). В состав органических веществ входят радикалы;. Радикалы всегда постоянны, не подвергаются ...Теория строения строения органических соединений
Первые теории строения органических соединений. Органическая химия в начале XIX века: Ученые определяли количественный и качественный состав вещества. ...Строение органических соединений А.М. Бутлерова
Биография А.М.Бутлерова Теория химического строения органических веществ Предпосылки создания теории Теории до Бутлерова Основные положения теории ...Основы строения органических соединений. Теория строения органических соединений
К первой половине XIX века в органической химии был накоплен громадный фактический материал, дальнейшее изучение которого тормозилось отсутствием ...Теория строения органических соединений
Например: Сбраживая виноградный сок, получали вино, а при его перегонке - спирт; Нагревая жир с содой, получали мыло; Из цветов извлекали эфирные ...Теория химического строения органических веществ
"Просто знать - мало, знания нужно уметь использовать" Гёте. Кластер ОО. Органическая химия. Органические вещества. Теория химического строения. Валентные ...Современные методы установления строения органических соединений
Современные методы установления строения органических соединений. Аналитические методы. Качественный и количественный элементный анализ Определение ...Теория строения Бутлерова
Цели и задачи :. понимание специфики естественнонаучного и гуманитарного компонентов культуры, ее связей с особенностями мышления; формирование представлений ...Классы неорганических соединений
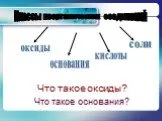
Оксиды. Образованы двумя химическими элементами Один из элементов кислород, имеющий степень окисления -2 Примеры: MgO, H2O. Оксидами являются оба ...Классы неорганических соединений
Почему у фруктов кислый вкус? Вы любите фрукты? Что такое КИСЛОТА? Какие бывают КИСЛОТЫ? Кислоты. Состав и классификация. урок по химии 8 класс. Цель ...Классификация органических соединений
Органическая химия – химия углеводородов и их функциональных производных. органические вещества. углеводороды. функциональные производные углеводородов. ...Классификация органических соединений
Классификация. Органические вещества. Углеводороды СхНу. Кислородсодержащие. Азотсодержащие Углеводы предельные непредельные Алканы СnH2n+2 Алкины ...Классификация органических соединений
Классификация соединений по строению углеродной цепи. Ациклические соединения - соединения с открытой (незамкнутой) углеродной цепью. Эти соединения ...Классификация органических соединений
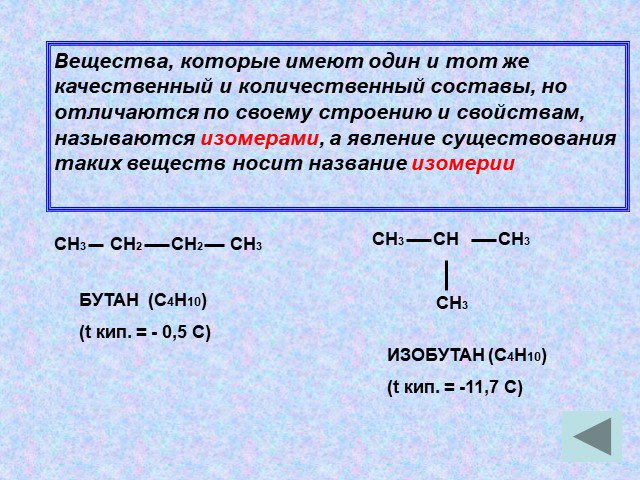
II Наличие в молекуле функциональной группы. Виды изомерии. Объект воздействия на реагент. БЛАГОДАРЮ ЗА ВНИМАНИЕ. ...Важнейшие классы неорганических соединений
Цели урока:. ВОСпитывающая. Формирование интереса к умению, создание положительной атмосферы, воспитание взаимного уважения между учащимися, для раскрытия ...Важнейшие классы неорганических соединений
Оксид - сложное вещество, состоящее из атомов двух элементов, один из которых - кислород. Э Ме неМе + О2 ЭО-2. Гидроксиды — соединения оксидов химических ...Взаимосвязь между классами неорганических соединений
19.02.2019 Оськина Т.А. Даны схемы превращений. Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. ...Конспекты
Теория химического строения органических соединений А. М. Бутлерова
МАВ(С)ОУ вечерняя (сменная) общеобразовательная школа № 13 города тюмени. . . Теория химического строения органических соединений А. М. Бутлерова. ...Первоначальные сведения о строении органических веществ. Основные положения теории строения органических соединений А. М. Бутлерова
Дата_____________ Класс_______________. Тема: Первоначальные сведения о строении органических веществ. Основные положения теории строения органических ...Теория строения органических соединений
тест Теория строения органических соединений. 1. Верны ли следующие суждения о понятиях «химическое строение» и «изомерия»? А. Химическое ...Органическая химия. Теория химического строения А.М. Бутлерова
План учебного занятия № 18. Дата Предмет. химия. группа. Ф.И.О. преподавателя:. Кайырбекова И.А. . І. Тема занятия:. . Органическая химия. Теория ...Обобщение знаний по классам неорганических соединений
Тема урока. . Обобщение знаний по классам неорганических соединений. ( урок для учащихся 8 классов по неорганической химии, изучаемый в разделе « ...Важнейшие классы неорганических соединений
МОУ Кинель – Черкасская средняя общеобразовательная школа № 1. «Образовательный центр». Конспект. . открытого урока по химии в 8 ...Важнейшие классы неорганических соединений
ГБОУ СОШ пос. Сургут муниципального района Сергиевский Самарской области . . ПЛАН-КОНСПЕКТ УРОКА. . по химии в 8 классе Важнейшие ...Свойства основных классов неорганических соединений
. ПЛАН УРОКА « Свойства основных классов неорганических соединений». Учитель Ефименко З.А. Класс, профиль: 11 класс, базовый уровень. . Программно-методическое ...Обобщение свойств основных классов неорганических соединений в свете теории электролитической диссоциации
Конспект урока химии. . 9 класс. Тема : «Обобщение свойств основных классов неорганических соединений в свете теории электролитической диссоциации». ...Систематика органических соединений
предельные. . непредельные. . Алканы. . . Циклоалканы. . . Алкены. . этиленовые. . Диеновые. . . Алкины. . ацетиленовые. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Пивкина Лариса Анатольевна
Содержит:18 слайд(ов)
Поделись с друзьями:
Скачать презентацию