Презентация "Сера" (9 класс) по химии – проект, доклад
Презентацию на тему "Сера" (9 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 22 слайд(ов).
Слайды презентации
Список похожих презентаций
Сера и её соединения
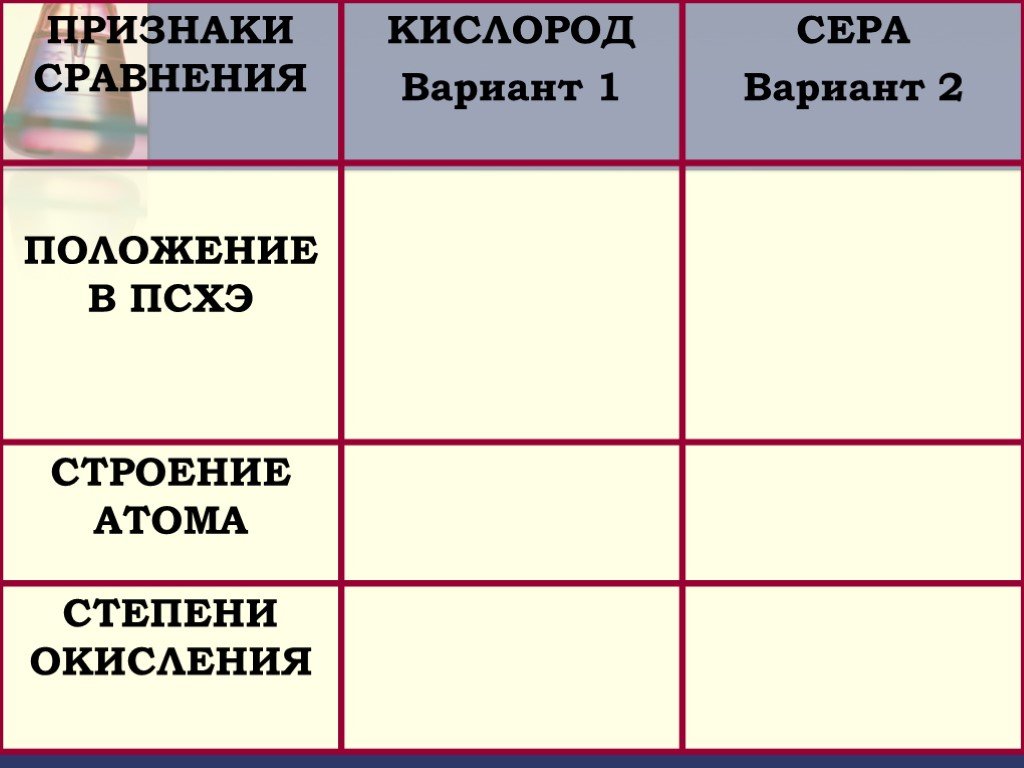
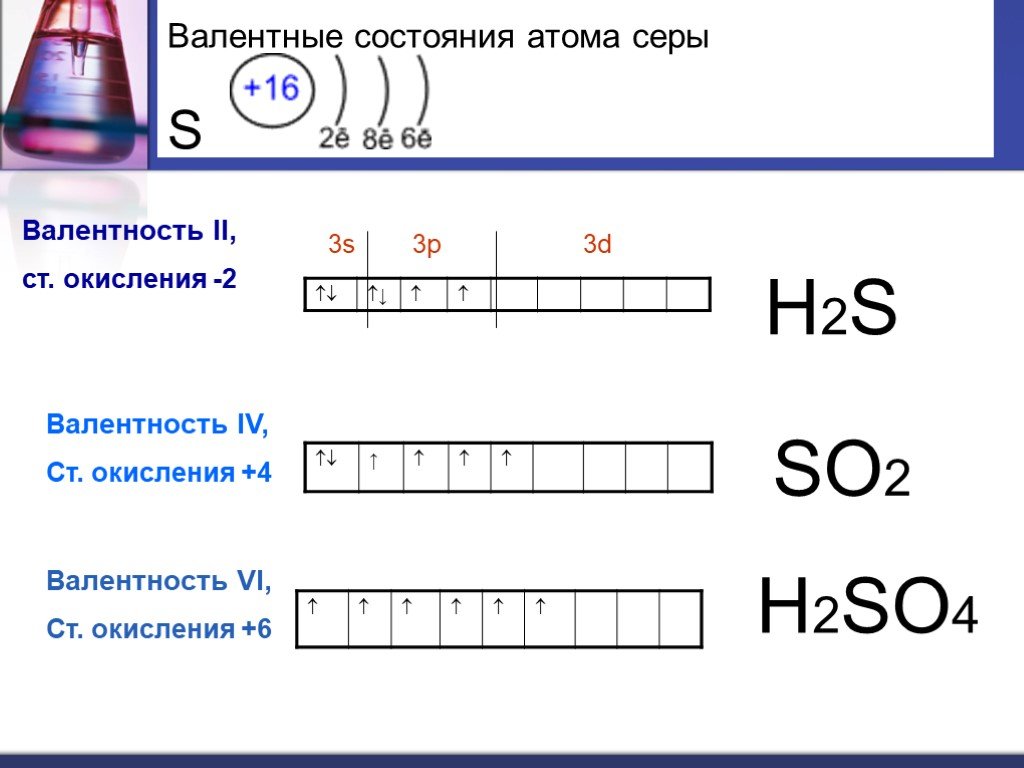
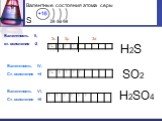
Валентные состояния атома серы S. Валентность II, ст. окисления -2. 3s 3p 3d. Валентность IV, Ст. окисления +4. Валентность VI, Ст. окисления +6. ...Сера и ее соединения
Сера и ее соединения. Цель работы: Изучение физических и химических свойства серы и ее соединений. Выявление отрицательного воздействия на окружающую ...Сера 2
Натрий — химический элемент с атомным номером 11 в периодической системе, обозначается символом Na (лат. Natrium), мягкий щелочной металл серебристо-белого ...Сера и ее свойства
Химический мой знак – S, А 32 есть атомный мой вес. Я кристаллическое вещество, Горю я очень хорошо. Вхожу в состав серной кислоты, Известны соли ...Сера
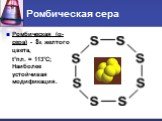
Се́ра — элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), третьего периода периодической системы химических элементов ...Сера
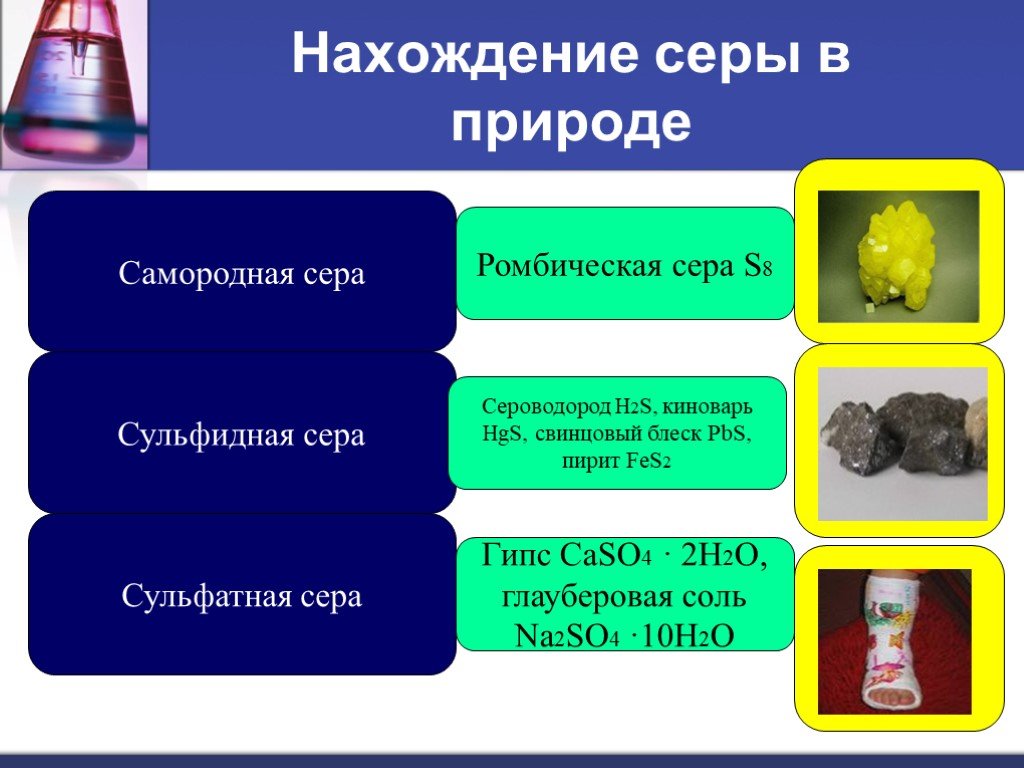
Цель урока. Дать характеристику серы на атомарном, молекулярном и макроуровне. План урока. Сера в природе Атомы серы Аллотропия серы Физические свойства ...Сера
История открытия. С запахом горящей серы, удушающим действием сернистого газа и отвратительным запахом сероводорода человек познакомился ещё в доисторические ...Сера как химический элемент и простое вещество
Основные вопросы. 1.Истрия открытия и изучения серы. 2. Распространение серы в природе. 3. Аллотропия и физические свойства серы. 4.Химические свойства ...Сера как элемент и как простое вещество
Работу выполнили: Учителя химии ГБОУ СОШ № 1465 им. Н.Г.Кузнецова Попова Светлана Анатольевна и Образовательного комплекса ГБОУ СОШ № 880 Гершановская ..."Сера"
Решаем загадки «Неметалы». Красив в кристаллах и парах, на детей наводит страх. Белый, воздуха боится, покраснел чтоб сохраниться. Хоть многие вещества ...Сера
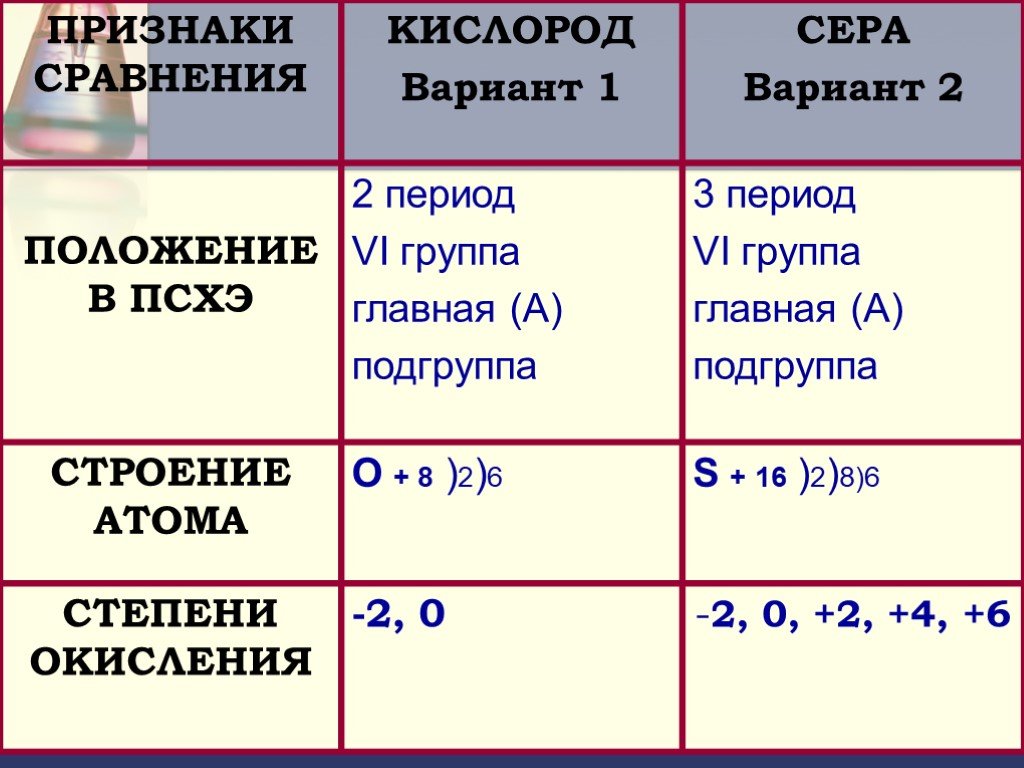
Положение в Периодической системе:. Сера: Порядковый номер № 16 Период : 3 период Группа: VI группа, главная подгруппа. S +16 2 6 8 1s2 2s2 2p6. Краткая ...Сера. Ее физические и химические свойства
«В древней магии присутствую при рождении огня, называют серой издавна меня". 1вариант –О2 2вариант-О3. Газ без запаха Проявляет окислительные и восстановительные ...Сера химия
Сера принадлежит к числу веществ, известных человечеству испокон веков. Ещё древние греки и римляне нашли ей разнообразное практическое применение. ...Интерактивная игра "Химия в ребусах: Химические элементы"
НИКЕЛЬ. ИОД. АЗОТ. БОР. МАГНИЙ Й. МАРГАНЕЦ. КРЕМНИЙ Л=й. МЫШЬЯК. УГЛЕРОД О. ЦИРКОНИЙ. АРГОН. МЕДЬ ДВЕ. КРИПТОН. ЗОЛОТО. СЕРА П=А. ВОДОРОД А=О Т=Д. ...«Электролитическая диссоциация» химия
Электролитическая диссоциация. H2O. Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электролитической диссоциацией. ...«Окислительно-восстановительные реакции» химия
СОДЕРЖАНИЕ:. 1. Какие реакции называются окислительно-восстановительными? 2. Что называют окислителем, восстановителем? 3. Окислительно-восстановительный ...«Нуклеиновые кислоты» химия
Цель урока: сформировать у студентов понимание взаимосвязанности и взаимозависимости веществ в клетке. Задачи урока: повторить строение и основные ...«Задачи» химия
- исследование задач по нанонауке; - ознакомление с наномиром: о достижениях нанохимии и нанотехнологии; - составление задач по нанонауке; - решение ...«Жиры» химия
жиры. Оглавление. Определение и общая формула Физические свойства Химические свойства Классификация жиров Животные жиры Растительные жиры Роль жиров ..."Химические элементы и вещества"
Цель урока:. Повторить основные вопросы по изученному разделу “Вещества и химические явления”, закрепить полученные знания. Физические свойства веществ. ...Конспекты
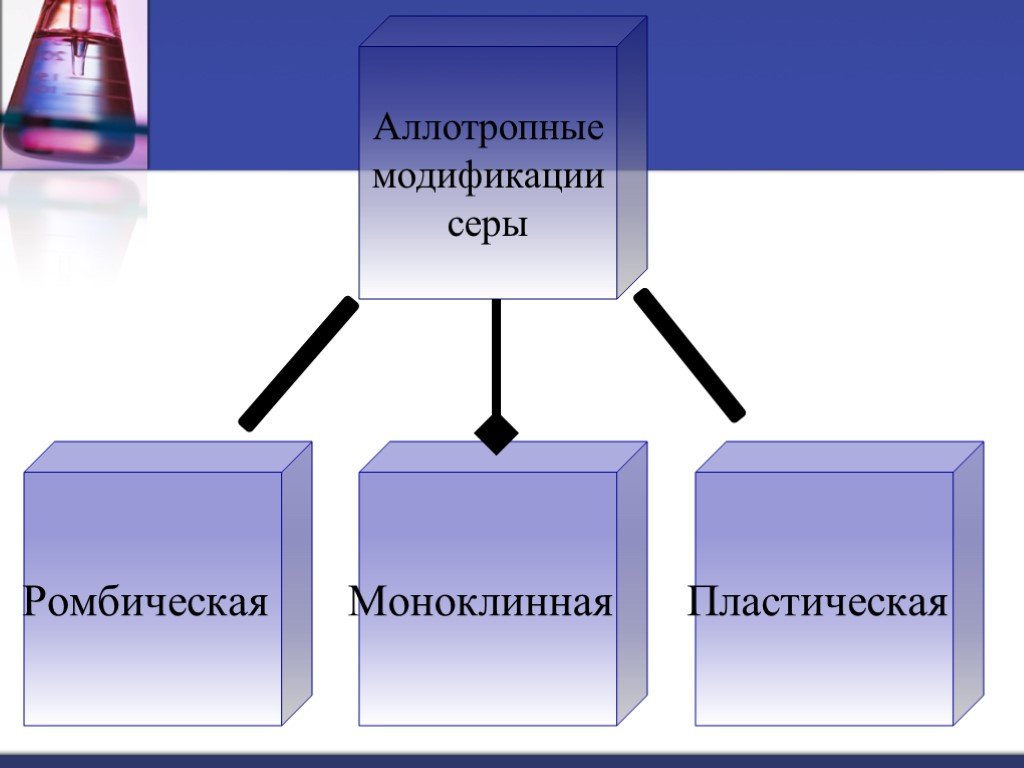
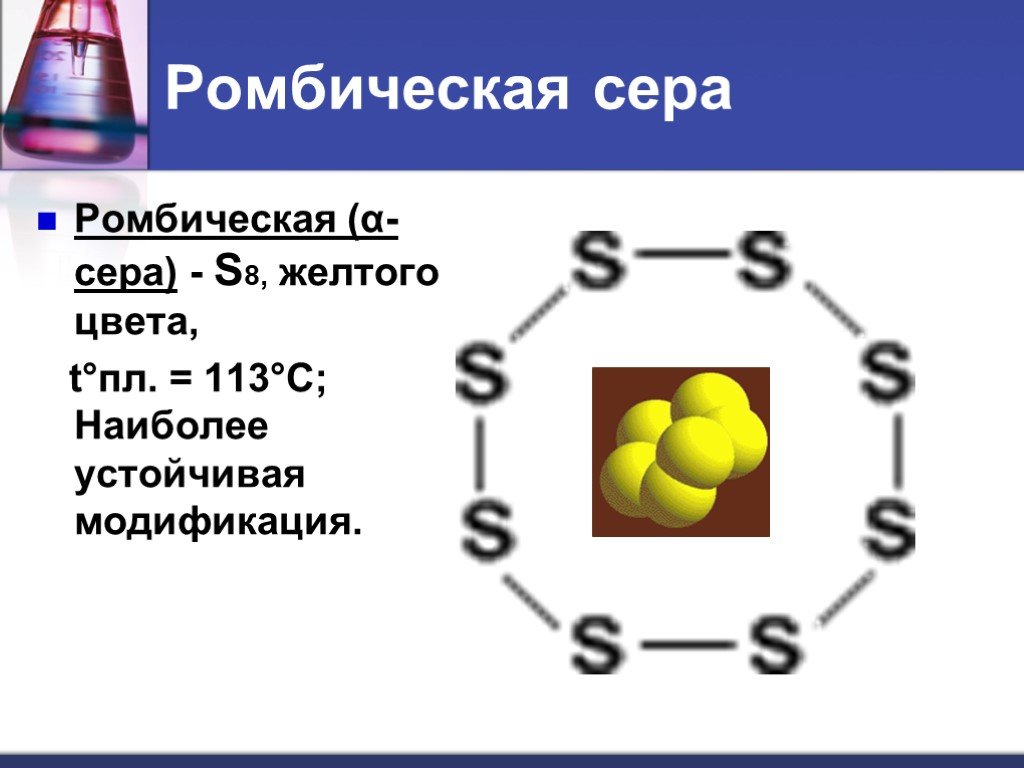
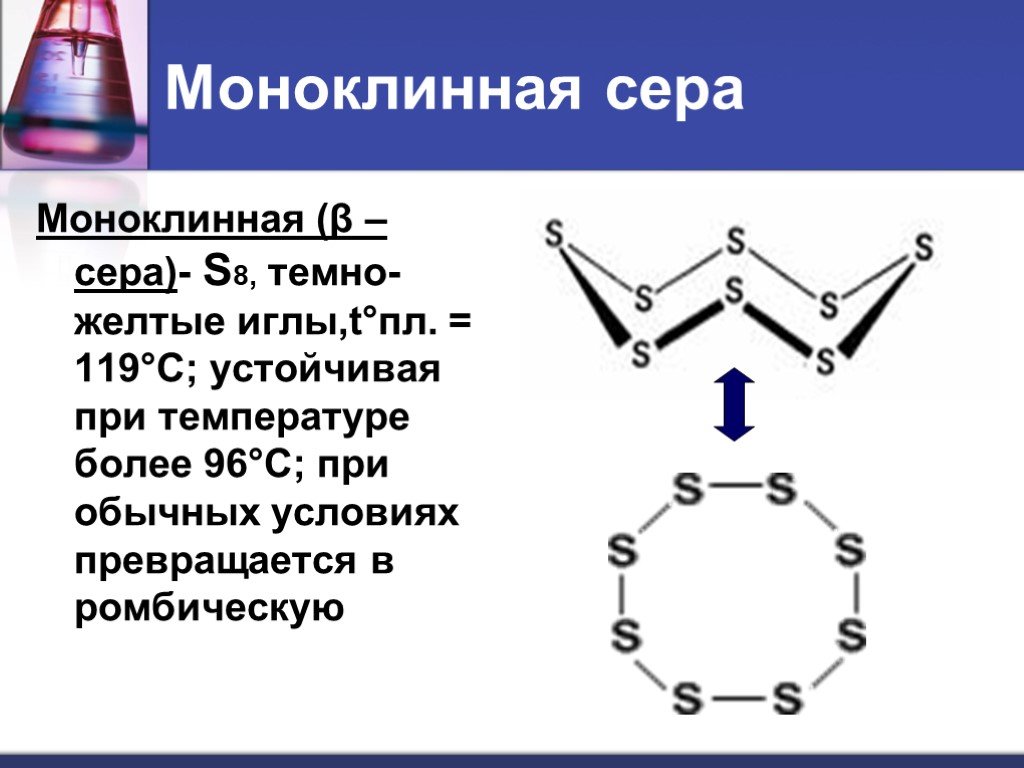
Сера и ее соединения. Аллотропия серы. Сероводород. Оксиды серы
Тема: Сера и ее соединения. Аллотропия серы. Сероводород. Оксиды серы (. IV, VI. ). . Цели урока:. рассмотреть вещество «сера», аллотропию серы, ...Сера, её физические и химические свойства
Конспект урока химии на тему «Сера, её физические и химические свойства» 9 клас. Цели урока:. 1. дать общую характеристику серы, рассмотреть аллотропные ...Сера – простое вещество
Тема «Сера – простое вещество». Цель урока. : определить положение серы в периодической системе химических элементов Д.И. Менделеева, рассмотреть ...Сера и её соединения
Конспект урока с использованием ЭОР. Тема:. Сера и её соединения. Класс: 9. Цель:. изучить строение, свойства серы и его соединений. Задачи:. ...Сера
Тема: Сера. Цель. : Изучить химические свойства серы в свете представлений об окислительно-восстановительных процессах и теории строения атома. ...Сера
МОУ 155 г.Самара Н.А. Ситникова. План - конспект урока химии в 9 классе. Тема: Сера. Цель:. формирование системы знаний о сере как о простом ...Сера
Подготовила студентка Суркова Екатерина. Алгоэвристическая программа для самостоятельного изучения. . учащимися темы «Сера». Сегодня тебе представляется ...Кислород. Сера
Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». Конспект урока по химии в 9 классе. тема урока " Кислород. ...Кислород. Сера
9 класс, обобщение материала по теме «Кислород. Сера». . Заполните пропуски в конспекте урока. КОНСПЕКТ. Кислород и сера: нахождение в ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:25 августа 2018
Категория:Химия
Классы:
Содержит:22 слайд(ов)
Поделись с друзьями:
Скачать презентацию