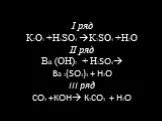"Гидролиз неорганических солей презентация, проект, доклад
Презентацию на тему ""Гидролиз неорганических солей" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 14 слайд(ов).
Слайды презентации
Список похожих презентаций
Гидролиз неорганических солей
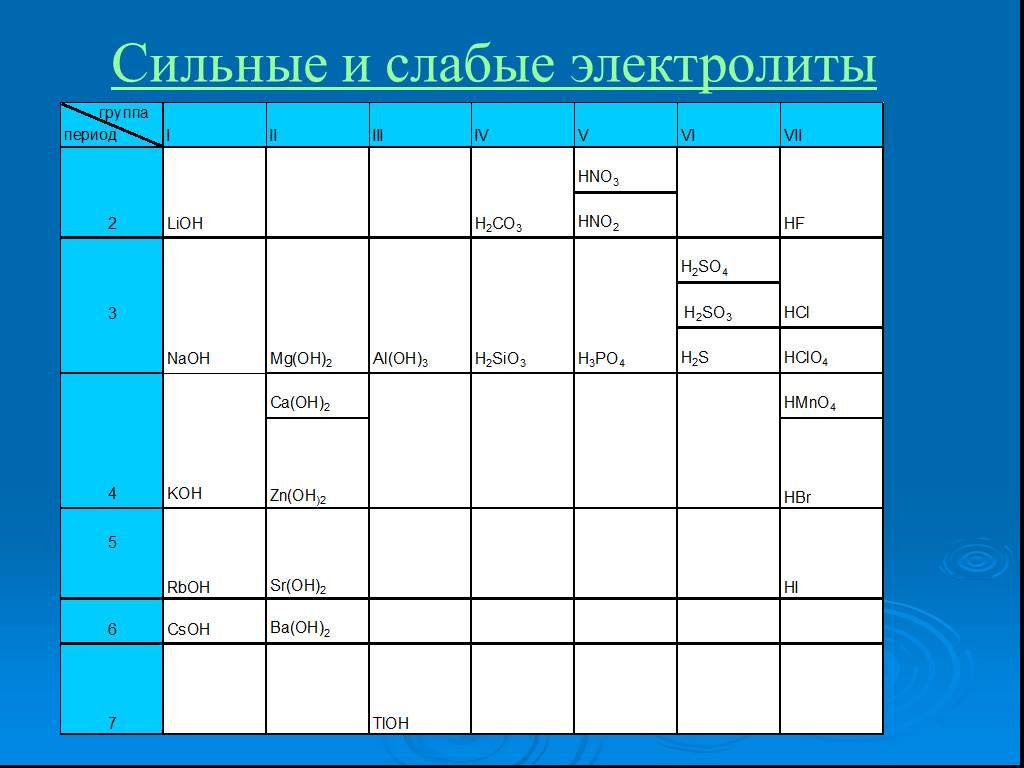
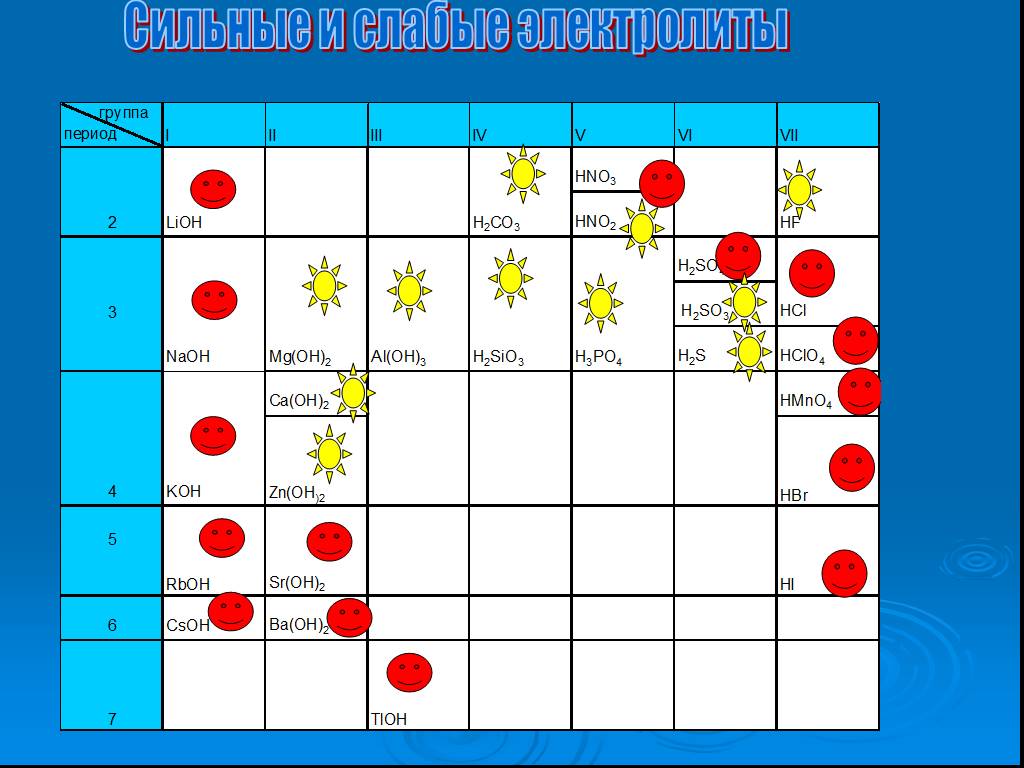
Словарь. Гидролиз – реакция обмена между растворимыми солями и водой Сильные кислоты – кислоты, являющиеся сильными электролитами (H2SO4, HCl, HNO3, ..."Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Содержание химии очень обширно и часто предстает копилкой огромного числа формул, уравнений, фактов и законов, запомнить которые не просто трудно, ...Гидролиз солей
СОДЕРЖАНИЕ Определение. Типы солей,участвующих в гидролизе. Алгоритм составления уравнений гидролиза. Применение гидролиза. Примеры солей,участвующих ..."Гидролиз органических и неорганических соединени"
Цель урока:. повторить гидролиз солей, закрепить полученные знания, отработать навыки составления уравнений реакции гидролиза, предсказывать продукты ...Гидролиз солей
Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого изменяется рН среды. В процессе гидролиза соли в водном растворе ...Гидролиз солей
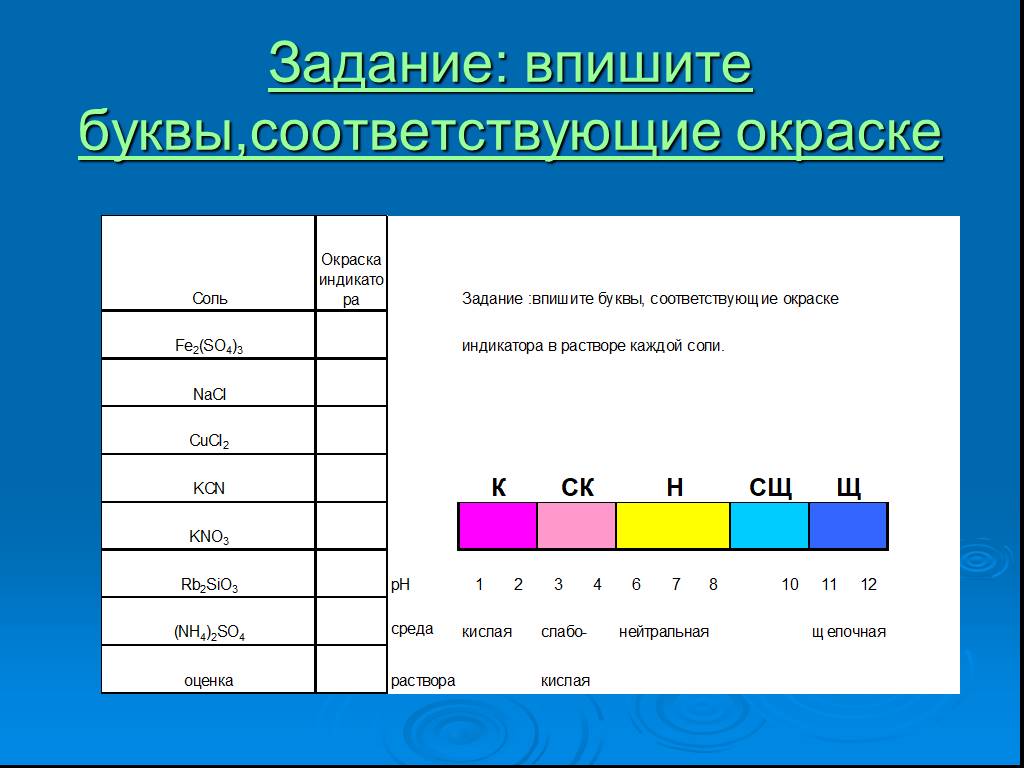
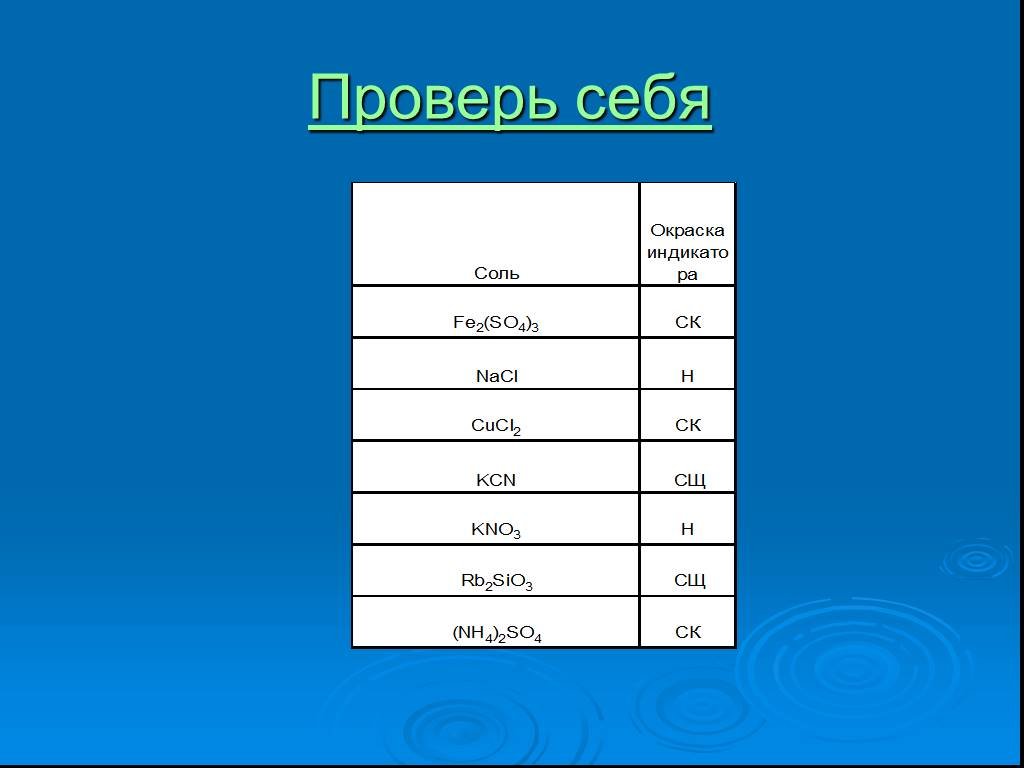
ОКРАСКА ЛАКМУСОВОЙ БУМАГИ В РАЗЛИЧНЫХ СРЕДАХ. Тема: Гидролиз солей. Цель: изучить сущность гидролиза солей в водных растворах. Задачи : сформулировать ...Гидролиз солей
Гидролиз – это реакция обменного разложения веществ водой. Гидролиз органических веществ. 1. Гидролиз галогеналканов. С2Н5Сl + Н2О →С2Н5ОН + НСl 2. ..."Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Химическая среда. Сама вода является очень слабым электролитом. При её электролитической диссоциации образуются катионы водорода и гидроксид-ионы ...Моделювання процесу кристалоутворення солей з розчинів
Об’єкт дослідження – алюмокалієві галуни – подвійні солі калій та алюміній сульфатів. Предметом дослідження є лабораторне моделювання процесу природного ...Определение солей аммония
УРОК-ПРЕЗЕНТАЦИЯ «соли аммония». Цель урока: Показать учащимся, что все соли аммония получают взаимодействием аммиака и соответствующих кислот , обладают ...Генетическая связь между классами неорганических вещ-в
Генетический ряд меди. Генетический ряд кремния. ЗАПИСАТЬ МОЛЕКУЛЯРНЫЕ УРАВНЕНЯ ПЕРЕХОДОВ. Литература:. 1.О.С.Габриелян Химия 8 , Дрофа 2009 2. О.С.Габриелян ...Виды химической связи в неорганических веществах
Знать. определение понятия химическая связь, виды химической связи, механизмы образования каждого вида связи. Уметь. определять вид связи по формуле ...Применение солей в быту
СОЛИ, О КОТОРЫХ СЕГОДНЯ ПОЙДЕТ РЕЧЬ: Поваренная соль Питьевая или пищевая сода Хлорная известь Поташ Медный купорос Железный купорос Марганцовка Гидросульфит ...Химические раскопки по классам неорганических соединений
Раскопки по холмам. Холм Знаний Холм Умений Холм Творчества Холм Памяти. Цель урока:. 1) повторить и систематизировать имеющиеся у вас знания об основных ...Гидролиз
ТЕМЫ:. Гидролиз солей Электролиз водных растворов солей Задачи. Гидролиз солей. Задание А25: кислую среду имеет водный раствор хлорида цинка; 2) нитрата ...Основные классы неорганических соединений. Генетическая связь между классами неорганических соединений
Девиз урока! Все знать, изведать, испытать! Путешествие на подводной лодке «Генезис". соляндия. основайские острова. кислотостан оксидония. Работа ...Гидролиз
Гидролиз галогеноводородов: t, OH R-Cl + H2O ↔ R-OH + HCl Гидролиз сложных эфиров: ∕∕ H , t ∕∕ R1-C + H2O ↔ R2-OH + R1- C O-R2 OH. О. Гидролиз углеводов:. ...Гидролиз
Гидролиз – это реакции обменного Взаимодействия вещества с водой, приводящие к их разложению. Гидролизу подвергаются соединения различных классов: ...Генетические связи между важнейшими классами неорганических соединений
Тема. Генетические связи между важнейшими классами неорганических соединений. А. С. Макаренко: «Теория и практика неотъемлемы». . SO2 HCl H3PO4 H2O ...Генетическая связь между классами неорганических веществ
А13-6-2009. В схеме превращений веществом «X2» является 1) Fe2O3 2) FeO 3) FeCl3 4) FeCl2. А13-2-2009. В схеме превращений веществами «X1» и «X2» ...Конспекты
Гидролиз неорганических веществ – солей
МБОУ « ООШ ст.Миннибаево» Альметьевского района Республики Татарстан. Методическая разработка урока химии. . по теме « Гидролиз неорганических ...Гидролиз солей
Дата _____________ Класс ____________________. Тема: Гидролиз солей. Цели урока:. сформировать у учащихся понятие гидролиза солей. Ход урока. ...Исследование гидролиза солей
Тема занятия:. . Исследование гидролиза солей. Цели занятия:. Провести исследования растворов некоторых солей и доказать, что большинство из них ...Гидролиз солей
Урок по теме: "Гидролиз солей". . . Цель урока. : Сформировать у учащихсе понятия гидролиза солей. Задачи урока:. . Развить у учащихся ...Гидролиз солей
11 класс. Тема:. «Гидролиз солей». Материал данной темы является объемным и сложным. Для лучшего понимания и усвоения этого материала необходимо, ...Гидролиз солей
Муниципальное казённое общеобразовательное учреждение. «Кобыльская средняя общеобразовательная школа». Глушковского района Курской области. ...Гидролиз солей
ПЛАН-КОНСПЕКТ. . проблемного урока по химии для учащихся 9 класса. Тема урока:. «Гидролиз солей». Тип урока:. урок изучения нового материала. ...Гидролиз солей
Муниципальное бюджетное общеобразовательное учреждение. «Средняя общеобразовательная школа №18 имени братьев Могилевцевых». . г. Брянска. ...Гидролиз солей
Тема урока:. . Гидролиз солей. Цели урока:. Сформировать представление о гидролизе, сущности гидролиза солей. . Научить ребят составлять уравнения ...Гидролиз неорганических соединений
ТЕМА УРОКА: Гидролиз неорганических соединений. Тип урока:. Изучение нового материала, обобщение и систематизация знаний. Вид урока:. Проблемно- ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:16 марта 2019
Категория:Химия
Содержит:14 слайд(ов)
Поделись с друзьями:
Скачать презентацию