Конспект урока «Гидролиз солей» по химии
Урок по теме: "Гидролиз солей".
Цель урока: Сформировать у учащихсе понятия гидролиза солей.
Задачи урока:
-
Развить у учащихся умение пользоваться знаниями, закрепить умения и навыки химического эксперимента.
-
Развивать мышление, уметь делать логические выводы из наблюдений по опыту.
-
Научить составлять ионные уравнения реакций гидролиза солей по первой стадии.
-
Сформировать понимание практического значения гидролиза в природе и жизни человека.
Оборудование:
-
реактивы: хлорид натрия, карбонат натрия, хлорид меди, гидроксид натрия, соляная кислота,
-
индикаторы - лакмус, фенолфталеин, пробирки
План урока:
1. Повторение знаний.
Постановка проблемы – стихотворение.
Электролиты и неэлектролиты.
Сильные слабые электролиты.
Работа индикаторов в различных средах.
Эксперимент и выводы опытов.
Доказательство через уравнения реакций.
Определение понятия гидролиза солей.
Значение гидролиза.
Домашнее задание.
Ход урока:
Лежа дома на диване
Про прогулку думал Ваня
Сколько в мире,- думал Ваня,-
Есть кислот и оснований
Например, вода морей-
Это ведь раствор солей.
Где-то я читал когда-то:
Там хлориды и сульфаты…
И соляной там и серной
Кислоты полно наверно:
Ведь вчера прошли мы в школе
Что в воде идет гидролиз!
И зачем себе на горе
Люди в отпуск едут к морю?
Если долго там купаться
Можно без трусов остаться:
Ткань любую кислота
Растворяет кислота
Ванин слушая рассказ,
Целый час смеялся класс
Больше Ваню не дразните,
Ведь сказал ему учитель:
"Зря Иван поддался страху,-
Лучше б шел купаться в море!"
Сейчас мы рассмотрим, что такое гидролиз, и в конце урока скажем, почему Ваня боялся зайти в море.
Фронтальный опрос в виде беседы:
Какие вещества называются электролитами и неэлектролитами?
Что такое кислоты и основания соли с позиции теории электролитической диссоциации?
Какие соли вы знаете? Учащиеся повторяют соли по таблице растворимости, их названия.
Окраска индикаторов в различных средах.
Какие кислоты и основания считаются сильными и слабыми? Степень электролитической диссоциации.
Учащиеся составляют таблицу:
| Слабые Кислоты | Сильные Основания | Слабые основания | |
| HCI H2SO4 HNO3 HJO3 HI HCIO3 | H2CO3 H>2S HCN HClO H3PO3 H2SlO3 H2SO3 | NaOH KOH Ca(OH)2 Ba(OH)2 LlOH | NH4OH и все трудно растворимые основания. |
Гидролиз – это взаимодействие ионов солей с водой, приводящие к появлению кислой или щелочной среды, но не сопровождающиеся образованием осадка или газа.
Процесс гидролиза состоит из двух этапов:
1. Диссоциация соли в растворе – необратимая реакция
2. Собственно гидролиз соли – обратимая реакция.
Условия для гидролиза:
А) Наличие воды.
Б) Реакция идет только по первой стадии.
В) Реакция обратима.
Выделяют три типа гидролиза:
1. Соль образованная сильным основанием и сильной кислотой.
Приведите примеры таких солей?
NaCl – соль образованная сильным основанием NaOH, и сильной кислотой – HCl.
Проводится опыт: К раствору соли добавляется индикатор – лакмус. Окрашивание фиолетовое. Учащиеся делают вывод, что реакция среды нейтральная и записывают вывод, что соль образованная сильным основанием и сильной кислотой гидролизу не подвергается и имеет нейтральную реакцию среды.
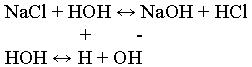
Практическое применение поваренной соли.
2. Соль, образованная сильным основанием и слабой кислотой. Гидролиз по аниону.
Приводятся примеры солей.
Na2CO3 - соль образованная сильным основанием NaOH, и слабой кислотой H2CO>3.
Проводится опыт: Берутся две пробирки, в которые наливают растворы гидроксида натрия, и карбоната натрия добавляем в обе пробирки фенолфталеин.
Учащиеся наблюдают малиновое окрашивание и делают вывод, что реакция среды щелочная и интенсивность окрашивания в обоих пробирках одинакова.
Записывается уравнение реакции.
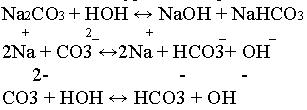
Поэтому сода находит большое применение в быту.
Избыток гидроксид-ионов дает соли щелочную реакцию среды, поэтому лакмус синий, а фенолфталеин становится малиновым.
3. Соль, образованная слабым основанием и сильной кислотой, гидролиз по катиону.
Приводятся примеры таких солей.
CuCl2 - соль образованная сильной кислотой HCI и слабым основанием Cu(OH)2
Проводится опыт: Берутся две пробирки в которые наливаются растворы кислоты и хлорида меди. В обе пробирки приливаем индикатор – лакмус, и наблюдаем красное окрашивание. Интенсивность окрашивания приблизительно одинакова.
Записываем уравнение реакции.
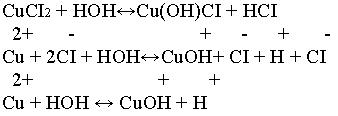
Избыток ионов водорода дает соли кислую реакцию, поэтому лакмус краснеет.
Вывод : Гидролиз – это взаимодействие солей с водой, в зависимости от типа соли индикаторы окрашиваются в различные цвета.
В конце урока мы возвращаемся к стихотворению и отвечаем, почему же Ваня боялся зайти в море.
Значение гидролиза: Учитель рассказывает о большом практическом значении гидролиза для человека, касаясь органических веществ: жиров, спиртов, мыла, крахмала, которые подробно изучаются в 10 классе.
Домашнее задание. Параграф в учебнике и записи в тетради.
Здесь представлен конспект к уроку на тему «Гидролиз солей», который Вы можете бесплатно скачать на нашем сайте. Предмет конспекта: Химия Также здесь Вы можете найти дополнительные учебные материалы и презентации по данной теме, используя которые, Вы сможете еще больше заинтересовать аудиторию и преподнести еще больше полезной информации.

