Конспект урока «Кислоты» по химии
Развёрнутый план-конспект урока по теме: «Кислоты».
8 класс
Тип урока: комбинированный, с использованием презентации «Кислоты».
Образовательные задачи: познакомить уч-ся с составом, определением кислот, их классификацией, способами получения, химическими свойствами; с правилами техники безопасности при работе с кислотами. Научить составлять и называть химические формулы кислот; пользоваться рядом активности металлов. Проверить знания уч-ся по теме «Основания»: классификация, получение, химические свойства.
Развивающие задачи: продолжить: формирование умения наблюдать, объяснять, делать выводы; совершенствовать умения объяснять (химические свойства кислот).
Воспитательные задачи: продолжить формирование интереса к предмету; развитие элементов эстетического воспитания (аккуратное оформление конспекта), патриотического (Бекетов Н.Н).
Методы обучения:
Словесные: объяснение (кислоты, их классификация, получение и химические свойства), элементы беседы.
Словесно – наглядные: объяснение с использованием презентации, записей на доске.
Словесно – наглядно – практические: выполнение уч-ся лабораторной работы, выполнение заданий на закрепление изученного материала.
Ход урока.
-
Организационный момент (≈2-3 мин.).
Учитель приветствует учащихся, создаёт рабочий настрой на урок. Сообщает, что вначале урока проверочная работа по теме «Основания».
-
Контроль знаний и умений (≈ 10 мин.).
1 вариант.
1. Напишите уравнения реакций получения следующих оснований: Al(OH)3, NaOH.
2. С какими из перечисленных веществ будет реагировать раствор гидроксида калия: HCl, Ba(OH)2, FeSO4. Напишите соответствующие уравнения реакций в молекулярном, ионном и сокращённом ионном виде.
2 вариант.
1. Напишите уравнения реакций получения следующих оснований: Zn(OH)2, KOH.
2. С какими из перечисленных веществ будет реагировать раствор гидроксида бария: H2SO4, KOH, FeCl2. Напишите соответствующие уравнения реакций в молекулярном, ионном и сокращённом ионном виде.
После проверочной работы учитель сообщает тему урока «Кислоты» и его цель – сформировать знания о кислотах, их составе, классификации и химических свойствах. Также учитель информирует о плане предстоящей деятельности на уроке – в начале изучение нового материала (с выполнением лабораторных опытов), а затем его закрепление.
-
Объяснение нового материала (≈25 мин.).
План изучения нового материала:
-
Состав кислот.
-
Классификация кислот.
-
Получение кислот.
-
Физические и химические свойства.
1.Состав кислот.
При изучении способов получения водорода в лаборатории вы уже ознакомились с реакциями цинка с соляной и серной кислотами. Сходно реагируют с кислотами и другие металлы, например:
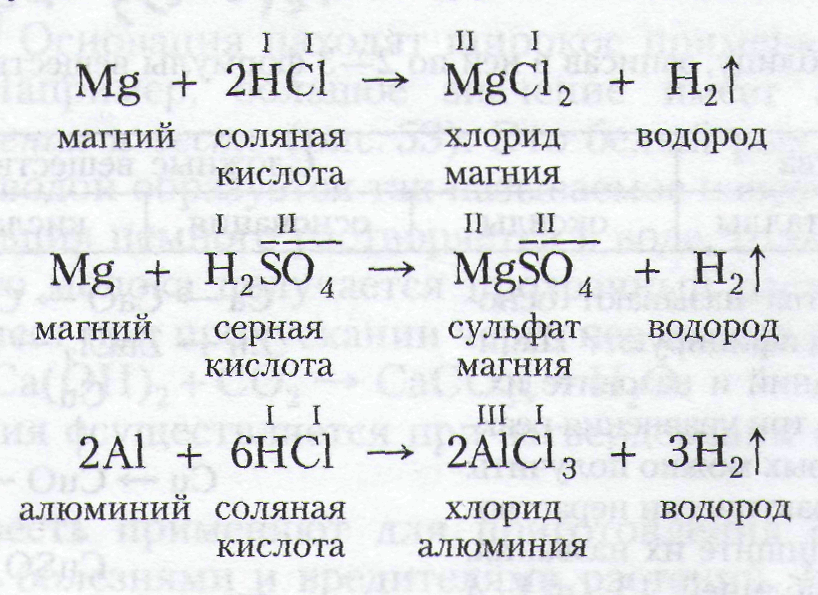
Учитель записывает уравнения реакции на доске (словесно-наглядный метод обучения). Рассматривая уравнения этих реакций, можно сделать следующий вывод о составе кислот:
Кислотами называют сложные вещества, состоящие из кислотных остатков и водорода, который может замещаться на атомы металлов (уч-ся записывают определение в тетрадь).
Из рассмотренных выше уравнений видно, что:
-
кислотные остатки в химических реакциях обычно сохраняются и
переходят из одних соединений в другие; -
валентность кислотных остатков определяется числом атомов водорода, способных замещаться атомами металлов (учитель обращает внимание уч-ся на табл. 12 в учебнике).

2. Классификация кислот.
По составу кислоты делятся на кислородсодержащие и бескислородные, а по числу содержащихся в них атомов водорода, способных замещаться на металл, — на одноосновные, двухосновные и трехосновные (схема 15).
(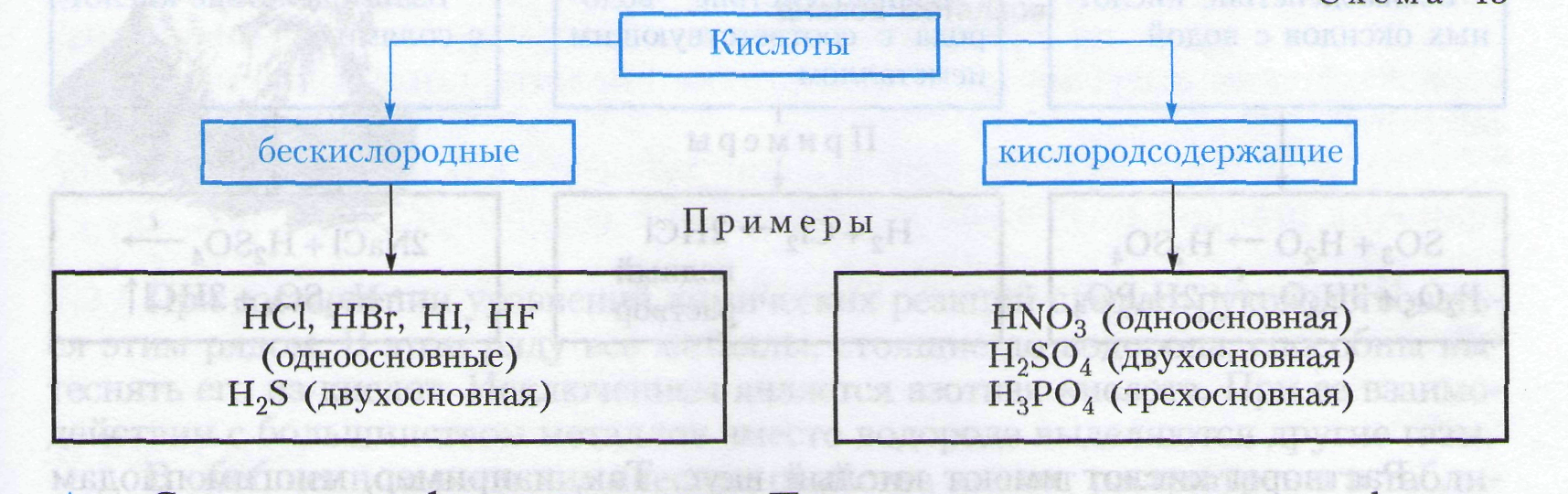 уч-ся записывают схему в тетрадь).
уч-ся записывают схему в тетрадь).
-
П
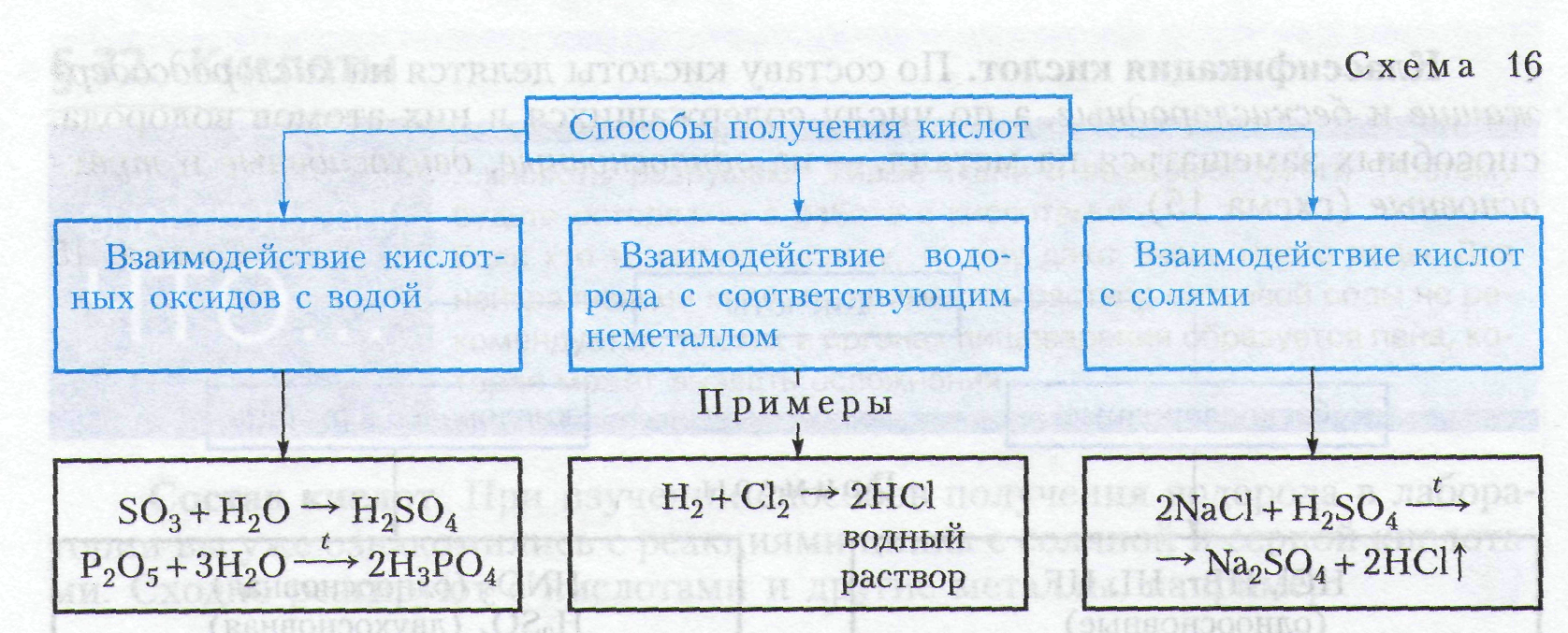 олучение кислот.
олучение кислот.
Учитель записывает схему на доске, уч-ся в тетради (словесно- наглядный метод обучения).
-
Физические и химические свойства.
Физические свойства. Многие кислоты, например серная, азотная, соляная, — это бесцветные жидкости. Известны также твердые кислоты: ортофосфорная Н3РО4, метафосфорная НРО3, борная Н3ВО3. Почти все кислоты растворимы в воде. Пример нерастворимой кислоты — кремниевая Н2SiO3.
Растворы кислот имеют кислый вкус. Так, например, многим плодам придают кислый вкус содержащиеся в них кислоты. Отсюда названия кислот: яблочная, лимонная и т. д.
Химические свойства. Рассмотрим наиболее характерные общие свойства водных растворов кислот. Учитель начинает объяснение.
1. Действие кислот на растворы индикаторов.
Вы уже знаете, что вещества, которые под действием растворов кислот и щелочей изменяют свой цвет. Как их называют? (индикаторами). Какие вам известны индикаторы? (лакмус, метиловый оранжевый, фенолфталеин) [словесный метод обучения]. Растворы кислот окрашивают лакмус в красный цвет, метиловый оранжевый — в розовый, а фенолфталеин остается бесцветным (уч-ся записывают в тетрадь).
2. Характерным свойством кислот является их взаимодействие с металлами. Особенно быстро реагирует с кислотами магний, несколько медленнее — цинк, еще медленнее — железо, а с медью никаких изменений не наблюдается (водород не выделяется).
При выпаривании образовавшихся растворов выделяются кристаллические вещества — соли. Аналогичные опыты были проделаны русским ученым Н. Н. Бекетовым. На основе опытов он составил вытеснительный ряд металлов:
![]()
(уч-ся записывают в тетрадь).
Учитель объясняет: При составлении уравнений химических реакций следует руководствоваться этим рядом. В этом ряду все металлы, стоящие до водорода, способны вытеснять его из кислот. Исключением является азотная кислота (уч-ся записывают). При ее взаимодействии с большинством металлов вместо водорода выделяются другие газы.
Рассмотрим химические свойства кислот (учитель записывает на доске, уч-ся в тетради).
Вещества, с которыми реагируют кислоты:
1.С индикаторами.
2.С металлами. Если металл находится в ряду, составленным Бекетовым, до водорода, то вытесняется водород и образуется соль. Искл. НNO3.
Уч-ся поводят опыт. Перед опытом обсуждение ТБ:
1.Внимание! Работать с кислотами необходимо аккуратно. При попадании кислоты на кожу надо смыть ее большим количеством воды.
2. Соблюдайте правила работы со спиртовкой.
Оборудование и реактивы: пробирочный зажим, спиртовка, спички; соляная кислота, цинк, оксид меди (II), серная кислота
Опыт 1. Взаимодействие цинка с соляной кислотой.
Налейте в пробирку 1мл соляной кислоты. Добавьте 1 гранулу цинка. Что наблюдаете? Запишите уравнение реакции.
Zn+2HCl=ZnCl2+H2↑
3.С оксидами Ме (основными, амфотерными). Образуется соль и вода.
Уч-ся поводят опыт.
Опыт 2. Взаимодействие оксида меди (II) с серной кислотой.
В пробирку насыпьте немного оксида меди (II), прилейте 1 мл серной кислоты H2SO4. Пробирку слегка нагрейте. Что наблюдаете? Запишите уравнение реакции.
CuO+ H2SO4=CuSO4+H2O
4.С основаниями. Образуется соль и вода. Этот опыт уч-ся не проводят, т.к делали его ранее при изучении химических свойств оснований. Учитель напоминает, что реакция взаимодействия соли с кислотой называется реакцией нейтрализации. Уч-ся записывают ур-е реакции:
NaOH+HCl=NaCl+H2O
5.С солями. В соответствии с рядом кислот (каждая предыдущая кислота может вытеснить из соли последующую): H2SO4, HCl, H2SO3, H2CO3, H2S, H2SiO3. Уч-ся записывают ур-е реакции:
ZnCl2+ H2SO4(конц)= ZnSO4+2HCl↑
6.При нагревании некоторые кислоты разлагаются. Как правило, образуется кислотный оксид и вода. Уч-ся записывают ур-е реакции:
H2SO3= H2O+SO2
В п. 3, 4 и 5 приведённые ур-я реакций относятся к реакциям обмена. Необходимо учесть, что реакции обмена протекают до конца в следующих случаях:
1. если в результате реакции образуется вода;
2. если в результате реакции образуется газ;
3. если в результате реакции образуется осадок.
IV. Первичное закрепление нового материала (≈10 мин.)
(уч-ся выполняют задания на местах. Проверяются задания у доски).
1. Составьте уравнения возможных реакций: серная кислота+алюминий; соляная кислота +серебро; бромоводородная кислота+цинк.
2. Составьте уравнения реакций: серной кислоты и Fe(OH)3; соляной кислоты и Ba(OH)2, азотной кислоты и Na2SiO3.
3. Составьте уравнения реакций между веществами: а) иодоводородная кислота и оксид бария; б) серная кислота и оксид железа (III); в) азотная кислота и оксид лития; г) фосфорная кислота и оксид калия.
4. Составьте уравнения реакций нейтрализации: а) гидроксида натрия серной кислотой; б) гидроксида бария азотной кислотой; в) гидроксида кальция соляной кислотой.
V. Домашнее задание (≈1 мин.).
Представлено на слайде §32
VI. Итог урока (≈1 мин.).
Сегодня на уроке вы познакомились с классификацией, способами получения и химическими свойствами кислот.
Здесь представлен конспект к уроку на тему «Кислоты», который Вы можете бесплатно скачать на нашем сайте. Предмет конспекта: Химия Также здесь Вы можете найти дополнительные учебные материалы и презентации по данной теме, используя которые, Вы сможете еще больше заинтересовать аудиторию и преподнести еще больше полезной информации.

