Презентация "Окислительно-восстановительные реакции: общие сведения" по химии – проект, доклад
Презентацию на тему "Окислительно-восстановительные реакции: общие сведения" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 15 слайд(ов).
Слайды презентации
Список похожих презентаций
Общие сведения о чугуне
План:. Состав чугуна. Структура чугуна. Влияние примесей на свойства. Состав чугуна. Чугунами называют железоуглеродистые сплавы содержащие углерода ...Общие сведения о металлах
Особенности электронного строения атомов металлов. Положение металлов в ПСХЭ. Закономерности в изменении свойств элементов – металлов. . Типы кристаллических ...Реакции обмена в водных растворах электролитов. Ионные реакции и уравнения
Ионные реакции – реакции протекающие между ионами в растворе. Порядок составления ионных уравнений реакции. 1. Записывают молекулярное уравнение реакции ...Почему протекают химические реакции
Первый закон термодинамики – закон сохранения энергии. Энергия не возникает из ничего и не исчезает бесследно, а только переходит из одной формы в ...Влияние условий на скорость химической реакции
Заполните схему с вопросами о скорости реакции:. Задачи урока. Природа реагирующих веществ Концентрация реагирующих веществ Площадь реагирующих веществ ...Цветные качественные реакции, как способ химического кодирования документов
Тайнопись и защита информации. Защита информации и документов от подделки актуальна с древности. Наибольшую популярность в прошлом имели химические ...Химические реакции
Типы химических реакций. По числу вступивших в реакцию веществ По тепловому эффекту По обратимости По изменению степени окисления По агрегатному состоянию ...Химические реакции
Разминка. НСl Н2SО4 НNО3 Н3РО4 СаСl2 Н2SiО3 Мg(NO3)2 НI К3РО4 НNO2 Cu(OH)2. Серная кислота Соляная кислота Азотная кислота. Ортофосфорная кислота. ...Скорость химической реакции
Скорость гомогенной и гетерогенной реакций. Изменение концентрации вещества по мере протекания реакции. Диаграмма изменения внутренней энергии веществ ...Неорганические соединения - формулы и реакции
Цели урока. В игровой форме обобщить и закрепить знания о химических свойствах основных классов неорганических соединений и их взаимопревращениях. ...Некоторые Окислительно-восстановительные реакции алкенов
Правила составления ОВР. Взаимодействия алкенов с водным раствором KMnO4 (реакция Вагнера). При взаимодействии алкенов с водным раствором KMnO4 происходит ...Качественные реакции на ионы металлов
Проблемный вопрос: каким образом можно определить ионы металлов в растворах. Цель работы: научиться определять ионы металлов Задачи: расширить знания ...Качественные реакции в органической химии
Алканы. Качественная реакция на алканы: Определить, что какое-то вещество в смеси или в чистом виде алкан, несложно. Для этого газ либо поджигают ...История появления стекла и все сведения о нем
План. 1.Теория происхождения стекла. 2.Реакция получения стекла и его молекулярная формула. 3.Состав стекла 4.Окраска стекол 5.Свойства 6.Виды стекла. ...Изучение реакции среды в зависимости от типа гидролиза соли
Лабораторная работа Изучение реакции среды в зависимости от типа гидролиза соли. Цели: понять сущность гидролиза. научиться определять реакцию и тип ...Скорость реакции
Скорость химической реакции определяется изменением количества реагирующих веществ или продуктов реакции за единицу времени в единице объема (для ...Скорость химической реакции
План лекции. 1. Основные понятия 2. Классификация процессов 3. Скорость химической реакции 4. Влияние концентрации реагента на скорость реакции 5. ...Окислительно - восстановленные реакции
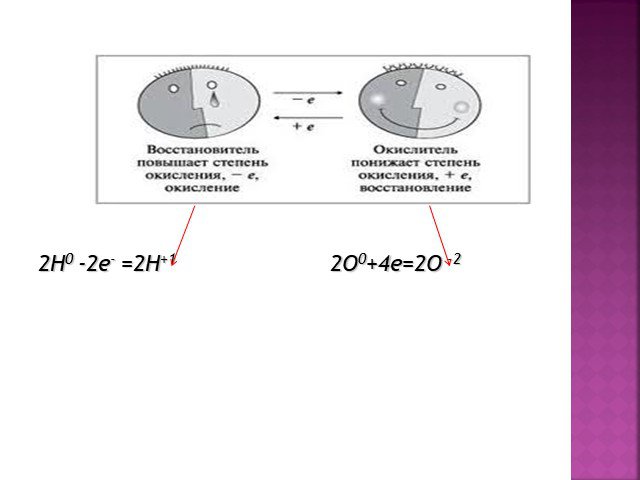
Окислительно-восстановительные реакции (ОВР) – реакции, сопровождающиеся изменением степени окисления элементов (атомов). Степень окисления (СО) – ...Факторы, влияющие на скорость химической реакции
Скорость химических реакций зависит от многих факторов. Основными из них являются: природа и концентрация реагирующих веществ, давление (в реакциях ...Окислительно – восстановительные реакции
Значение окислительно – восстановительных реакций в окружающем нас мире трудно переоценить. ЦЕЛИ:. 1.Расширение, углубление и обобщение знаний в области ...Конспекты
Физические и химические явления. Химические реакции
« Химия». Тема урока: «Физические и химические явления. Химические реакции». Предмет: Химия Класс :8. Занозина Елена Владимировна , учитель химии ...урок Горение простых и сложных веществ. Тепловой эффект реакции
. Горение простых и сложных веществ. . . Тепловой эффект химической реакции.(8 класс). Учитель химии. Вохмякова Татьяна ...Факторы, влияющие на скорость химической реакции
Тема урока: «Факторы, влияющие на скорость химической реакции». I. . Цели:. Показать влияние различных факторов на скорость химических реакций. ...Скорость химической реакции . Факторы, влияющие на скорость химической реакции
Тема урока: «Скорость химической реакции . Факторы, влияющие на скорость химической реакции.». Цели урока. :. -актуализировать и углубить знания ...Степень окисления. Окислительно-восстановительные реакции
Казахстан, Северо-Казахстанская область, район имени Габита Мусрепова, село Сокологоровка. КГУ «Сокологоровская средняя школа». ...Химические реакции
8 класс. Урок по теме «Химические реакции». Цель:. обобщить и систематизировать знания по теме «Химические реакции». Задачи: 1) образовательная:. ...Именные реакции в органической химии
Урок обобщения: "Именные реакции в органической химии" 10 класс. Максимова И.Н. учитель химии и биологии. . МБОУ «Среднекибечская СОШ» Канашского ...Обобщение знаний об основных типах химической реакции
. /8 класс/. Тема урока:. Обобщение знаний об основных типах химических реакций. Цель:. Обобщить и закрепить знания о типах ...Окислительно - восстановительные реакции
Рогова Е.В. Учитель химии и биологии. МКОУ Васильевская ООШ Воронежской области. Тема урока. - лекции: Окислительно - восстановительные ...Кислоты органические и неорганические. Классификация и общие свойства кислот
Конспект открытого урока химии в 11 классе. «Кислоты органические и неорганические. Классификация и общие свойства кислот». Тема урока. Кислоты. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Боротюк Татьяна Сергеевна, учитель химии
Содержит:15 слайд(ов)
Поделись с друзьями:
Скачать презентацию