Презентация "Бензол" по химии – проект, доклад
Презентацию на тему "Бензол" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 13 слайд(ов).
Слайды презентации
Список похожих презентаций
Химия Бензол
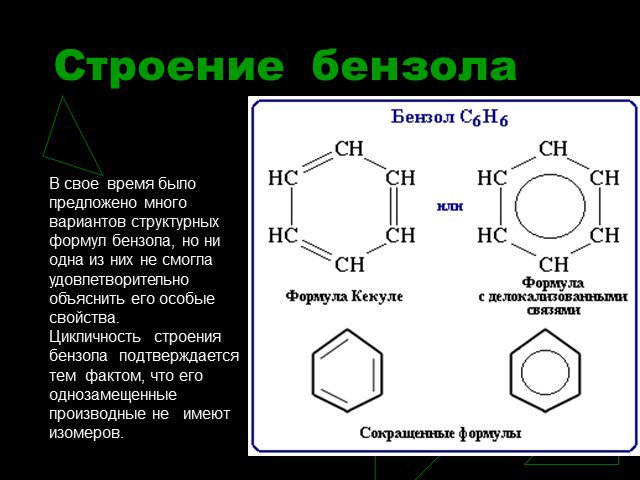
План. 1. Бензол – представитель аренов. 2. Строение аренов. Ароматическая связь. 3. Свойства бензола: а) сходство с алканами б) сходство с алкенами. ...Ароматические углеводороды. Бензол
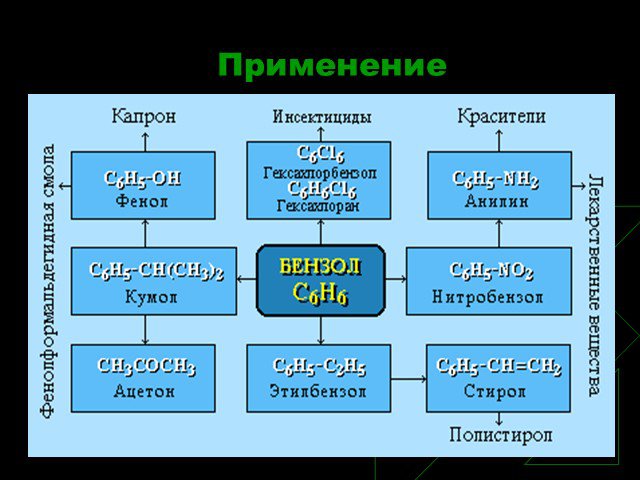
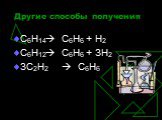
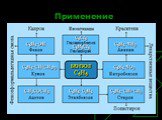
Строение молекулы. УВ. Химические свойства. Изомерия. Физические свойства. Проверка знаний Получение Номенклатура Применение. История открытия бензола. ...Бензол и его свойства
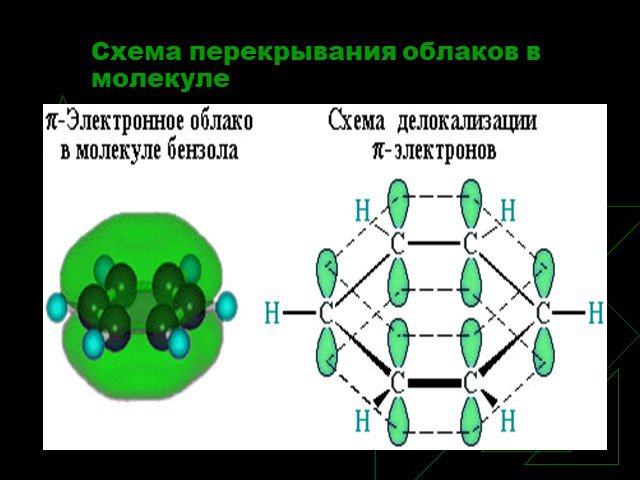
История открытия бензола Второе рождение Новое получение Строение бензола Схема перекрывания облаков в молекуле Физические свойства Химические свойства ...Ароматические углеводороды. Бензол
Ароматические углеводороды Название эти углеводороды получили от первых известных представителей этого класса, имевших приятный запах…. По международной ...Ароматические углеводороды – арены. Бензол как представитель ароматических углеводородов
Бензол как представитель ароматических углеводородов. Задачи урока:. на примере бензола познакомиться с углеводородами, которые имеют замкнутые цепи ...Арены. Бензол
История открытия бензола. Иоганн Глаубер Майкл Фарадей. Эйльгард Митчерлих. Юстус Либих. Структура молекулы бензола. Фридрих Август Кекуле. Формула ...Арены. Бензол
Майкл Фарадей (1791 - 1867). Английский физик и химик, член Лондонского королевского общества. В 1823 г. впервые получил жидкие хлор, сероводород, ...Арены. Ароматические углеводороды. Бензол
Запишите уравнения реакций:. 1 вариант бутанбутен бутадиен 1,3 1,4-дибромбутен-2. Получение этина . 2 вариант 1.Пропенпропинхлор-пропендихлорпропан. ...Конспекты
Бензол как представитель ароматических углеводородов
Методическая разработка. . УРОК : «Бензол как представитель ароматических углеводородов» . . (Модульный урок). Немытькова А.В учитель химии МБОУ ...Арены. Бензол
Урок в 10 классе. Тема: Арены. Бензол. МБОУ РСОШ «10. Учитель: Григоренко Е.В. Цели урока. ...Ароматические углеводороды – арены. Бензол как представитель ароматических углеводородов
ФОРМА УРОКА:. презентация с музыкальным сопровождением. ТИП УРОКА:. изучение нового материала. ТЕМА УРОКА. «Ароматические углеводороды – арены. ...Арены. Бензол
Арены. Бензол. . . Цель: . сформировать представление обучающихся о строении бензола, познакомить с его физическими и химическими свойствами, ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:15 января 2015
Категория:Химия
Содержит:13 слайд(ов)
Поделись с друзьями:
Скачать презентацию