Презентация "Щелочные металлы - элементы I группы главной подгруппы" по химии – проект, доклад
Презентацию на тему "Щелочные металлы - элементы I группы главной подгруппы" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 13 слайд(ов).
Слайды презентации
Список похожих презентаций
Элементы главной подгруппы V группы
Фосфор и здоровье человека. Содержание фосфора в организме человека (масса тела 70 кг) составляет 780 г. Суточная доза для взрослых 1 г. Бирюза(минерал ...Металлы IА-группы щелочные металлы
14.11.2018 Что узнаем…. Положение щелочных металлов в Периодической системе Изменение свойств в группе История названия Нахождение в природе Физические ...Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Строение атома. КИСЛОРОД. Кислород O2 (К.В. Шееле 1772 г., Дж. Пристли 1774 г.) Самый распространенный элемент на Земле; в воздухе - 21% по объему; ...Соединения Ca и Mg, представителей элементов II группы главной подгруппы
План урока. Проверка домашнего задания. 2. Знакомство с соединениями металлов главной подгруппы второй группы. 3. Л/р «Изучение коллекции соединений ...Характеристика элементов VII группы главной подгруппы. Хлор
. . . . Нахождение в природе.В земной коре хлор - самый распространённый галоген. Поскольку хлор очень активен, в природе он встречается только ...
Железо – элемент побочной подгруппы
Общая характеристика железа. Нахождение в природе. Fe ХАЛЬКОПИРИТ ПИРИТ ЧЁРНЫЙ ПИРИТ ГЕМАТИТ. 1s2 2s2 2p6 3s2 3p6. Краткая электронная формула. Валентные ...Железо элемент побочной подгруппы
Цель:. 1. Вводная тема для формирования и развития познавательного интереса к материалу. 2. Осознания учащимися исторического значения освоения железа ...Щелочные металлы
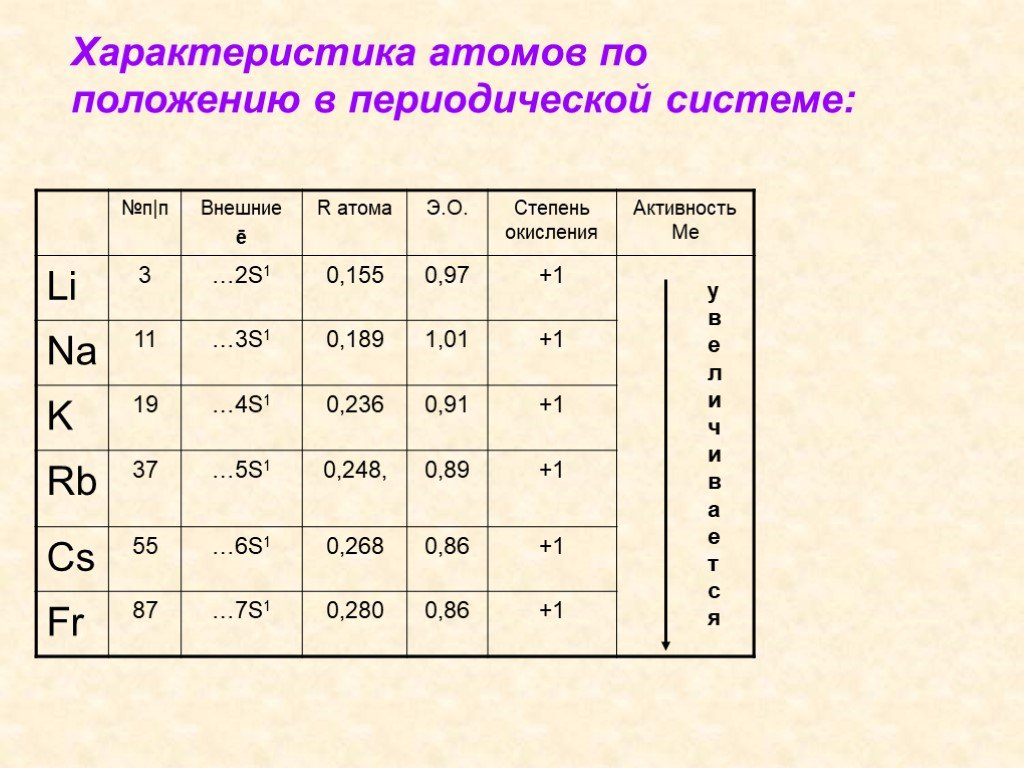
Строение и свойства атомов. Щелочные металлы – это элементы главной подгруппы I группы Периодической системы химических элементов Д.И. Менделеева: ...Общая характеристика подгруппы углерода
Сравнительная характеристика элементов IV группы главной подгруппы. 2s22p2 3s23p2 4s24p2 5s25p2 6s26p2 C Si Ge Sn Pb 73 119 )) ))))) ))) )))))) ))))))) ...Щелочные металлы
Цель: повторить свойства металлов, систематизировать и углубить знания о щелочных металлах на основании их сравнительной характеристики. Сформировать ...Щелочные металлы
Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно».Самый тугоплавкий. Самый распространенный ...
Щелочные металлы
Щелочные металлы. Периодическая система химических элементов Д.И.Менделеева. Группы элементов I III II VIII IV V VI VII 2 1 4 5 6 7 10 F фтор 9 18.9984 ...Щелочные металлы
Цель урока:. Дать общую характеристику щелочным металлам. Рассмотреть их электронное строение, сравнить физические и химические свойства. Узнать о ...Общая характеристика элементов подгруппы кислорода
ПАМЯТКА К ИЗУЧЕНИЮ ПОДГРУППЫ ЭЛЕМЕНТОВ. 1.Пользуясь Периодической системой, выпишите символы и названия химических элементов, относящихся к данной ...Щелочные металлы
В одном царстве-государстве Жили-были, не тужили Галогены удалые И металлы щелочные. Скупых галогенов-окислителей В народе прозвали грабителями. А ...Щелочные металлы
Химические элементы главной подгруппы IА группы периодической системы элементов Д. И. Менделеева: Li, Na, К, Rb, Cs, Fr. Название получили от гидрооксидов ...Щелочные металлы
Цель урока:. познакомиться с историей открытия и распространением щелочных металлов в природе и живых организмах; изучить физические и химические ...Щелочные и щелочноземельные металлы
Щелочные металлы – элементы IA группы. Перечислите известные вам щелочные металлы. Сколько электронов на внешнем энергетическом уровне у атомов всех ...Щелочные металлы
Щелочны́е мета́ллы — элементы главной подгруппы I группы Периодической системы химических элементов Д. И. Менделеева: литий Li, натрий Na, калий K, ...Химические элементы металлы и здоровье человека
Ионы этого металла входят в состав вещества, употребляемого в пищу и называемого «белой смертью». Существенными источниками этого элемента являются ...Конспекты
Общая характеристика элементов 1 группы, главной подгруппы
№. п/п. . Структурные элементы. . . . . Дата. . . 08.10.2014г. . . . Класс. . 9. . . . . Тема урока. . ...Характеристика металлов II группы главной подгруппы
Тема урока:. . Характеристика металлов. II. группы главной подгруппы. Цель урока: дать характеристику металлов II. группы главной подгруппы. ...Общая характеристика элементов главной подгруппы VI группы. Кислород и сера.Важнейшие соединения: оксиды, кислоты и их соли
Класс: 10 , учитель: Султанова Е.А. СШ № 17 , г. Балхаш, химия. Тип урока:. комбинированный,. язык обучения. : русский. Оборудование:. флипчарт, ...Общая характеристика металлов. Металлы главных и побочных подгрупп. Щелочные металлы и их важнейшие соединения
План учебного занятия № 10. Дата Предмет. химия. группа. Ф.И.О. преподавателя. : Кайырбекова И.А. . І. Тема занятия:. Общая характеристика металлов. ...Металлы. Щелочные металлы
ПЛАН-КОНСПЕКТ УРОКА Щелочные металлы. . ФИО (полностью). . . Пономарева Л.Н. . . . Место работы. . . . . . ...Способы классификации химических элементов. Понятие про щелочные металлы и галогены
Тема:. . Способы классификации химических элементов. Понятие про щелочные металлы и галогены. . . Цель:. . Закрепить знания учащихся о ...Элементы IA-IIIA группы ПСХЭ
Дата_____________ Класс_______________. Тема: Общение знаний по теме. «Элементы. IA. -. IIIA. группы ПСХЭ». . Цели урока:. повторить, углубить ...Щелочные металлы
. Урок химии в 9 классе. Щелочные металлы. Цели урока:. Дать общую характеристику ЩМ. Рассмотреть их атомное строение, основные физические, ...Щелочные металлы. Нахождение в природе, свойства и применение
Дата_____________ Класс_______________. Тема: Щелочные металлы. Нахождение в природе, свойства и применение. . Цели урока:. расширить и углубить ...Щелочные металлы
Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». Конспект урока по химии в 9 классе. тема урока " Щелочные ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:2 июля 2018
Категория:Химия
Содержит:13 слайд(ов)
Поделись с друзьями:
Скачать презентацию