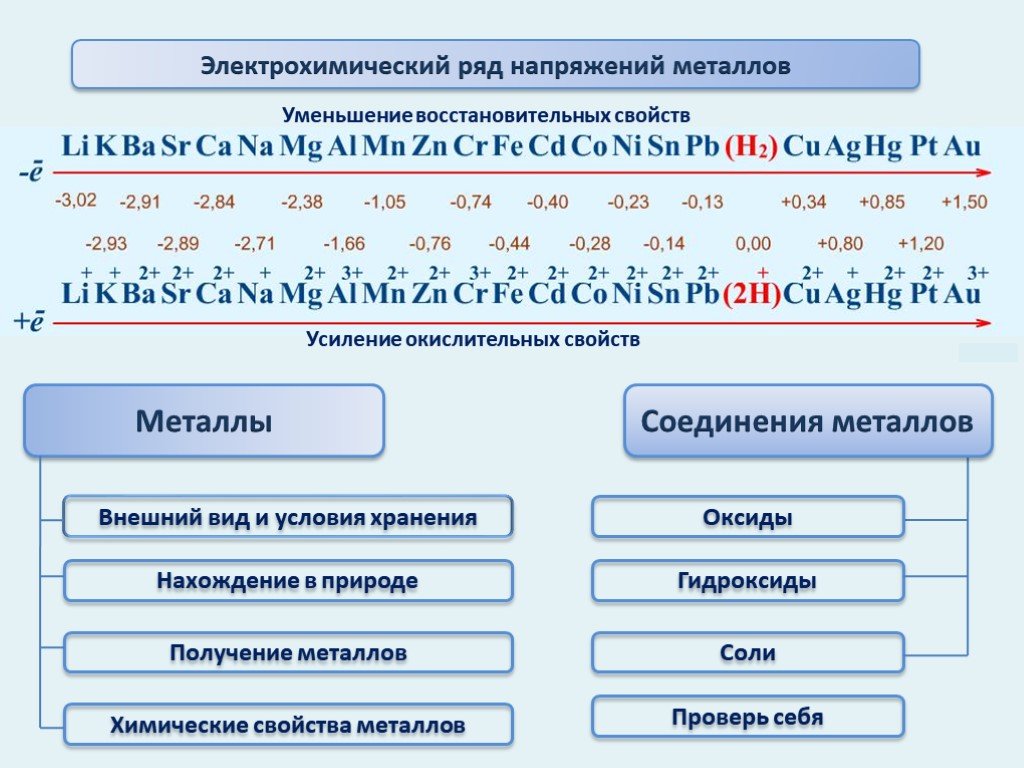
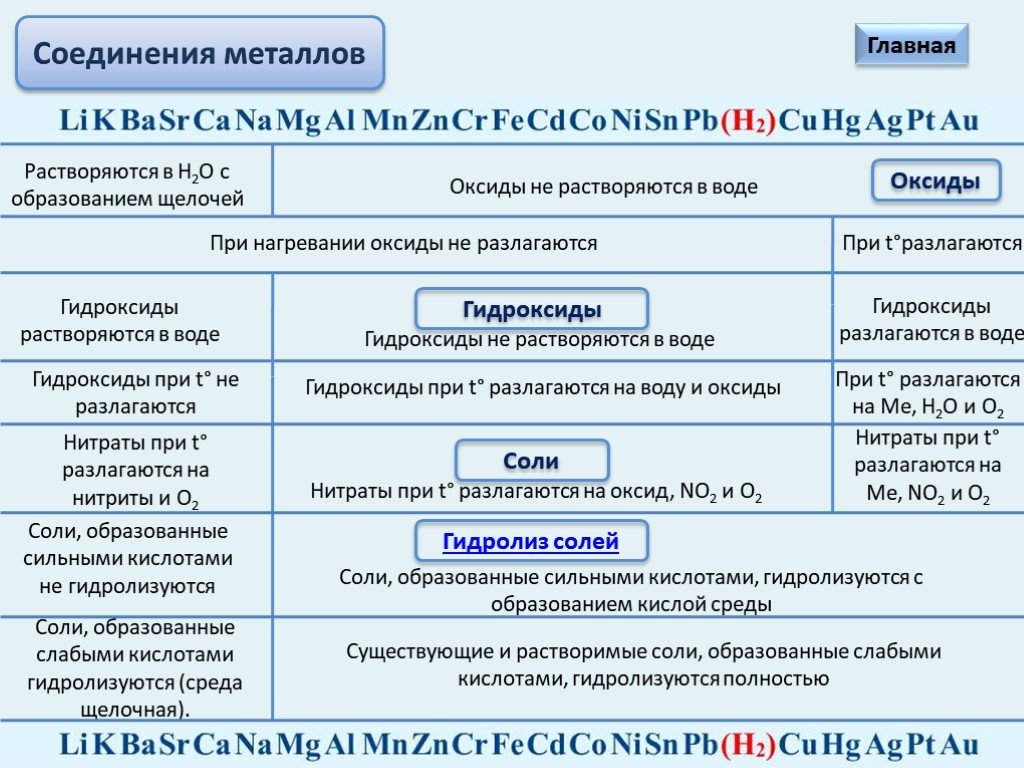
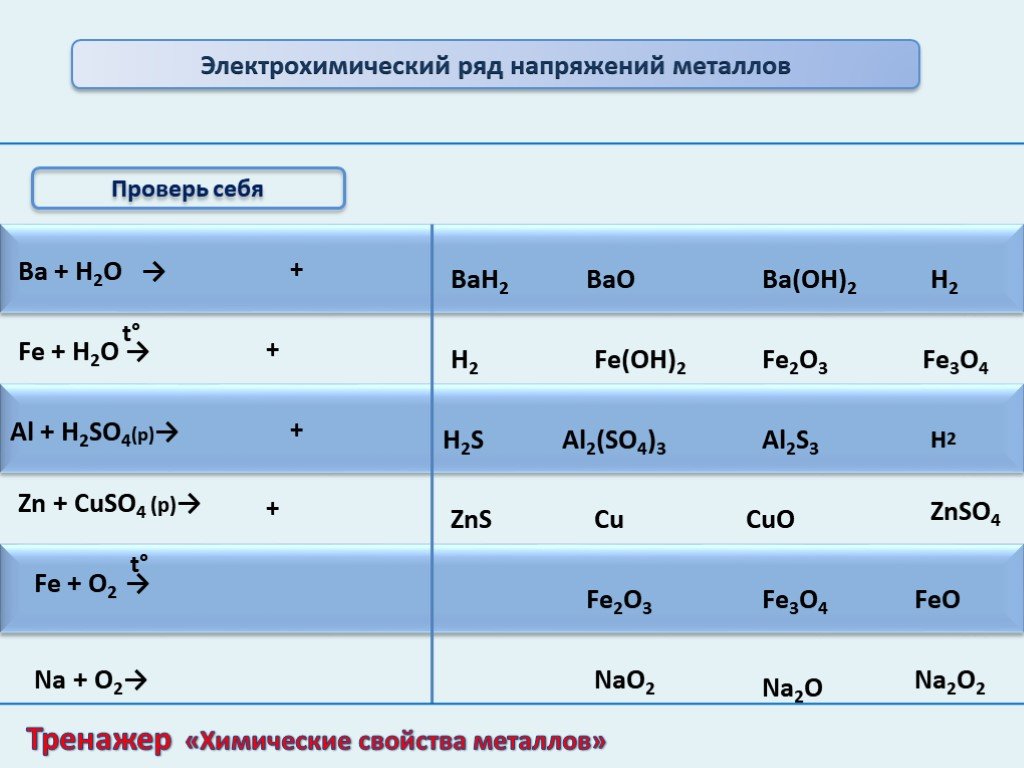
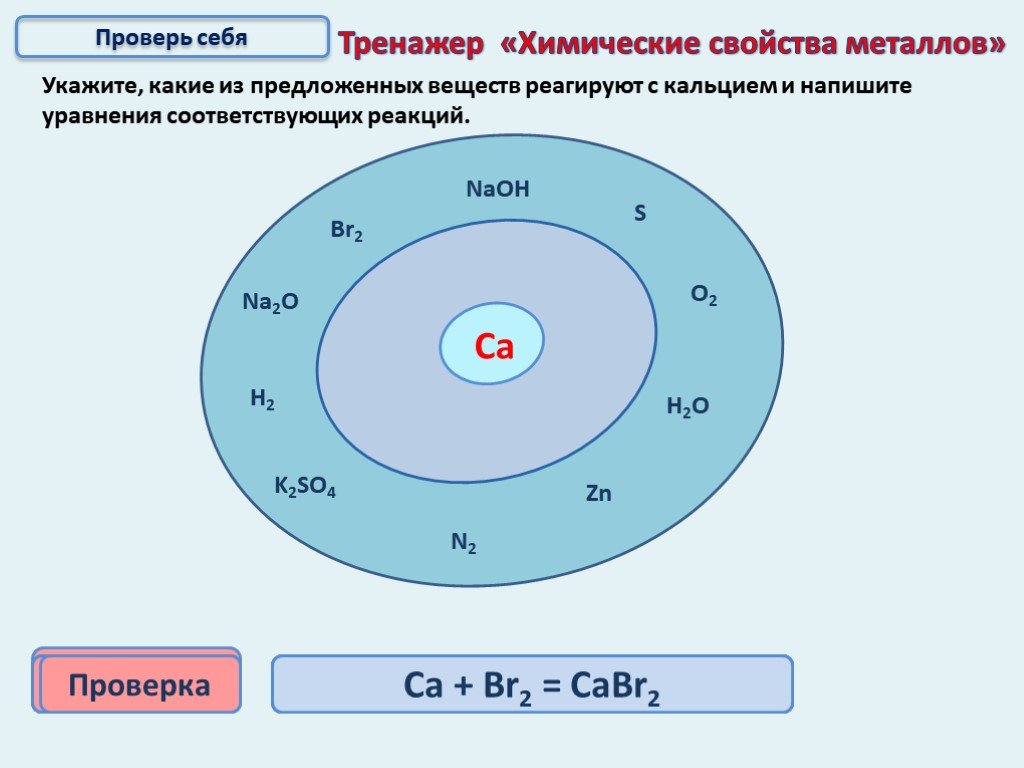
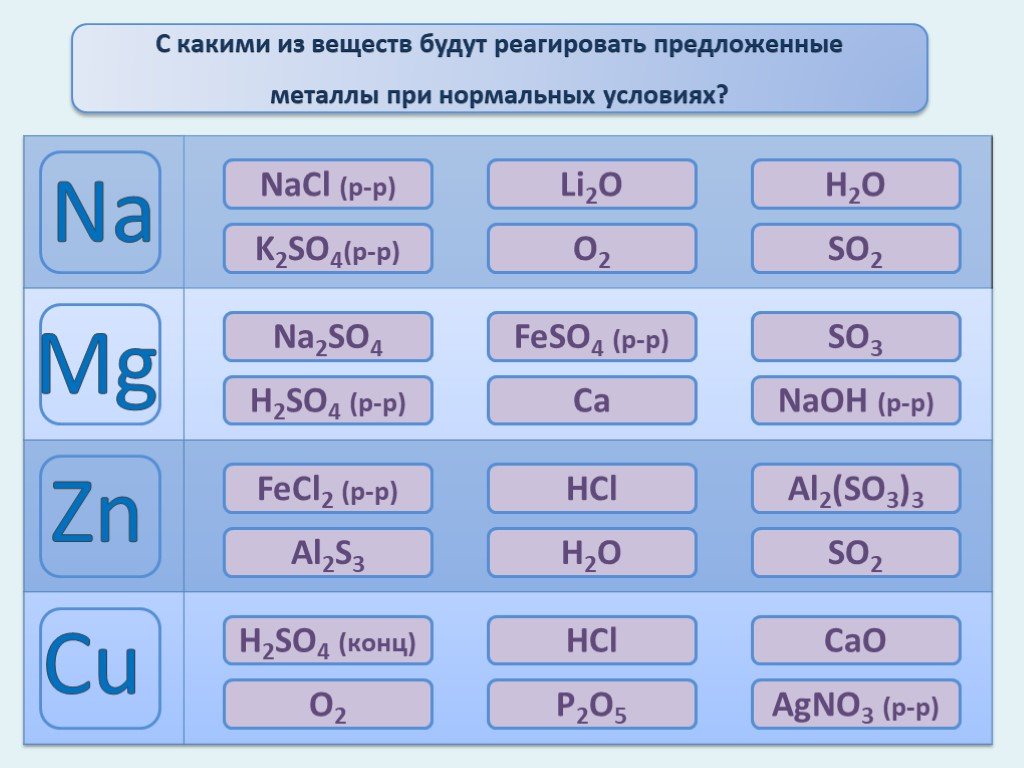
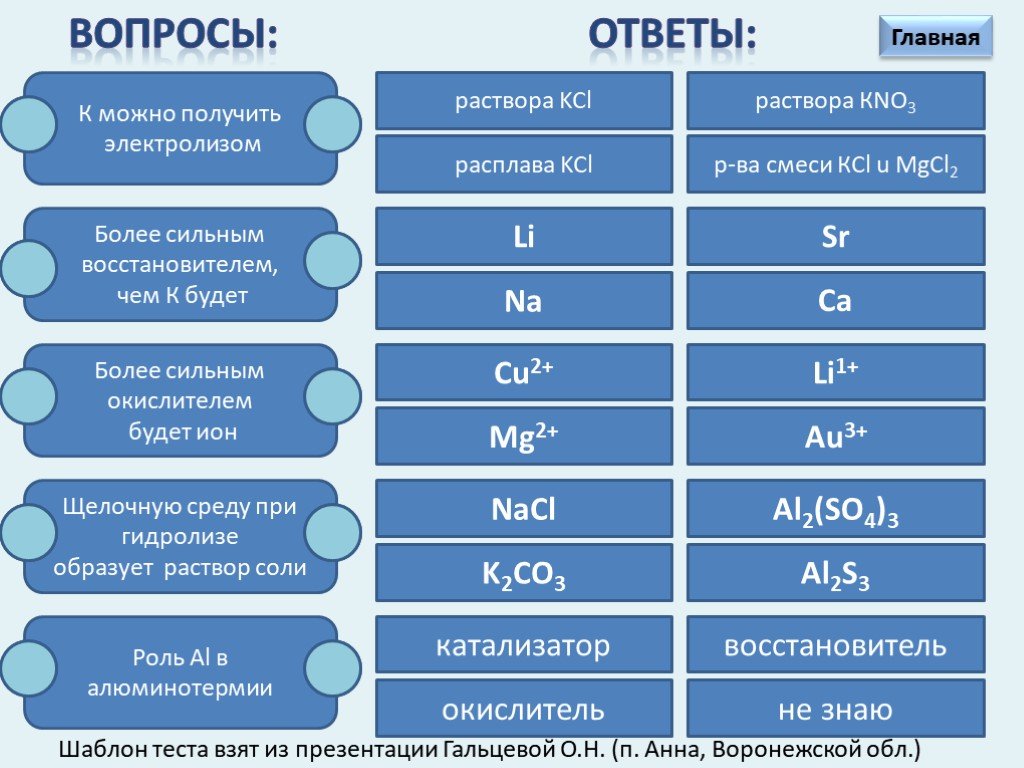
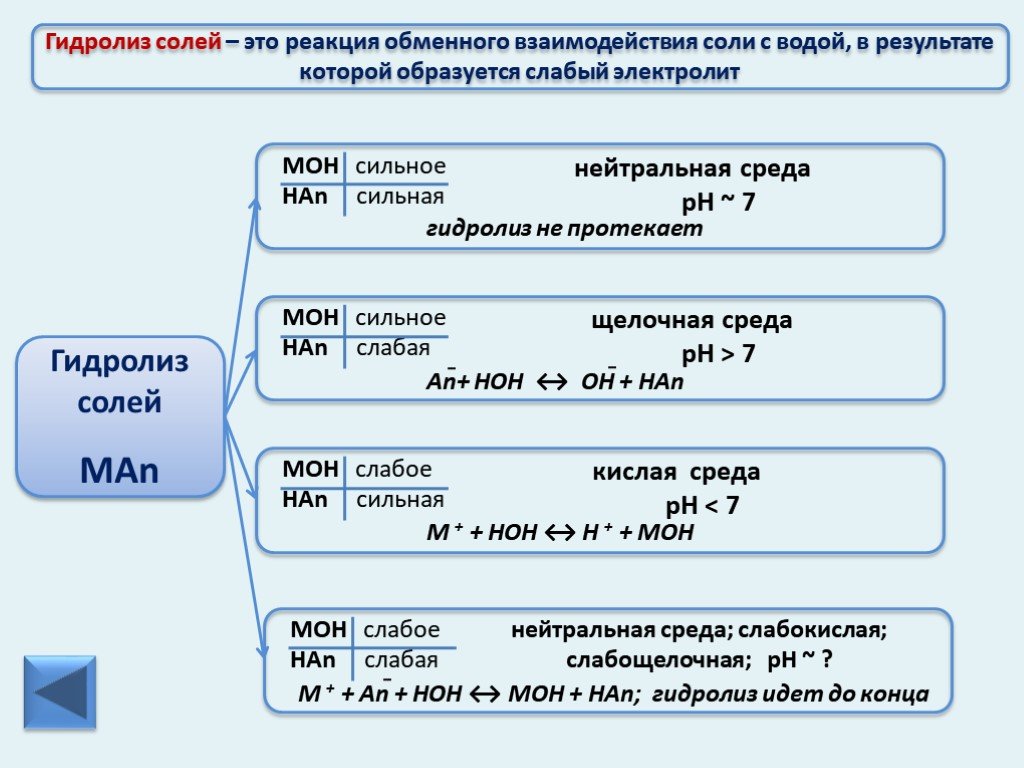
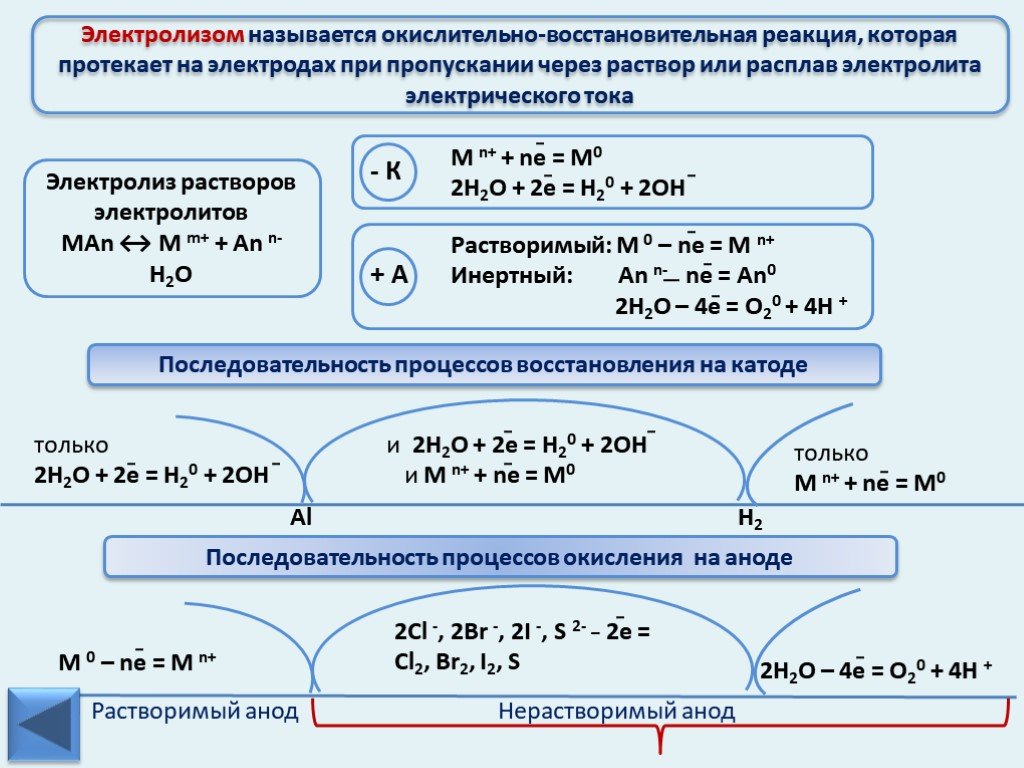
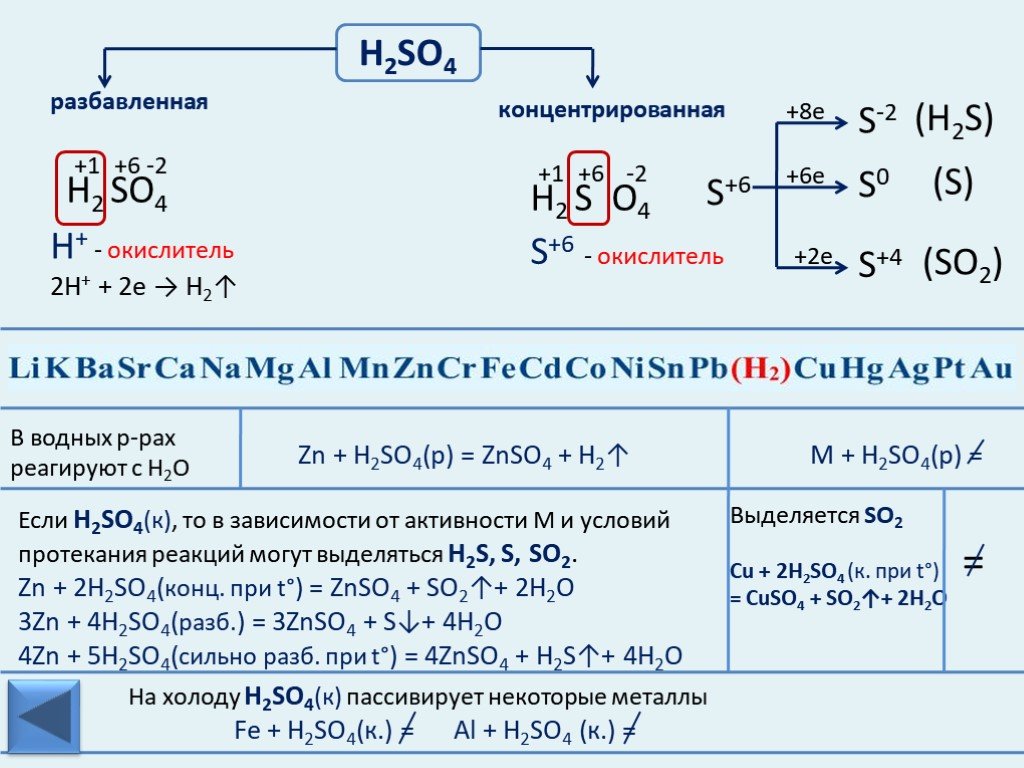
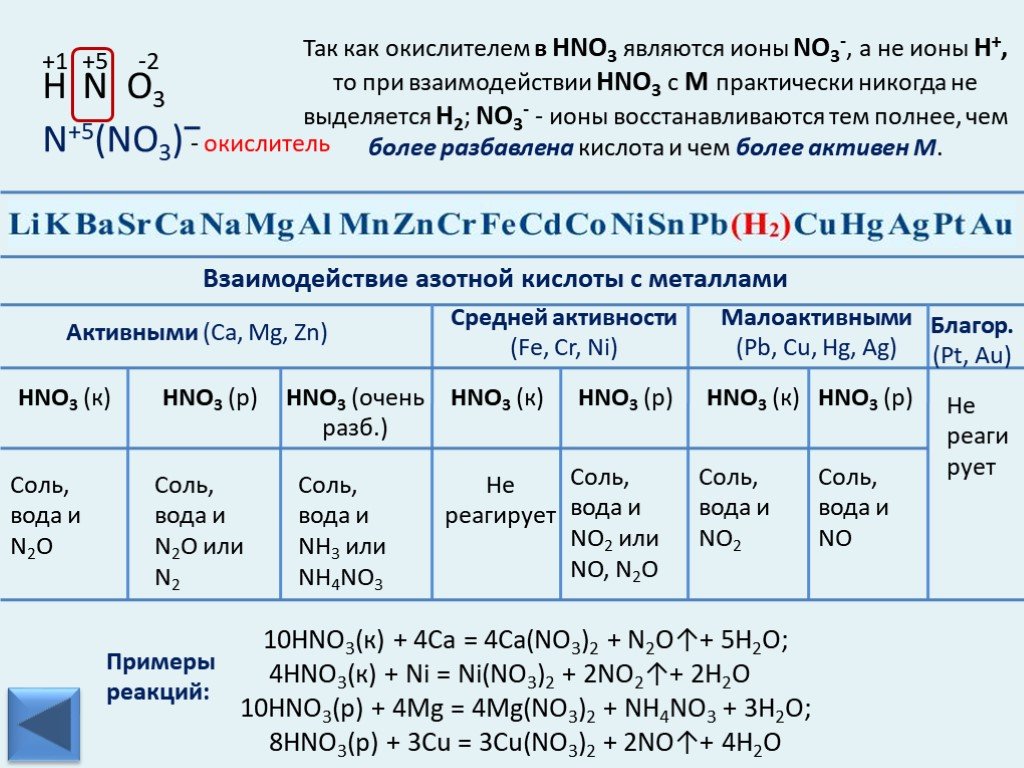
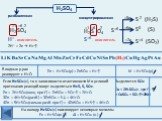
Презентация "Электрохимический ряд напряжений металлов" по химии – проект, доклад
Презентацию на тему "Электрохимический ряд напряжений металлов" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 23 слайд(ов).
Слайды презентации
Список похожих презентаций
"Электрохимический ряд напряжений металлов. Общие химические свойства металлов". 11-й класс
Цель урока:. Повторить и обобщить общие химические свойства металлов с учетом их положения в ЭХРНМ. Задачи урока:. Повторить общие химические свойства ...Реакции замещения. Электрохимический ряд напряжений.
Цель урока:. I. Дать понятие о реакциях замещения. II. Познакомить с: 1) электрохимическим рядом напряжений металлов; 2) условиями взаимодействия ...Химические свойства металлов. Электрохимический ряд напряжения металлов. 11-й класс
Верите ли Вы,что... Металлы занимают верхний левый угол в ПСХЭ. В кристаллах атомы металла связаны металлической связью. Валентные электроны металлов ...Коррозия металлов
Коррозия – рыжая крыса, Грызет металлический лом. В Шефнер. - называют самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды ...Понятие металлов
Урок "Обобщение и закрепление материала по теме: "Металлы". Цели урока:. Повторить и закрепить все основные понятия по теме: «Металлы» с помощью разноплановых ...Строение атомов металлов
Домашнее задание. Параграф 8 По печатной тетради: На «3» - стр.7: № 6,9,10,11. стр.12: №4 На «4,5» - стр.8 №7,8; стр.11№16; стр.13 № 7(последний);стр.14 ...Химические свойства металлов
Верите ли вы, что … Металлы занимают верхний левый угол в ПСХЭ. В кристаллах атомы металла связаны металлической связью. Валентные электроны металлов ...Сплавы металлов
Сплавы – это материалы с характерными свойствами, состоящие из двух или более компонентов, из которых по крайней мере один – металл. СПЛАВЫ. однородные ...Способы получение металлов
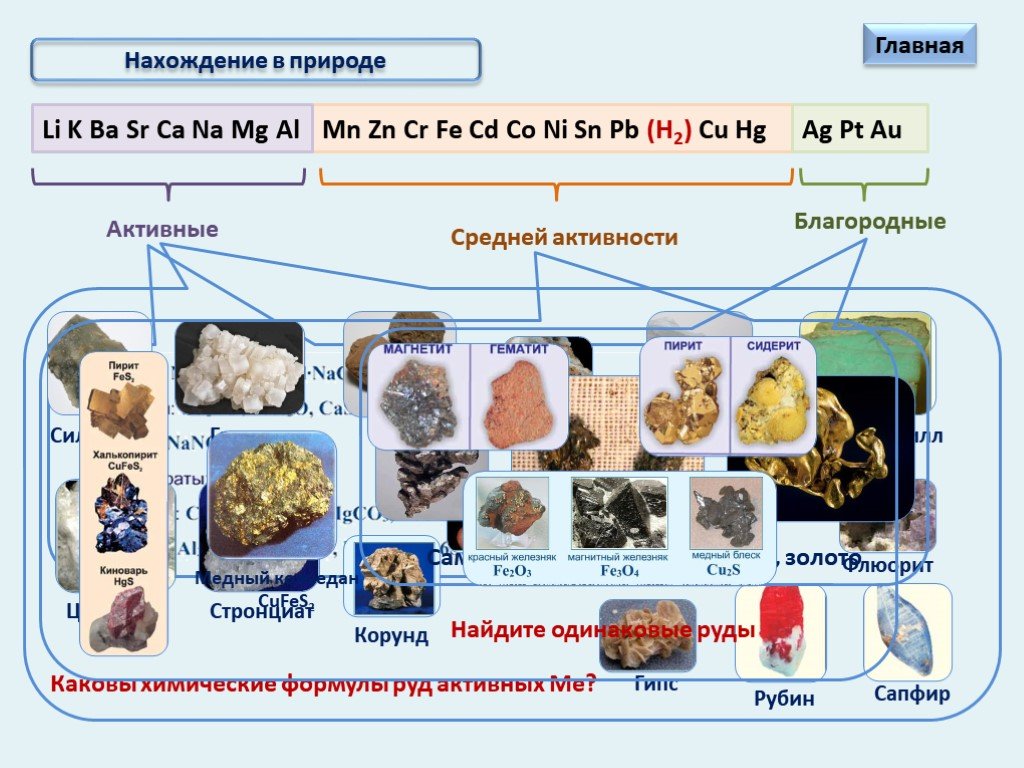
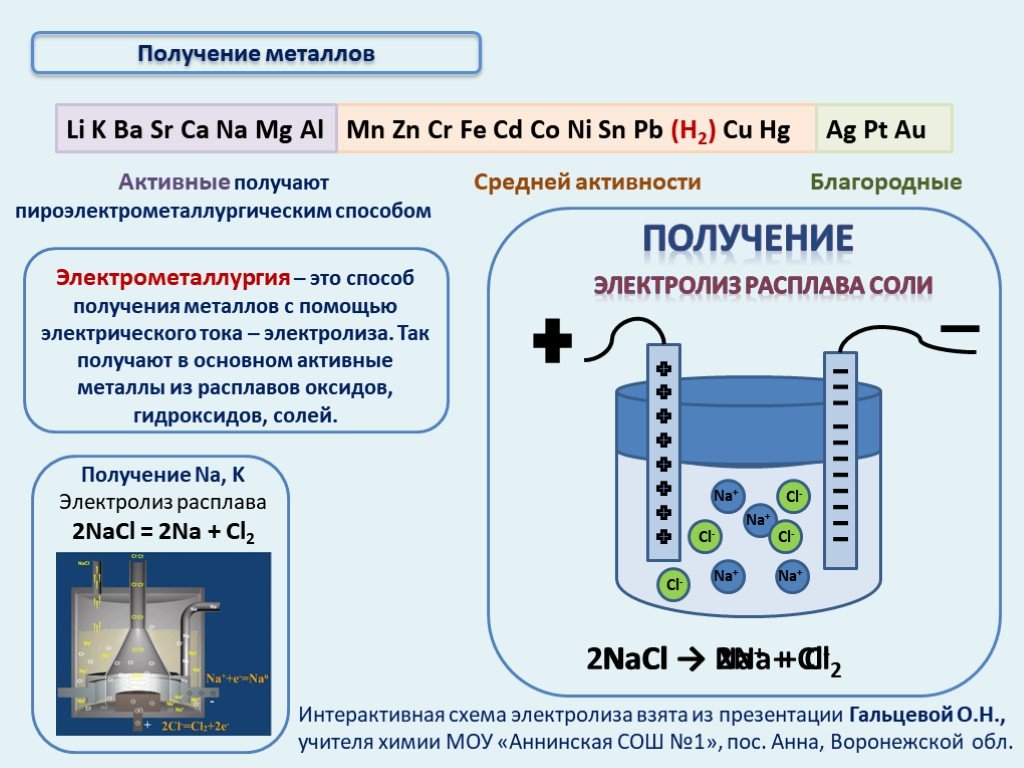
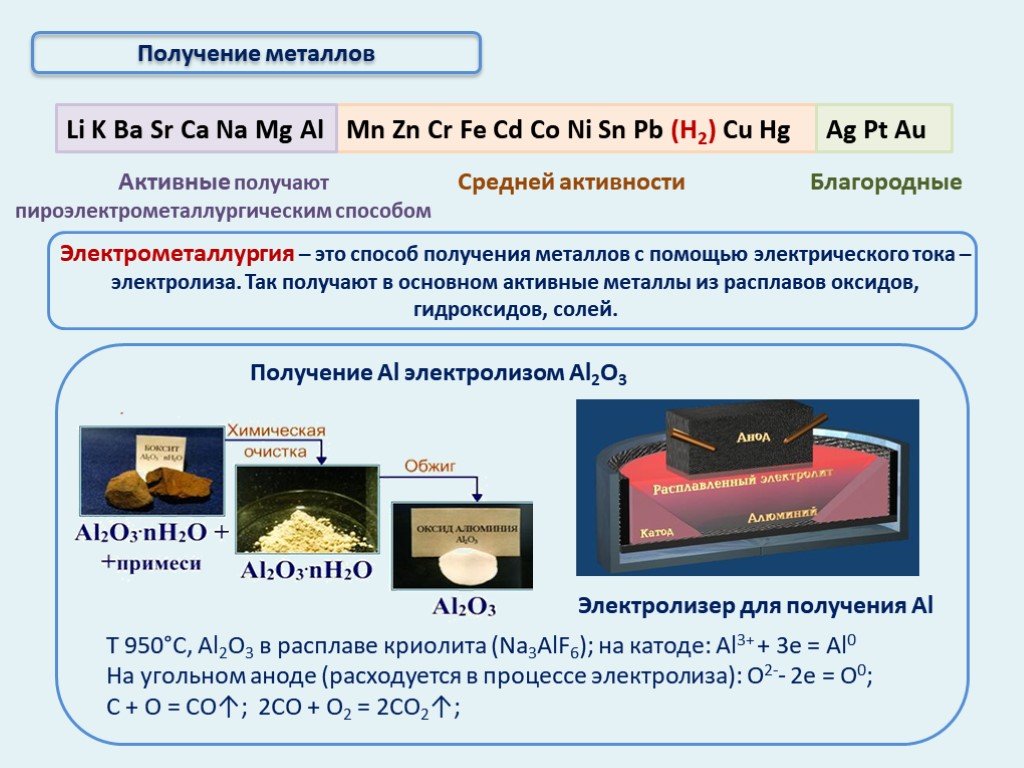
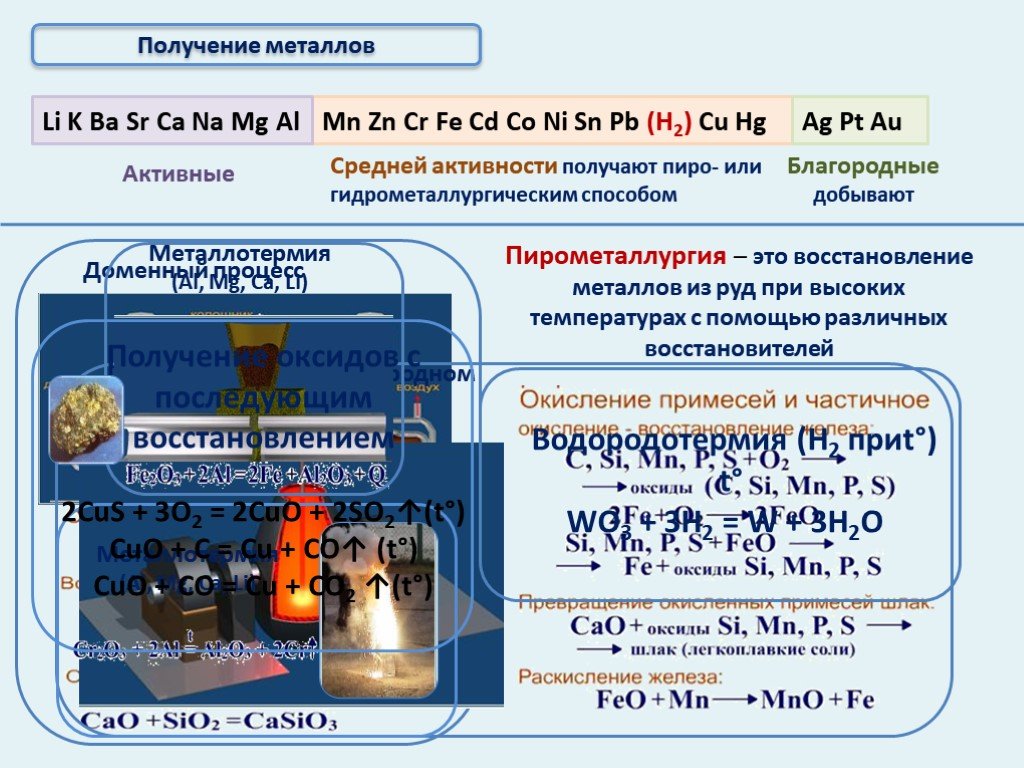
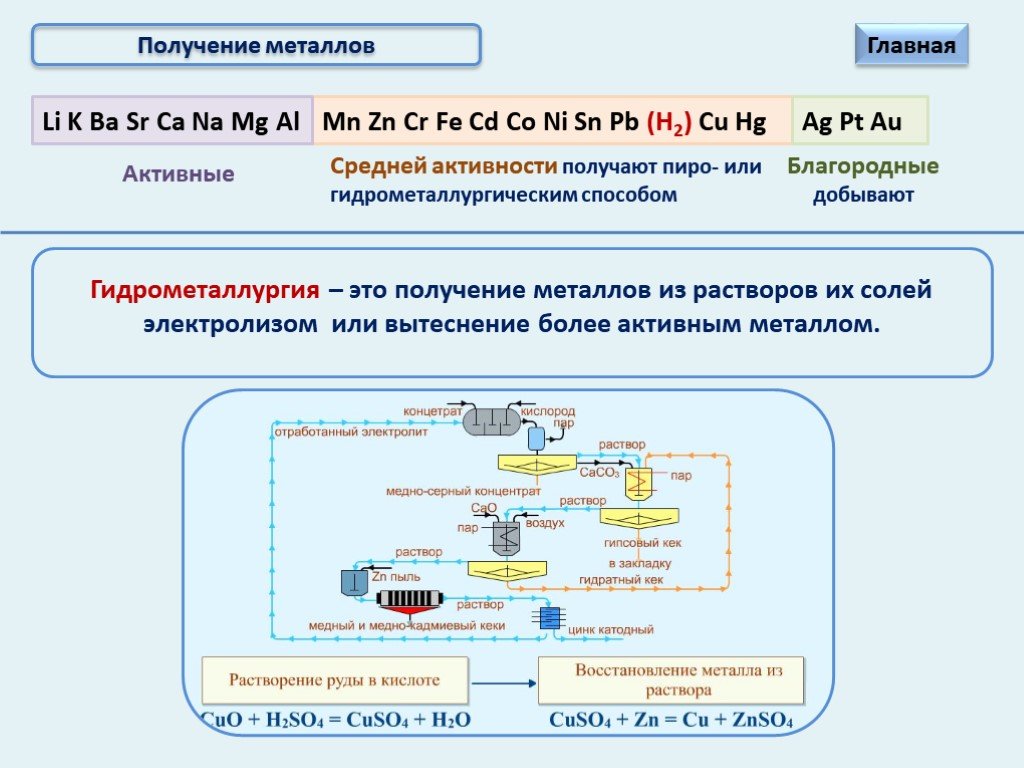
Распространенность металлов в природе. Нахождение металлов в природе. Очень активные металлы. Неактивные (благородные). Средней активности. Важнейшие ...Руды металлов
Полезные ископаемые России, бывшего Советского Союза. . Гематит Гарниерит Лимонит Магнетит Халькопирит Галенит Пирит Боксит Сфалерит Пиролюзит. Формула ...Свойства черных и цветных металлов
Что такое металлы и сплавы? Металл — это вещество, обладающее ярким блеском и хорошей проводимостью тепла и электричества. Сплав — макроскопически ...Качественные реакции на ионы металлов
Проблемный вопрос: каким образом можно определить ионы металлов в растворах. Цель работы: научиться определять ионы металлов Задачи: расширить знания ...Коррозия металлов
Цель. Исследовать действие факторов окружающей среды на степень ржавления металлов. Гипотеза Если поместить железо в щелочную среду, то скорость коррозии ...История металлов
Цель:. Рассказать об открытии металлов. Гипотеза:. Возможно открытие металлов никак не повлияло на развитие цивилизаций. Медь. История цивилизаций ...Изучение свойств оксидов металлов
Цель: определить характер оксидов металлов, имеющихся в школьной лаборатории (оксиды бария, железа, кальция, меди, свинца), изучить их свойства. Задачи: ...Изучение коррозии и защиты металлов
Цель. Изучение проблемы коррозии металлов и исследование коррозийной стойкости металлов и способов их защиты. Задачи. изучить литературу по теме исследований; ...Грозит ли миру военный конфликт из-за металлов?
Плотность металлов. Металлы Лёгкие ρ5 гр/см3. Вся авиационная техника построена на основе сплавов лёгких металлов. Ртуть плотность - 14,19 г/см3. ...Горение металлов
Свойства летучих горючих металлов и их оксидов. На способность металлов возгораться и гореть большое влияние оказывают химические и физические свойства ...Свойства металлов
План реферата. Положение металлов в периодической системе Д.И. Менделеева. Строение атомов металлов, кристаллических решеток. Физические свойства ...Коррозия металлов
Зачем нужны металлы? Что вы узнаете (план изучения темы). Физические свойства металлов. Химические свойства металлов. Mеталлы в нашей жизни. Металлическая ...Конспекты
Химические свойства металлов. Ряд напряжения металлов
Дата_____________ Класс_______________. Тема:. . Химические свойства металлов. Ряд напряжения металлов. Цели урока:. расширить и углубить знания ...Характеристика щелочных металлов
Тема урока: Характеристика щелочных металлов. Цель урока:. . дать общую характеристику щелочных металлов по положению в периодической таблице ...Способы получения металлов
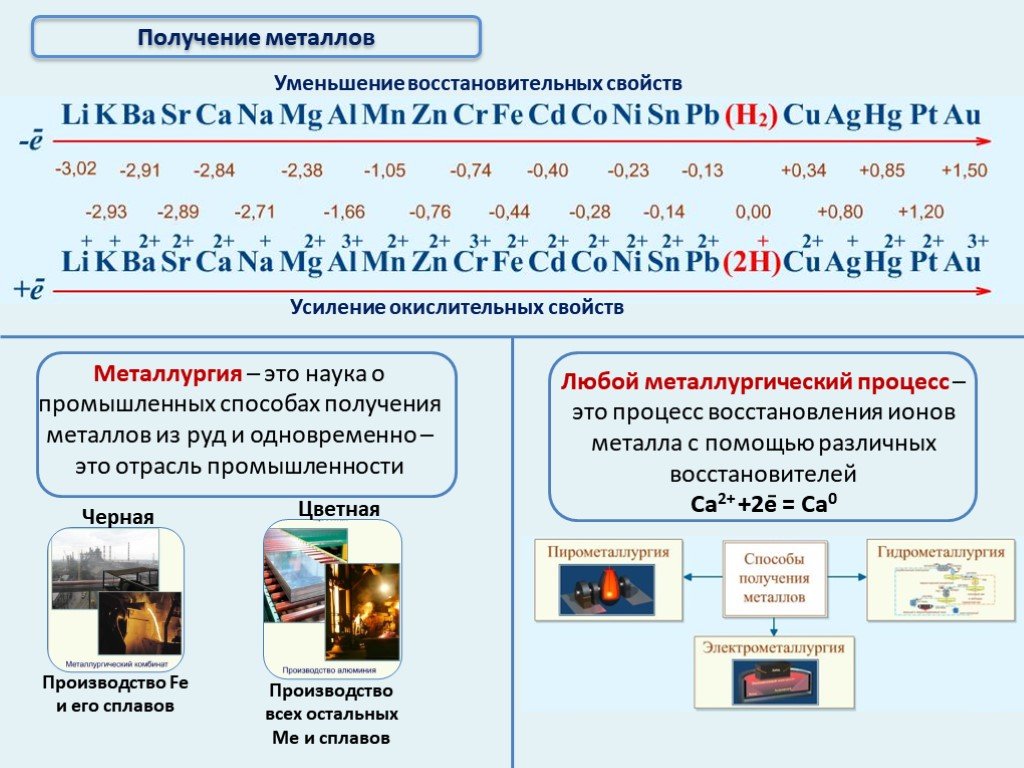
Разработка урока для учащихся 10 класса. Тема урока. «Способы получения металлов». Цель урока:. . Рассмотреть запасы природных соединений металлов ...Роль металлов и их соединений в природной среде и в живых организмах
Дата. . . Предмет химия. . Класс 9 Урок 45. . . . Название занятия. . . Роль металлов и их соединений в природной среде. и в живых ...Практическая работа № 1 Получение и свойства соединений металлов
Лысоконь Ирина Алексеевна. МБОУ СОШ № 2 ст. Архонская Пригородного района РСО-Алания. Учитель химии. Тема урока: Практическая работа № 1 Получение ...Положение металлов в периодической системе химических элементов Д. И. Менделеева. Металлическая связь
Дата_____________ Класс_______________. Тема:. . Положение металлов в периодической системе химических элементов Д. И. Менделеева. Металлическая ...Алкены. Гомологический ряд, номенклатура, изомерия, получения
Конспект урока на тему. «Алкены. Гомологический ряд, номенклатура, изомерия, получения». Цель:. - познакомиться с этиленовыми углеводородами, ...Химические свойства металлов
Тема: «Химические свойства металлов». Цель урока:. Сформировать понятие об общих химических свойствах металлов и их восстановительных способностях. ...Качественное определение ионов металлов в воде реки Лысьва
Урок химии в 9-м классе. . . «. Качественное определение ионов металлов в воде реки Лысьва». Учитель химии: Шилоносова Елена Леонидовна. Образовательная ...Значение металлов в жизни человека
Тема:. Значение металлов в жизни человека. Цель урока:. Формирование знаний о значении металлов в жизни человека. Задачи:. обучающие:. знать ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:23 мая 2019
Категория:Химия
Автор презентации:Генералова Т.Я.
Содержит:23 слайд(ов)
Поделись с друзьями:
Скачать презентацию