"Электрохимический ряд напряжений металлов. Общие химические свойства металлов". 11-й класс презентация, проект, доклад
Презентацию на тему ""Электрохимический ряд напряжений металлов. Общие химические свойства металлов". 11-й класс" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 23 слайд(ов).
Слайды презентации
Список похожих презентаций
Металлы. Химические и физические свойства металлов
Физические свойства металлов. Очень важным свойством металлов является их сравнительно легкая механическая деформируемость. Металлы пластичны, они ...Общие свойства металлов
Цель: обобщить знания учащихся об основных свойствах элементов-металлов и образуемых ими простых и сложных веществ. Задачи: Развитие умения записывать ...Металы. Общая характеристика металлов. Физические свойства и применение металлов
Цели урока: повторить и обобщить сведения о металлической химической связи и кристаллической металлической решетке. Изучить общие физические свойства ...Металлы, свойства металлов
Металлы – химические элементы , образующие в свободном состоянии простые вещества с металлической связью. М.В. Ломоносов - металлы «светлое тело, ...Качественные реакции на ионы металлов
Проблемный вопрос: каким образом можно определить ионы металлов в растворах. Цель работы: научиться определять ионы металлов Задачи: расширить знания ...Основания. Химические свойства оснований
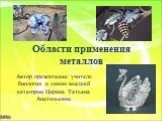
Классификация оснований. Растворимые в воде (щелочи). Нерастворимые в воде. NaOH Ca(OH)2 Al(OH)3 Сu(OH)2. Название оснований. Гидроксид +. Название ...Области применения металлов
Железо. Железо издревле использовалось в качестве лекарства. В папирусах Египта ржавчина предписывалась в качестве мази от облысения. В XVII веке ...Карбоновые кислоты в природе, химические свойства, применение
План конференции:. 1. «мозговой штурм» 2. Блицопрос 3.Презентация (часть1): номенклатура, строение, классификация 4. Пресс-конференция 5. Презентация ...Общая характеристика металлов главных подгрупп I-III
Характеристика металлов главной подгруппы I группы. Щелочны́е мета́ллы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr. Эти металлы ...Нахождение металлов в природе
Большая часть металлов присутствует в природе в виде руд и соединений. Они образуют оксиды, сульфиды, карбонаты и другие химические соединения. Для ...Нахождение металлов и их соединений в природе
«Человек не может обойтись без металлов. Если бы не металлы, человек влачил бы самую жалкую жизнь среди диких зверей» Г. Агрикола XVI век. Альманах ...Методы очистки воды от тяжелых металлов
Тяжелые металлы:. Биогеохимические свойства тяжелых металлов. Технологии очистки промышленных сточных вод от следов тяжелых металлов. Метод электрокоагуляции ...Альдегиды получение, применение, физические и химические свойства
Парфюмерная продукция. Верхние ноты: бергамота, нероли, лимона Средние ноты: ландыша, ириса, жасмина Базовые ноты: мускуса, ванили, сандалового дерева. ...Алкины-способы получения и химические свойства
Тема и цели урока:. Тема: «Ацетилен. Алкины». Цель урока: Дать представления об углеводородах с тройной связью. О их физико-химических свойствах и ...Мир металлов
Содержание. Золото. Серебро. Медь. Бронза. Железо. Чугун. Сталь. Золото. Из золота можно изготовить проволоку в тысячу раз более тонкую, чем человеческий ...Алюминий – металл ХХ века. Физические и химические свойства
Алюминий. Алюминий вы найдете В ложке, кружке, самолете. Нужен легонький металл, Чтобы самолет летал! Самолет парит легко, Небосвод пронзает синий, ...Изучение свойств оксидов металлов
Цель: определить характер оксидов металлов, имеющихся в школьной лаборатории (оксиды бария, железа, кальция, меди, свинца), изучить их свойства. Задачи: ...История металлов
Цель:. Рассказать об открытии металлов. Гипотеза:. Возможно открытие металлов никак не повлияло на развитие цивилизаций. Медь. История цивилизаций ...Кремний, его физические и химические свойства
Цели урока: - рассмотреть положение кремния в периодической системе Д.И.Менделеева и строении его атома; - рассмотреть нахождение кремния в природе; ...Металлоорганические соединения непереходных металлов
Лекция 2 Характерные типы и энергетика связей металл-углерод Основные синтетические подходы к металлоорганическим соединениям. Характерные типы связей ...Конспекты
Общие свойства металлов
Общие свойства металлов. Цели урока:. . Образовательная: Исходя, из нахождения в таблице Д.И. Менделеева рассмотреть строение атома, выяснить тип ...Общие свойства металлов
Муниципальное бюджетное образовательное учреждение. «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА № 3». Конспект урока по химии в 9 классе. «Общие ...Алканы. Гомологический ряд, изомеры, номенклатура, свойства и получение алканов Цели: Изучить алканы, как один из классов ациклических соединений
План учебного занятия №. 19. Дата Предмет. Химия. группа. Ф.И.О. преподавателя: Кайырбекова И.А. . Тема. :. Алканы. Гомологический ряд, изомеры, ...Общие способы получения металлов
Тема:. "Общие способы получения металлов" 9-класс. Цель урока. :. познакомить с природными соединениями металлов и с самородными металлами; дать ...Основания, их классификация и химические свойства в свете теории электролитической диссоциации
ТЕМА УРОКА :. Основания, их классификация и химические свойства в. . свете теории электролитической диссоциации. . . II. слайд:. ЦЕЛЬ УРОКА:. ...Получение и свойства соединений металлов
Муниципальное общеобразовательное учреждение лицей. Технологическая карта урока по химии. Практическая работа. «Получение и свойства соединений ...Практическая работа № 1 Получение и свойства соединений металлов
Лысоконь Ирина Алексеевна. МБОУ СОШ № 2 ст. Архонская Пригородного района РСО-Алания. Учитель химии. Тема урока: Практическая работа № 1 Получение ...Кислоты. Классификация. Химические свойства с точки зрения электролитической диссоциации
8 класс. . . Урок-игра «Химическое лукошко» по теме «Урок-упражнение по теме «Кислоты. Классификация. Химические свойства с точки зрения электролитической ...Кислоты органические и неорганические. Классификация и общие свойства кислот
Конспект открытого урока химии в 11 классе. «Кислоты органические и неорганические. Классификация и общие свойства кислот». Тема урока. Кислоты. ...Кислоты, их состав, классификация, общие свойства
Информационный план-проспект урока. №. . Описание. . . . Тип урока. . Урок изучения нового материала с использованием химического ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:18 октября 2018
Категория:Химия
Классы:
Содержит:23 слайд(ов)
Поделись с друзьями:
Скачать презентацию





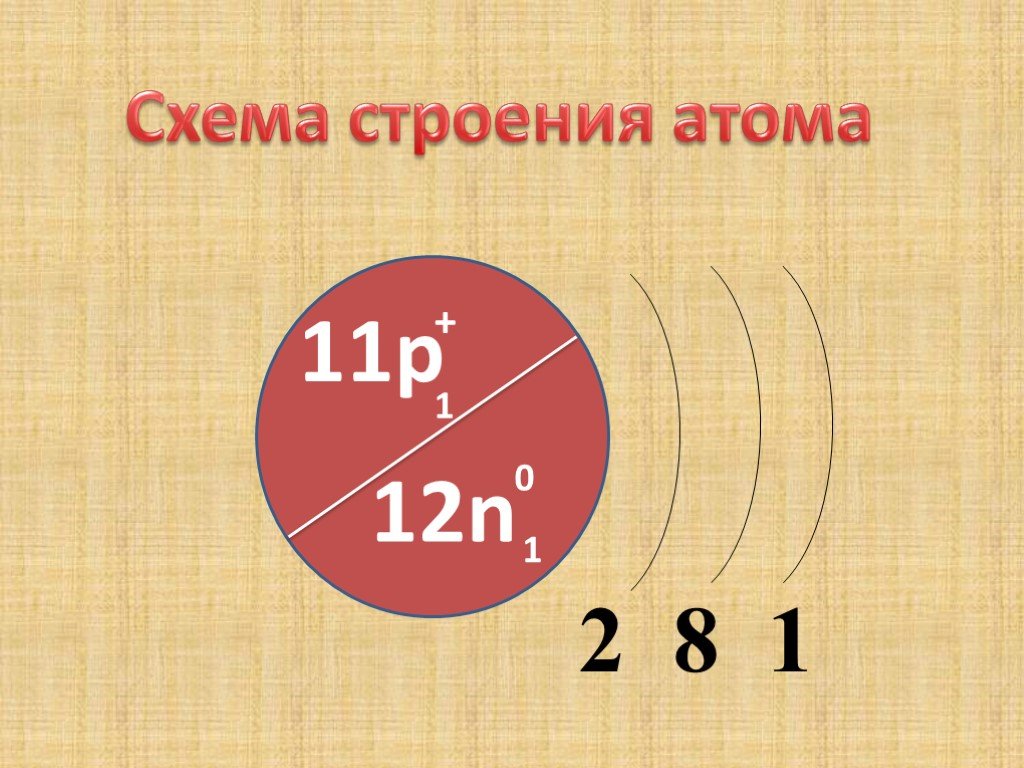




























![3. Взаимодействие золота с «царской водкой» Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O 3. Взаимодействие золота с «царской водкой» Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O](https://prezentacii.org/upload/cloud/18/10/88358/images/thumbs/screen15.jpg)