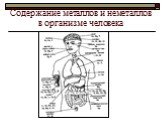
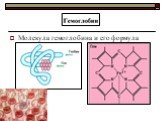
Презентация "Органические соединения железа" по химии – проект, доклад
Презентацию на тему "Органические соединения железа" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 22 слайд(ов).
Слайды презентации
Список похожих презентаций
Кислородсодержащие органические соединения
КИСЛОРОДСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ. Кафедра ЭПП, к.х.н., доцент Саверченко А.Н. Студент должен: знать строение, номенклатуру, свойства, способы ...Соединения железа
Железо расположено в 4 периоде, в побочной подгруппе VIII группы Периодической системы химических элементов Д.И.Менделеева. Относительная атомная ...Керамики - неорганические соединения
Еще Глейтером в 1981 году был введен термин «нанокристаллические» материалы, позже стали использоваться такие термины как «наноструктурные», «нанофазные», ...Неорганические соединения - формулы и реакции
Цели урока. В игровой форме обобщить и закрепить знания о химических свойствах основных классов неорганических соединений и их взаимопревращениях. ...Химический состав клетки. Неорганические соединения
Что же до первоначал, то они еще больше имеют Средств для того, чтоб из них возникали различные вещи, Нет ни одной из вещей, доступных для нашего ...Жиры – биологически важные органические соединения
Содержание. Нахождение жиров в природе. История изучения жиров. Строение и разнообразие жиров. Физические свойства жиров. Химические свойства жиров. ...Неорганические соединения
Цель: Повторить и обобщить знания, умения и навыки по данной теме. Фронтальный опрос. Что такое степень окисления? Какие соединения называются бинарными? ...Металлоорганические соединения непереходных металлов
Лекция 2 Характерные типы и энергетика связей металл-углерод Основные синтетические подходы к металлоорганическим соединениям. Характерные типы связей ...Ферменты как биологически активные соединения
Ферменты (энзимы) – это органические катализаторы белковой природы, которые ускоряют реакции, необходимые для функционирования живых организмов. Типы ...Сера и её соединения
Валентные состояния атома серы S. Валентность II, ст. окисления -2. 3s 3p 3d. Валентность IV, Ст. окисления +4. Валентность VI, Ст. окисления +6. ...Структура ячейки на примере атома железа
Периоды Группы 1 3 4 5 6 7 I II III IV V VII VIII VI малые большие А Б. Условная граница от бора до астата. Бор Кремний Мышьяк Теллур Астат Металлы ...Органические кислоты
Выберите раздел Лимонная кислота. Муравьиная кислота. Ацетилсалициловая кислота. Молочная кислота Яблочная кислота. Высшие жирные кислоты. Уксусная ...Поли- и гетерофункциональные соединения, участвующие в процессах жизнидеятельности
Особенности химического поведения полифункциональных соединений. 1. Кислотно-основные свойства полифункциональных соединений. Антифриз. Кислотные ...НЕМЕТАЛЛЫ природные соединения применения продуктов их переработки
Элементы в природе. Нахождение в природе. Самородные элементы. Сера Графит С Алмаз С. Азот и кислород, инертные газы в составе воздуха. Нахождение ...Важнейшие соединения серы
Сероводород выделяется в результате вулканической деятельности, при гниении белков животных и растений, при работе производств химической, текстильной, ...Галогены и их соединения
Цели урока:. Рассмотреть свойства и применение важнейших соединений галогенов. Изучить качественные реакции на галогенид-ионы. Рассмотреть свойства ...Галогены и их соединения
СОДЕРЖАНИЕ. 1. Общая характеристика галогенов 2. Фтор 3. Хлор 4. Бром 5. Йод 6. Соединения галогенов. Общая характеристика галогенов. Hal неметаллы ...Все о железе и его соединения
Урок-проект в 9 классе подготовила Яскевич В.А. учитель химии МОУ «Кадетская школа «Патриот» г.Энгельса 2010 г. План изучения вещества. Железо как ...Галогены и их соединения
Опыт и наблюдение- таковы величайшие источники мудрости, доступ к которым открыт для каждого человека. (Чаннинг.). Вопросы:. Что такое «вытеснительный ...Водородные соединения неметаллов
метан аммиак вода сероводород кислоты. Метан. Газ без цвета и запаха, малорастворим в воде, легче воздуха, горит бледным синеватым пламенем. Смесь ...Конспекты
Кислородсодержащие органические соединения
Е.А.Кудравец, учитель химии. МОУ гимназии № 32. . Дидактическая разработка урока. . Тема:. «Кислородосодержащие органические соединения». ...Химический состав клеток. Неорганические соединения клетки
Урок на тему. «Химический состав клеток. Неорганические соединения клетки». Цели урока:. Расширение и углубление знаний учащихся о роли металлов ...Кислородсодержащие органические соединения и их природные источники
ПЛАН-КОНСПЕКТ УРОКА. «Химические свойства спиртов». . ФИО (полностью). . Хочуева Фатима Заурбековна. . . . Место работы. . ...Азотосодержащие органические соединения
4. . . Урок разработала Серебрянская Нелля Александровна,. учитель химии МОУ «Образцовская СОШ». Фроловского муниципального района. Волгоградской ...Кислородсодержащие органические соединения
Модульное изучение темы «. Кислородсодержащие органические соединения. ».10 класс. Цель:. создание условий для выявления учащимися взаимосвязи между ...Азотсодержащие органические соединения и их нахождение в живой природе
Рекомендации по изучению темы. «Азотсодержащие органические соединения и их нахождение в живой природе». . . 1. . Амины. . Понятие об ...Соединения железа
Класс:. 9. Тема урока:. «. Соединения железа». Цель урока:. организовать деятельность учащихся по усвоению и первичному закреплению знаний ...Кислородосодержащие органические соединения
Конспект урока химии 10 класс по теме. . Кислородосодержащие органические соединения. Файрушина Зифа Рустямовна. Учитель химии МБОУ СОШ с. Калтыманово, ...Соединения железа
МКОУ Богучарская общеобразовательная школа № 2. Учитель химии Хаустова Ольга Анатольевна. . Класс:. 9. Тема урока:. . Соединения железа. Тип ...Соединения железа
. . Тема: «Соединения железа». Урок-исследование. Цель:. изучить состав , получение и свойства гидроксидов железа, научиться распознавать ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:1 апреля 2019
Категория:Химия
Содержит:22 слайд(ов)
Поделись с друзьями:
Скачать презентацию


















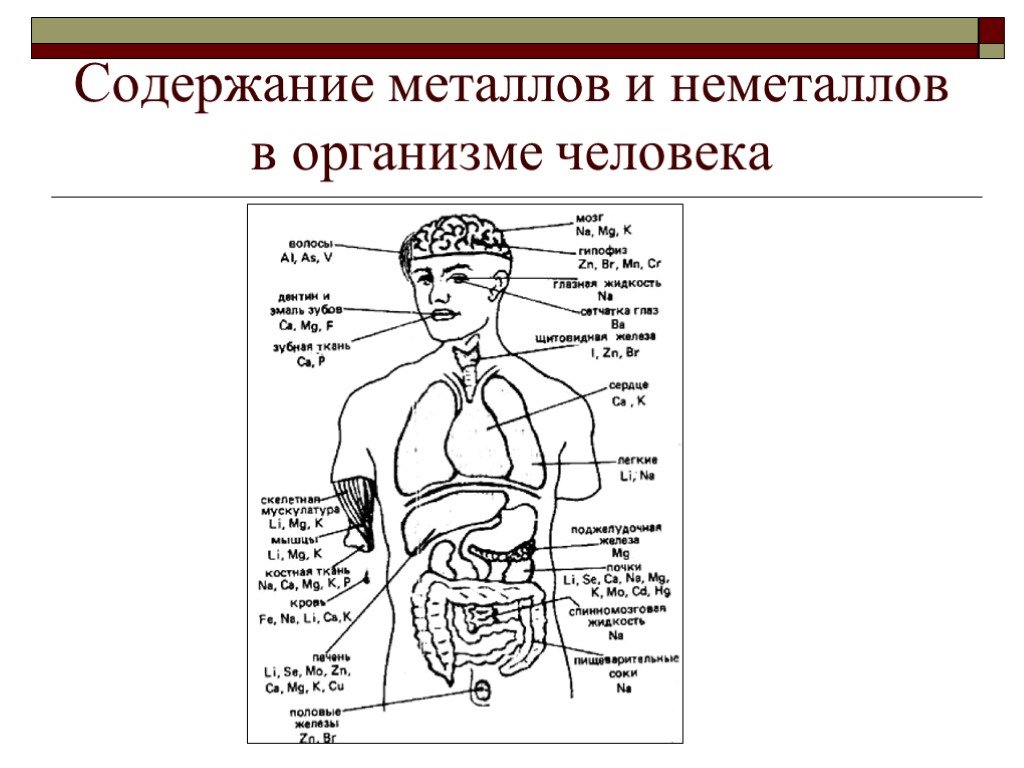














![Качественная реакция на ион Fе2+. Качественная реакция на ион Fе2+ 1.Реактив – красная кровяная соль К3[Fе(СN)6 ] Результат – синий осадок( турнбулева синь) 3FeSO4+2К3[Fе+3(СN)6 ]→Fe3 [Fе(СN)6 ]2 +3К2SO4 Качественная реакция на ион Fе2+. Качественная реакция на ион Fе2+ 1.Реактив – красная кровяная соль К3[Fе(СN)6 ] Результат – синий осадок( турнбулева синь) 3FeSO4+2К3[Fе+3(СN)6 ]→Fe3 [Fе(СN)6 ]2 +3К2SO4](https://prezentacii.org/upload/cloud/19/04/138347/images/thumbs/screen12.jpg)
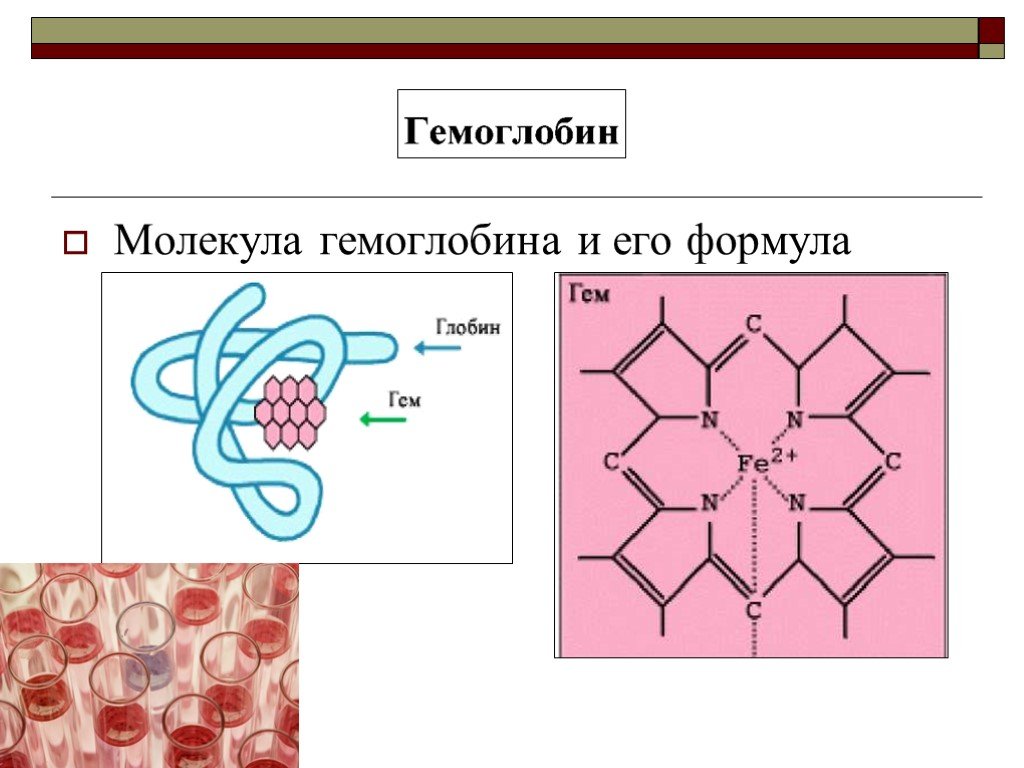
![Качественная реакция на ион Fе3+. Реактив – желтая кровяная соль К4[Fе(СN)6] Результат – синий осадок(берлинская лазурь) 4FeCl3+К4[Fе+2(СN)6 ] →Fe4[Fе(СN)6 ]3 + 12KCl Качественная реакция на ион Fе3+. Реактив – желтая кровяная соль К4[Fе(СN)6] Результат – синий осадок(берлинская лазурь) 4FeCl3+К4[Fе+2(СN)6 ] →Fe4[Fе(СN)6 ]3 + 12KCl](https://prezentacii.org/upload/cloud/19/04/138347/images/thumbs/screen13.jpg)