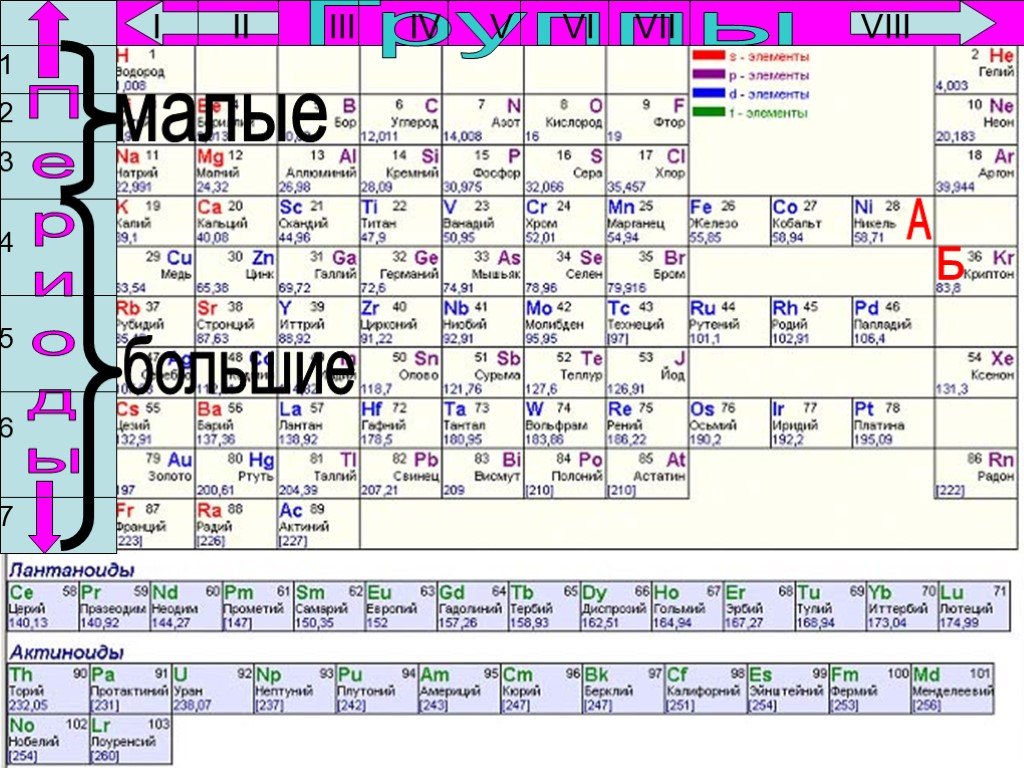
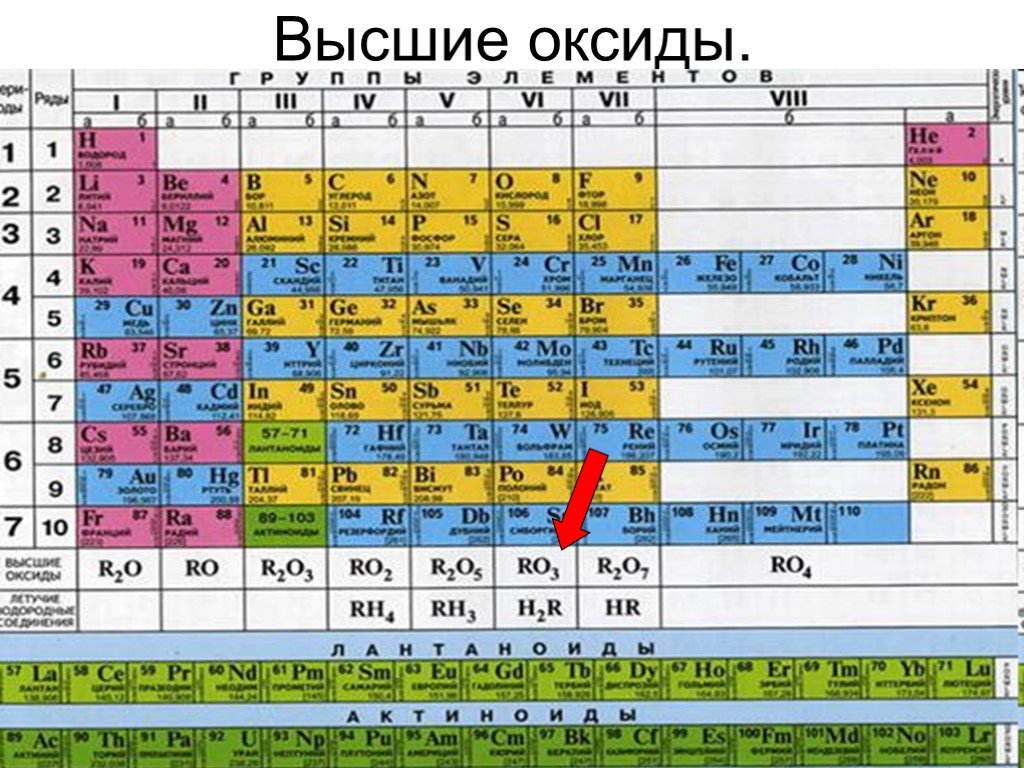
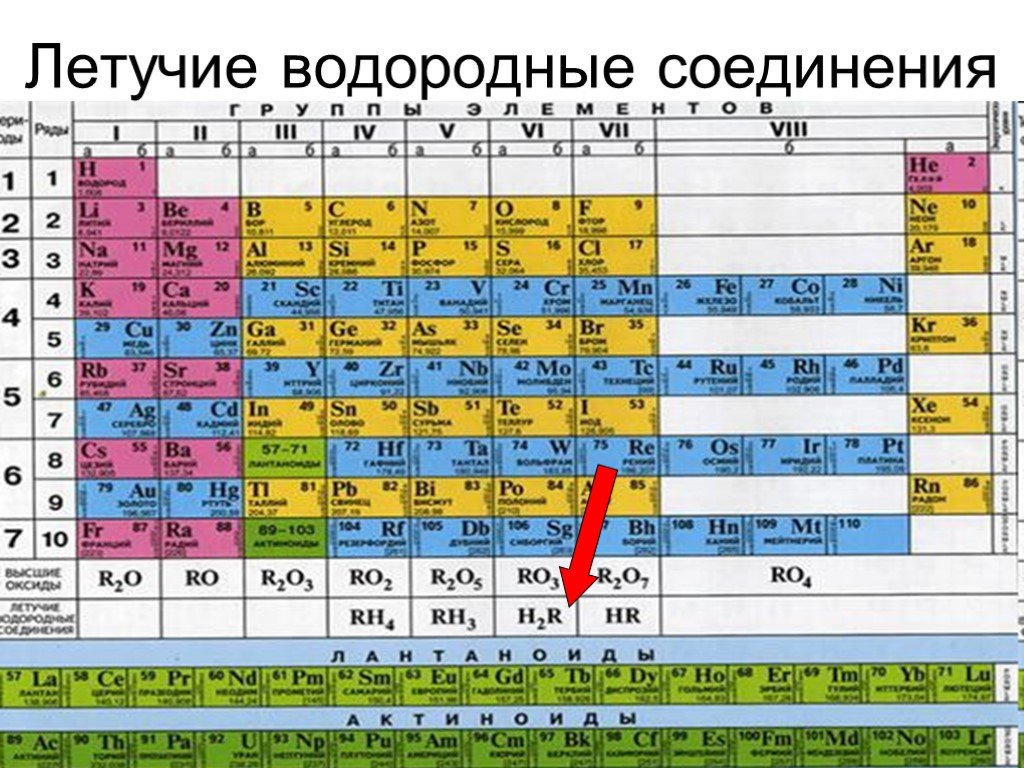
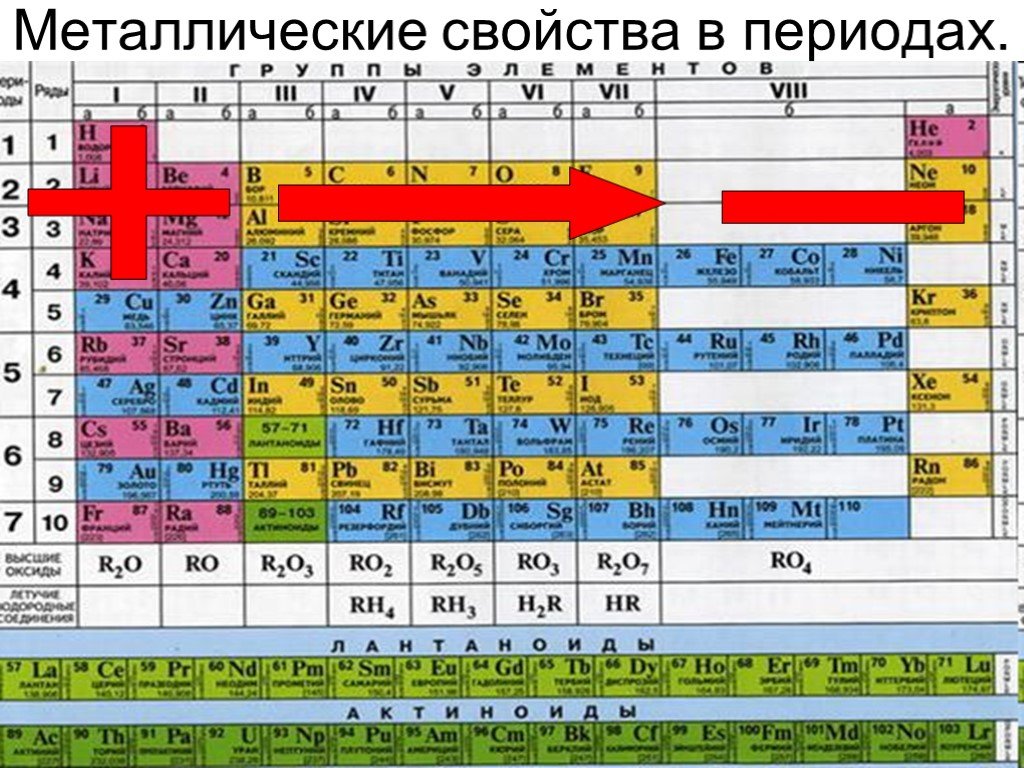
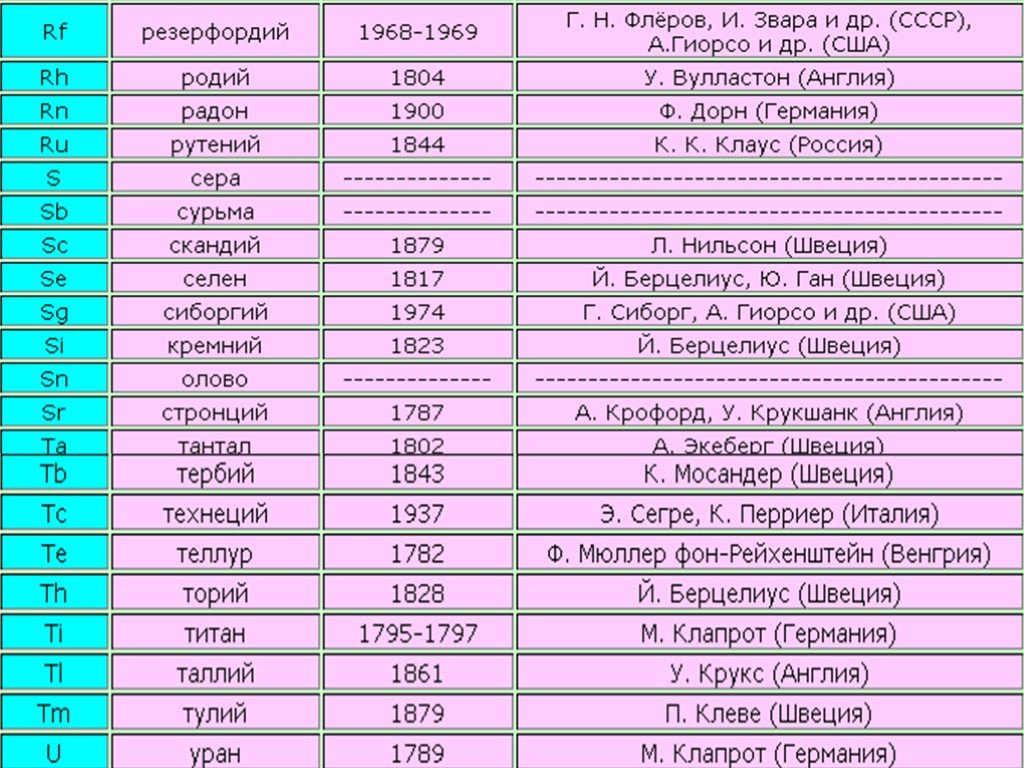
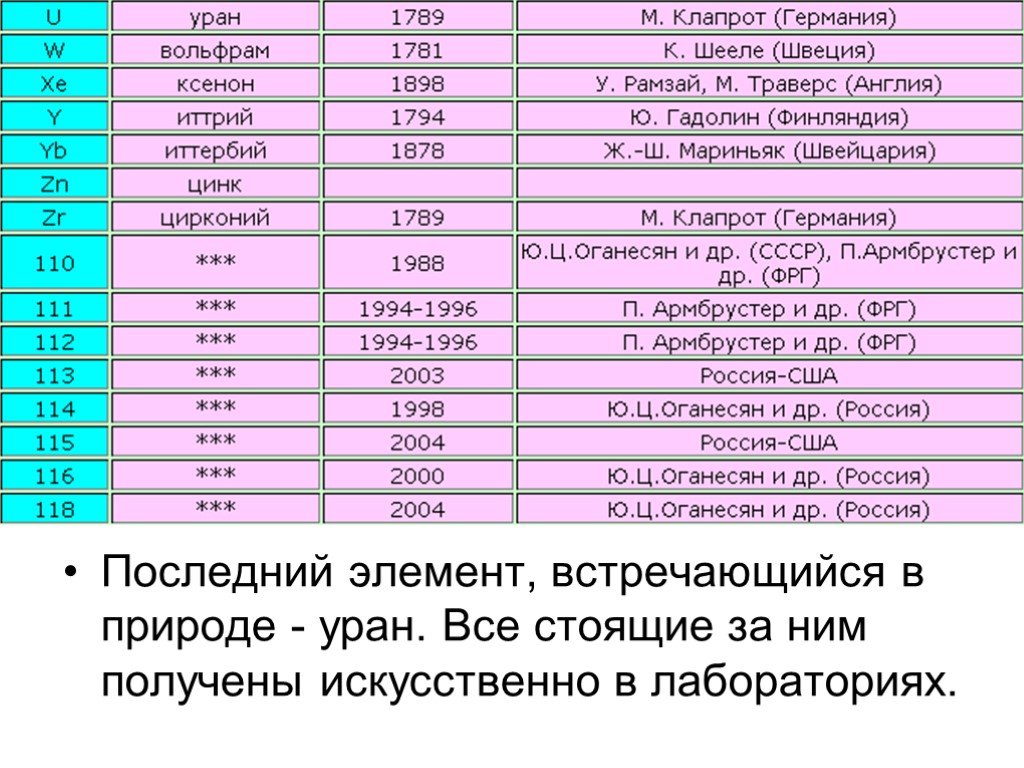
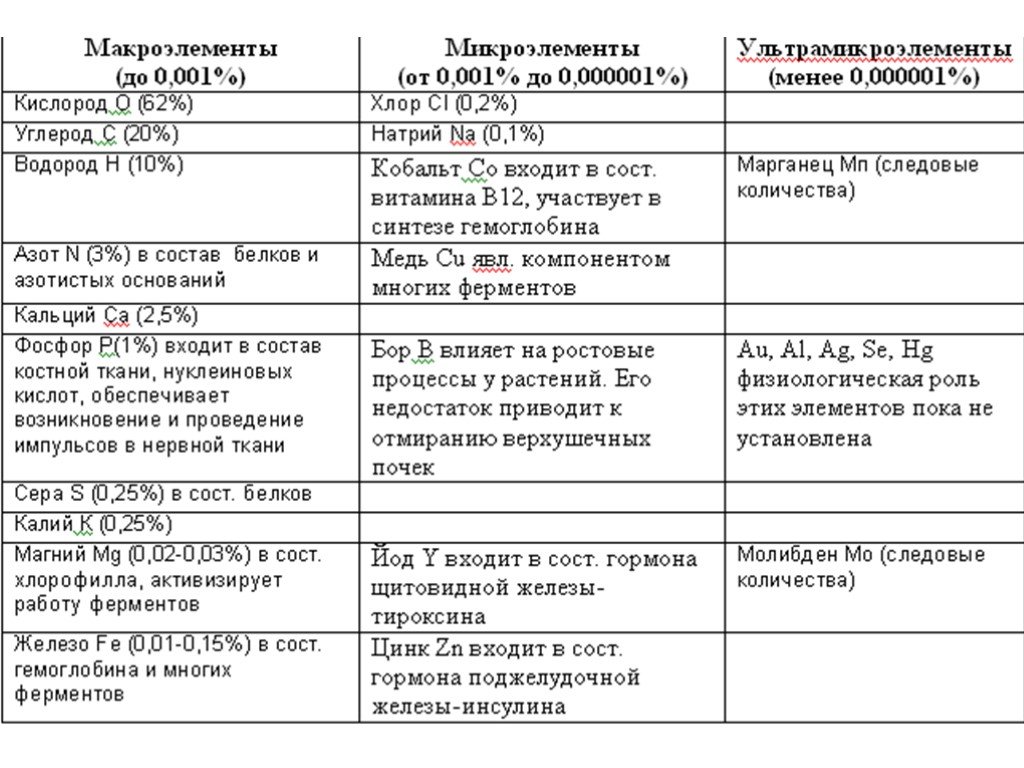
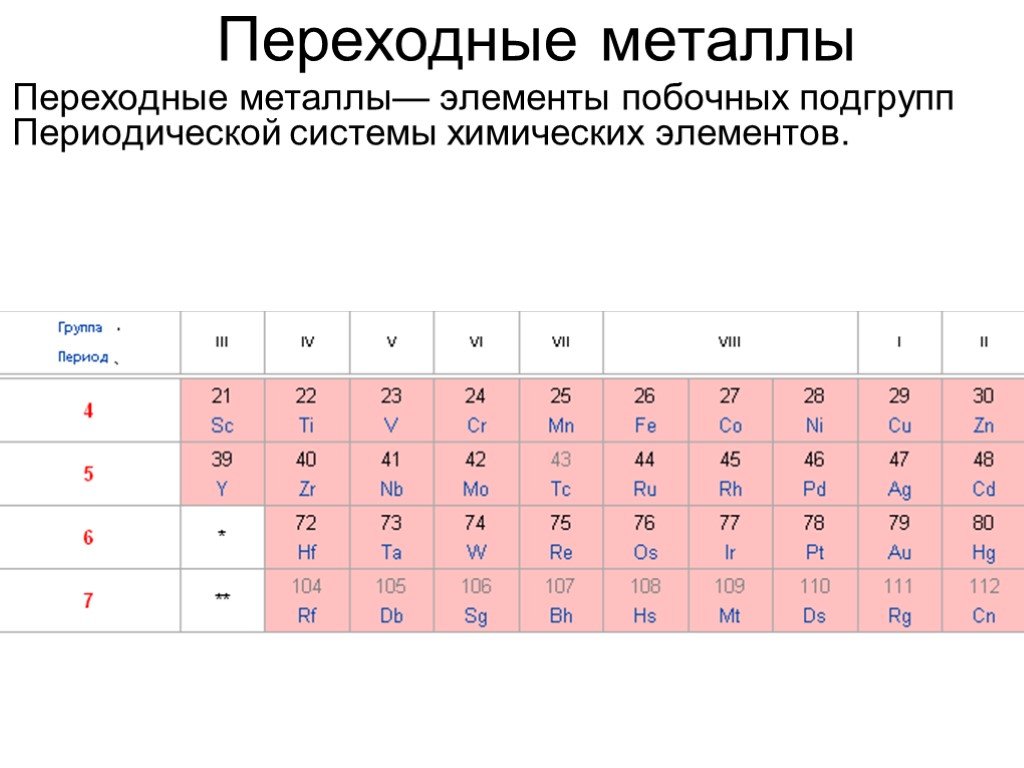
Презентация "Структура ячейки на примере атома железа" по химии – проект, доклад
Презентацию на тему "Структура ячейки на примере атома железа" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 30 слайд(ов).
Слайды презентации
Список похожих презентаций
Дружи с ионами железа ты всегда, и краски ты получишь без труда
Наша задача. Получить соединения железа, которые могут быть использованы как пигменты для красок цветного фото. Получаем краски. К растворам FeSO4 ...Влияние железа на организм
Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности, оно – орудие войны и мирного ...Всё на свете химия!
А что же такое химия? Наука о веществах и превращениях друг в друга. Химия в быту. Химия в быту, сравнительно молодая наука, является нашим незаменимым ...Вплив радіонуклідів на живі організми
іонізує молекули; руйнує клітинні мембрани; уражає клітини кісткового мозку; призводить до генетичних ушкоджень; порушує імунну систему; викликає ...Вода – важнейшая составляющая жизни на Земле
Введение:. Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и ...Использование ИКТ на уроках химии
В своей педагогической деятельности использую технологию развивающего обучения, направленную на обеспечение личности гимназиста. При данной технологии ...ИКТ на уроках
Компьютерные технологии на уроках химии дают возможность:. индивидуализировать и дифференцировать процесс обучения за счет возможности изучения с ...Игровые моменты на уроках химии
Обобщать и закреплять знания. Развивать умения и навыки. Вызвать стремление познавать и объяснять. Создать ситуацию успеха для ученика. Вызвать положительные ...Будова атома
Дмитро Іванович Менделєєв. Пригадайте: Яку дату вважають “Днем народження” періодичного закону? Що було взято вченим за основу при створенні періодичного ...Благородные металлы на службе у человека
Цель урока:. Рассмотреть и сравнить с разных точек зрения Химии и экологии; Литературы и философии; Географии и истории Самые популярные металлы окружающие ...Безопасность на уроке химии
Пробовать вещества на вкус, есть и пить в химическом кабинете. Осторожно направляйте к себе газ рукой. ЗАПРЕЩАЕТСЯ. . . . . ЗАПРЕЩАЮЩИЕ ЗНАКИ. Запрещается ...Атомы химических элементов. Структура Периодической системы
Цель урока:. Цель урока: Обобщение знаний о строении атома, изотопах, формирование понятия «химический элемент», закрепление знаний о структуре Периодической ...Активизация обучающихся на уроках химии как показатель развития их мыслительной деятельности.
Приёмы активизации мыслительной деятельности обучающихся:. Приём стимулирующих звеньев Приём реконструкции Приём прогнозирования. Приём стимулирующих ...«Радіоактивний розпад хімічних елементів. Вплив радіації на живі організми».
«Радіоактивний розпад хімічних елементів. Вплив радіації на живі організми». Тема уроку:. “Ворога необхідно знати в обличчя. Знати – значить перемогти!” ...«Вода – основа жизни на Земле».
Вода – основа жизни на Земле. Цель: используя учебный материал курсов химии, биологии, физики, географии, экологии, обобщить знания о воде, подвести ...Задачи на смеси и сплавы
Цель. Расширить представления о процентных вычислениях при решении задач на смеси, сплавы, растворы Показать широту применения процентных расчетов ...Валентные состояния атома углерода
Первое валентное состояние атома углерода (на примере молекулы метана). СН4 Н Н С Н Н. Два «противоречия» в строении метана:. Валентность углерода ...Изучение отдельных тем базового содержания курса химии в 8 классе, на основе технологии полного усвоения
Проблема. Усвоение всеми учащимися базового содержания образования через обучение в соответствии с индивидуальными особенностями восприятия и усвоения. ...Влияет - ли рН воды на рост бобовых
Актуальность выбора темы: Для роста растений необходимы определенные условия. Им нужен грунт, свет, вода и воздух. С помощью нашей работы мы хотели ...Конспекты
Железо. Положение железа в периодической системе и строение его атома. Нахождение в природе. Физические и химические свойства железа
Дата_____________ Класс_______________. Тема:. Железо. Положение железа в периодической системе и строение его атома. Нахождение в природе. Физические ...Развитие интеллекта и творческих способностей учащихся на уроках химии
Перед современной школой стоит задача воспитания грамотного, продуктивно мыслящего человека, адаптированного к условиям жизни в обществе. Проблема ...Причины и последствия токсичного воздействия этанола на организм
МОУ «Средняя общеобразовательная школа №7». г.Нижнекамск, Республика Татарстан. Причины и последствия. . токсичного воздействия ...Основные сведения о строении атома
лицей № 9. имени заслуженного учителя школы Российской Федерации А.Н.Неверова Дзержинского района г. Волгограда. Конспект ...Основные сведения о строении атома
Унковская Светлана Андреевна. МБОУ СОШ №18 г.Ставрополь. учитель химии. Тема урока: «Основные сведения о строении атома». Цель урока. ...Нефтехимическая промышленность Республики Татарстан и ее влияние на окружающую среду
Тема:. «Нефтехимическая промышленность Республики Татарстан и ее влияние на окружающую среду». Цель:. . Познавательна. я – углубить знания о составе, ...Решение экспериментальных задач на распознавание катионов и анионов
Название работы:. Урок-практикум в 8-м классе на тему «Решение экспериментальных задач на распознавание катионов и анионов». Тема урока. Урок-практикум ...Решение задач на определение молекулярной формулы вещества
Муниципальное бюджетное общеобразовательное учреждение. «Средняя общеобразовательная школа №17» г. Брянска. Урок на тему: «Решение задач ...Восхождение на пик знаний
МОУ «Основная общеобразовательная школа с. Калмантай Вольского района Саратовской области». Тема. урока:. . «Восхождение на ...Воздух. Горение веществ на воздухе
. Урок по теме:. . «Воздух. Горение веществ на воздухе». . . . Учитель химии МКОУ СОШ № 7. с. Величаевского Левокумского района ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:24 февраля 2019
Категория:Химия
Содержит:30 слайд(ов)
Поделись с друзьями:
Скачать презентацию