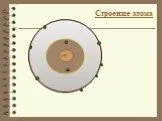
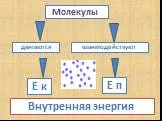
Презентация "Атомы химических элементов. Структура Периодической системы" по химии – проект, доклад
Презентацию на тему "Атомы химических элементов. Структура Периодической системы" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 20 слайд(ов).
Слайды презентации
Список похожих презентаций
Элемент периодической системы химических элементов Д.И.Менделеева -АЛЮМИНИЙ
Около 100 лет назад Николай Гаврилович Чернышевский, сказал об алюминии, что этому металлу суждено великое будущее, что алюминий – металл социализма. ...Путешествие по Периодической системе химических элементов
Загадки Ребусы Шарады. Он и легок и пластичен, С блеском серебристым, Но снаружи никогда не бывает чистым. Мы найдем его на кухне, И на стройке, и ...Характеристика химических элементов и их соединений на основе положения элементов в периодической системе.
Цель урока? Химический элемент. Семейство Щелочные Ме Халькогены Период Группы Изотопы Валентность Д.И.Менделеев. Горячий стул. Химический диктант ...Атомы химических элементов
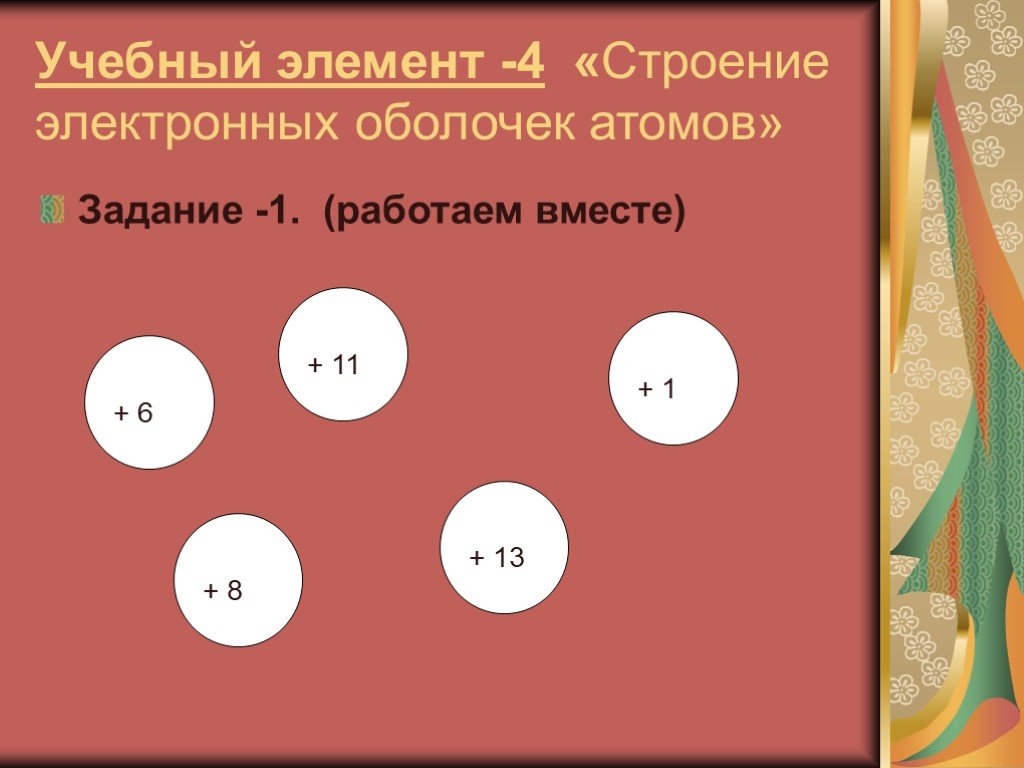
Задание 1: найдите в каждом ряду один химический элемент, который отличается от остальных по положению в периодической системе химических элементов ...Периодическая система химических элементов Д.И. Менделеева и строение атома
Цель:. Повторить основные теоретические вопросы программы 8 класса; Закрепить знания о причинах изменения свойств химических элементов на основании ..."Знаки химических элементов. Периодическая таблица
скисание молока, испарение воды, образование ржавчины, горение древесины, гашение соды уксусом, горение свечи, таянье льда, кипение воды, подгорание ...Биогенная классификация химических элементов
бром железо натрий. Элементы необходимые организму для построения и жизнедеятельности клеток и органов, называют биогенными элементами. Введение в ...Периодическая система химических элементов Д.И. Менделеева
МЕНДЕЛЕЕВ Дмитрий Иванович (1834-1907). выдающийся русский деятель науки и культуры, автор фундаментальных исследований по химии, химической технологии, ...Периодическая система химических элементов Д.И. Менделеева
Цель. Сформировать представление о строении периодической системы Рассмотреть закономерности свойств химических элементов. Меню. Содержание. Историческая ...Валентность химических элементов
Валентность некоторых химических элементов в химических соединениях. С постоянной валентностью. C переменной валентностью. Определение валентности ...Периодическая система химических элементов в почтовых марках.
Границ научному познанию и предсказанию предвидеть невозможно. Д.И.Менделеев. Сюжетные изображения на почтовых марках отражают:. Свойства простых ..."Соединения химических элементов"
Цель урока. обобщить и систематизировать знания по теме «Соединения химических элементов», подготовиться к контрольной работе. Конкурс 1 «Найди родственников». ...Соединения химических элементов. Степень окисления
Бинарные соединения – сложные вещества, состоящие из двух химических элементов. NaCl Хлорид натрия Na0+Cl0=Na+Cl‾ Связь ионная +11Na )2)8)1 Атом натрия ...Периодическая система химических элементов
1. В главных подгруппах периодической системы химических элементов с увеличением заряда ядер не изменяется. Радиус атома; Число электронов на внешнем ...Круговорот химических элементов в природе
Цель и задачи проекта. Цель: Задачи:. Рассмотреть круговороты веществ и взаимодействие их между собой. 1) Изучить литературу по данной теме. 2) Изучить ...Соединения химических элементов
Конфуций сказал:. «Учиться, а время от времени повторять изученное, разве неприятно?». Задание 1.Выписать оксиды и распределить их в два столбика: ...Классификация химических элементов
Цели урока:. Ознакомление с понятием классификация и её первыми попытками по отношению к химическим элементам; Развитие умения сравнивать химические ...Периодическая таблица химических элементов
Тема урока: Классификация химических элементов. Начало классификации. К 70-м годам прошлого века было уже известно более 60 химических элементов. ...Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома
ДЕВИЗ УРОКА:. Чтобы стать настоящим химиком, надо знать, уметь, думать!". ЭПИГРАФ УРОКА:. «… Другого ничего в природе нет, Ни здесь, ни там, в космических ...Конспекты
Современная формулировка периодического закона и современное состояние периодической системы химических элементов Д. И. Менделеева
Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Тема. . Современная формулировка периодического закона и современное ...Положение неметаллов в периодической системе химических элементов Д.И. Менделеева, строение их атомов, физические свойства. Аллотропия
Тема:Положение неметаллов в периодической системе химических элементов Д.И. Менделеева, строение их атомов, физические свойства. Аллотропия. Цели ...Атомы химических элементов
Зачет по теме «Атомы химических элементов». Дайте определение:. . Уровень 1 (оценка «3»). – необходимо ответить на любые 5 вопросов. Уровень ...Положение азота и фосфора в периодической системе химических элементов, строение их атомов. Азот, физические и химические свойства, получение и применение
Дата_____________ Класс_______________. Тема:. . Положение азота и фосфора в периодической системе химических элементов, строение их атомов. Азот, ...Положение кислорода и серы в периодической системе химических элементов, строение их атомов. Озон-аллотропная модификация кислорода
Технологическая карта урока. . . Учитель Дьячук Е.Ю. учитель химии МБОУ СОШ №1 г.Оха Сахалинская область. Предмет. химия. . Класс. . ...Положение кислорода и серы в периодической системе химических элементов, строение их атомов. Озон – аллотропная модификация кислорода
Дата _____________ Класс ___________________. Тема: Положение кислорода и серы в периодической системе химических элементов, строение их атомов. ...Положение металлов в периодической системе химических элементов Д. И. Менделеева. Металлическая связь
Дата_____________ Класс_______________. Тема:. . Положение металлов в периодической системе химических элементов Д. И. Менделеева. Металлическая ...Введение. Атомы химических элементов
МОУ ИРМО «Никольская СОШ». 8 класс. Учитель:. . Г.М. Донская. 2014 – 2015 учебный год. . Урок – обобщение по темам. ...Характеристика элемента по его положению в периодической системе химических элементов Д.И. Менделеева
1001 идея интересного занятия с детьми. . ПРИМЕНЕНИЕ ТЕХНОЛОГИЙ КРИТИЧЕСКОГО МЫШЛЕНИЯ НА УРОКАХ ХИМИИИ. Бурдакова Кристина Олеговна, МБОУ СОШ ...Металлы главных подгрупп периодической системы элементов Д.И.Менделеева
Модуль 1. Тема: «Металлы главных подгрупп периодической системы элементов Д.И.Менделеева». номер. учебного. элемента. (УЭ). Учебный материал ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:12 июня 2018
Категория:Химия
Содержит:20 слайд(ов)
Поделись с друзьями:
Скачать презентацию