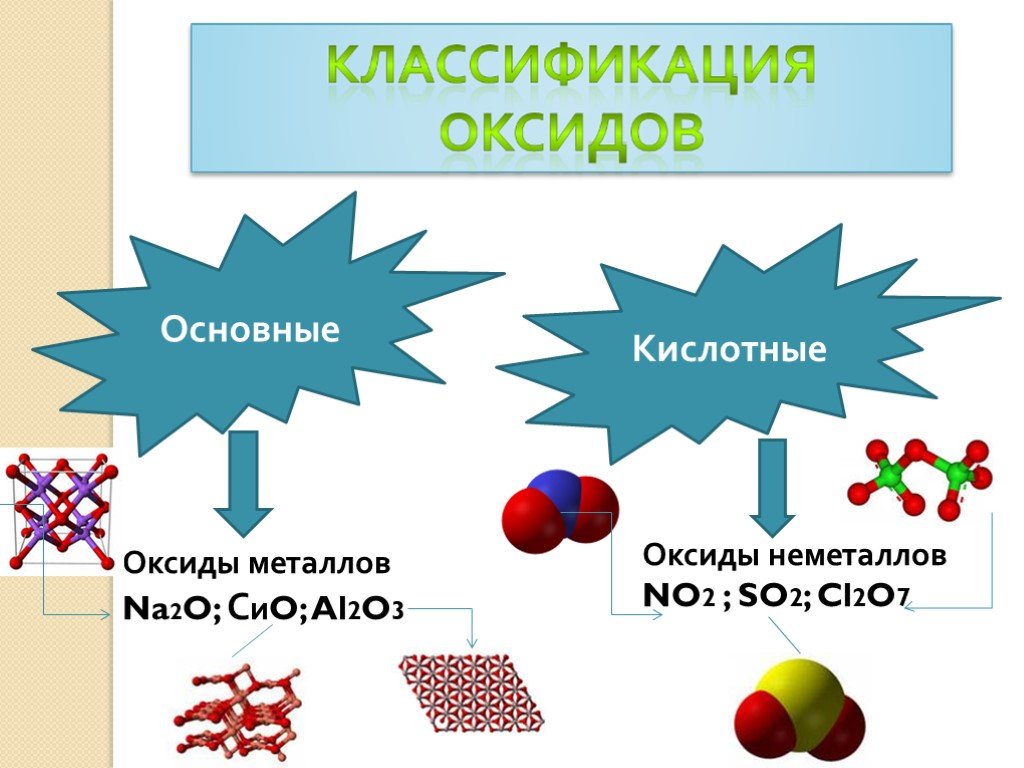
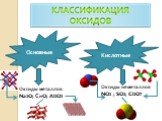
Презентация "Химические оксиды" по химии – проект, доклад
Презентацию на тему "Химические оксиды" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 12 слайд(ов).
Слайды презентации
Список похожих презентаций
Химические свойства воды
1) Вода реагирует со многими металлами с выделением водорода:. 2Na + 2H2O = H2 + 2NaOH (бурно) 2K + 2H2O = H2 + 2KOH (бурно) 3Fe + 4H2O = 4H2 + Fe3O4 ...Химические свойства и применение алканов
Цель урока. Образовательная: изучение химических свойств алканов, опираясь на их строение. Развивающая: продолжить формирование умения составлять ...Химические элементы в организме человек
Введение. Многие учёные считают, что в живом организме не только присутствуют все химические элементы, но каждый из них выполняет определённую биологическую ...Алкены. Строение. Изомерия. Химические свойства
Элементный анализ этилена показывает, что в его состав входят примерно 87,5% углерода и 14,3% водорода. Плотность этилена по отношению к водороду ...Химические свойства солей
Кто хочет съесть ядро ореха, должен расколоть его скорлупу плавт. Вычеркните «лишние» формулы и допишите предложения. А) H2SO4 , HNO3, H3PO4, HCl, ...Химические уравнения. Реакции обмена
24.05.2019 Лебедева Л.В.Повторим изученный материал.
Какое слово зашифровано в таблице?
2Na+2HCl=2NaCl +H2↑ 2Al + 3S = Al2S3 Al(OH)3 = Al2O3 + ...
Интерактивная игра "Химия в ребусах: Химические элементы"
НИКЕЛЬ. ИОД. АЗОТ. БОР. МАГНИЙ Й. МАРГАНЕЦ. КРЕМНИЙ Л=й. МЫШЬЯК. УГЛЕРОД О. ЦИРКОНИЙ. АРГОН. МЕДЬ ДВЕ. КРИПТОН. ЗОЛОТО. СЕРА П=А. ВОДОРОД А=О Т=Д. ...Химические свойства многоатомных спиртов
ХИМИЧЕСКИЕ СВОЙСТВА ГЛИКОЛЕЙ АНАЛОГИЧНЫ СВОЙСТВАМ ОДНОАТОМНЫХ СПИРТОВ. ОДНАКО У ГЛИКОЛЕЙ МОГУТ ВСТУПАТЬ В РЕАКЦИИ КАК ОДНА, ТАК И ОБЕ ГИДРОКСИЛЬНЫЕ ...Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения
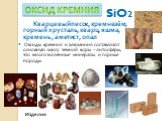
SiO2 , H2O , CO2 , AI2O3 , Fe2O3 , CO. Всесильная стихия природы-вода во все времена, во все периоды истории покоряла ум и воображение людей. Человек ...Важнейшие представители бинарных соединений – оксиды и летучие водородные соединения
Н2О - вода. СО2 углекислый газ. СУХОЙ ЛЁД. NH3 аммиак. HCL хлороводород. Бесцветный газ. Тяжелее воздуха. Хорошо растворяется в воде. Раствор хлороводорода ...Бинарные соединения: оксиды, гидриды
Цели урока. Познакомиться с понятием оксиды и гидриды; Закрепить навыки составления формул по С.О. и определение С.О. по формуле; Произвести расчёты ...Амфотерные оксиды и гидроксиды
Дать понятие об амфотерности, амфотерных оксидах и гидроксидах, переходных металлах; Повторить, закрепить и развить знания о классификации и свойствах ...Алкены. Строение. Изомерия. Химические свойства. Получение
Элементный анализ этилена показывает, что в его состав входят примерно 87,5% углерода и 14,3% водорода. Плотность этилена по отношению к водороду ...Химические свойства кислот
Кислоты. Тема урока: «Химические свойства кислот в свете теории электролитической диссоциации». «От кислых яблок сразу скисну». В. Шекспир. Задачи ...Кислотные оксиды
№ 3 стр. 99. CaCl2 MgCO3 Zn(NO3)2 Al2(SO4)3 K2CO3 Na2SO4 Na2SiO3 AgCl MgSO3 Al2S3. H O S. Образование солей. Zn. Номенклатура солей. + =. Составить ...Химические свойства металлов
Цель урока:. обобщить знание учащихся, полученные ранее при рассмотрении общих химических свойств металлов; повторить особенности протекания реакций ...Металлы. Химические и физические свойства металлов
Физические свойства металлов. Очень важным свойством металлов является их сравнительно легкая механическая деформируемость. Металлы пластичны, они ...Химические свойства оснований
2.Вещество, которое в водном растворе не диссоциирует на ионы: H 2SO4 2) Mg(OH)2 3) FeCl3 4) NaOH. 3.К растворам веществ, формулы которых приведены ...Обобщение темы: «Кислоты, основания, оксиды и соли, их классификация и свойства»
Вопрос №1. Сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид – ионов, называются: 1) кислоты 2) основания 3) оксиды 4) соли ...Химические синонимы
Химическая реакция. Химическое явление. химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции. катализатор фермент. эндотермический ...Конспекты
Химические свойства солей
. Зайчикова Ирина Николаевна. МБОУ «Пригородная СОШ». Учитель химии, биологии. Разработка урока по химии в 8 классе «Химические свойства ...Химические свойства оснований
Автор:. Голикова Ирина Викторовна, учитель химии, МБОУ «Сергеевская СОШ». Класс:. 8в. Раздел программы:. «Классы неорганических веществ». Тема ...Химические свойства серной кислоты
. Химические свойства серной кислоты. Данный урок- презентация по теме « Химические свойства серной кислоты» позволяет реализовать ...Химические свойства металлов
Губарева Вера Александровна, г.Нижнекамск РТ. . Муниципальное общеобразовательное учреждение. «Средняя общеобразовательная школа №7». Г.Нижнекамск, ...Химические свойства неметаллов и их соединений. Кислотные дожди
Разработка урока «Химические свойства неметаллов и их. . соединений. Кислотные дожди» 9 класс. . учителя химии МБОУ ССОШ №13 Зимовниковского ...Химические свойства кислот
Конспект урока по химии в 8 классе. Кузнецова Светлана Леонтьевна. ,. . учитель химии. . высшей категории. МАОУ СОШ «Земля родная». г.Новый ...Химические свойства металлов
Аннотация. Тема урока: Химические свойства металлов. Разработчик: Саляхова Гульгена Габдулловна – учитель биологии. Данный план-конспект урока ...Кислоты. Классификация. Химические свойства с точки зрения электролитической диссоциации
8 класс. . . Урок-игра «Химическое лукошко» по теме «Урок-упражнение по теме «Кислоты. Классификация. Химические свойства с точки зрения электролитической ...Кислоты. Химические свойства кислот в свете теории электролитической диссоциации
Урок химии в 8-м классе по теме: "Кислоты. Химические свойства кислот в свете теории электролитической диссоциации.". . Цели урока:. Образовательная. ...Важнейшие классы бинарных соединений – оксиды, их роль в природе и жизни человека
Урок химии в 8 классе по теме:. «Важнейшие классы бинарных соединений – оксиды, их роль в природе и жизни человека». Цели урока:. Предметные. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:3 марта 2019
Категория:Химия
Содержит:12 слайд(ов)
Поделись с друзьями:
Скачать презентацию