Презентация "Производство серной кислоты (польза и вред)" по химии – проект, доклад
Презентацию на тему "Производство серной кислоты (польза и вред)" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 20 слайд(ов).
Слайды презентации
Список похожих презентаций
Производство серной кислоты
Сырьё. FeS2 - пирит, серный колчедан, железный колчедан S8 самородная ромбическая сера H2S – сероводород Сu2S; ZnS; PbS – сульфиды цветных металлов ...Производство серной кислоты
Сернокислотные заводы. Пирит обыкновенный. Черный пирит. Самородная сера. Сероводород. Сульфиды цветных металлов. Подготовка сырья. Измельчение пирита. ...Производство серной кислоты
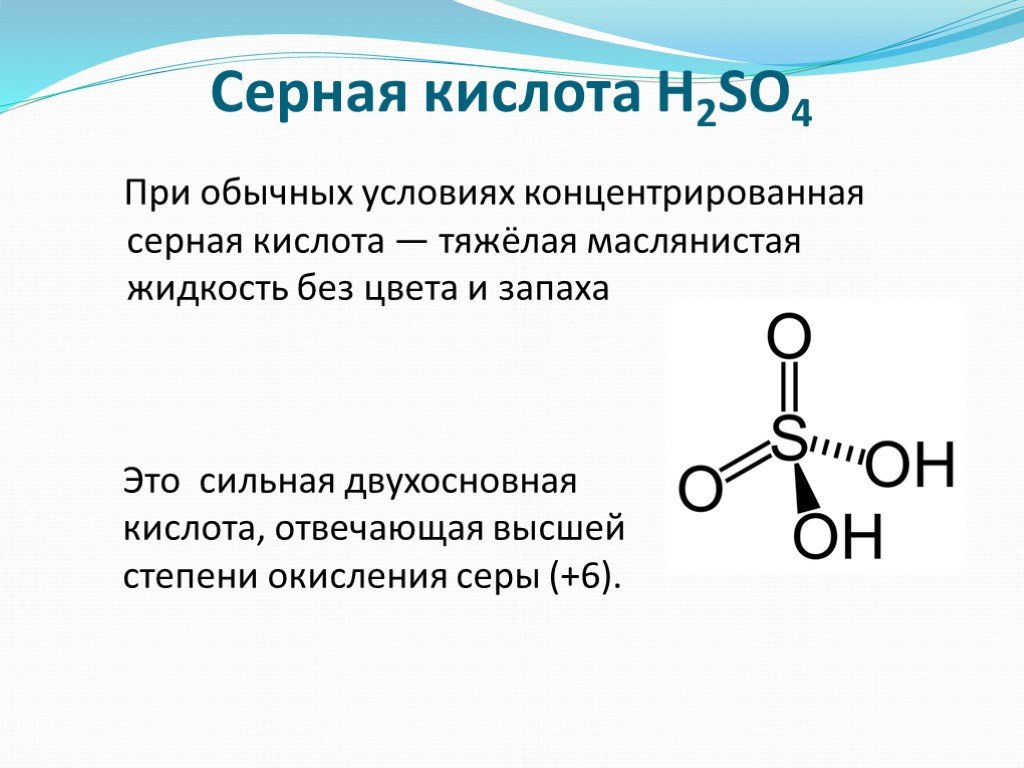
Серная кислота. H2SO4 cуществует в природе как самостоятельное химическое соединение, представляет собой бесцветную маслянистую жидкость без запаха ...Производство серной кислоты
Цель: обобщить сведения о стадиях и принципах, используемых при промышленном производстве серной кислоты. Рифмованные строчки. Для закрепления сейчас ...Производство серной кислоты контактным способом
Сырьё, используемое для производства серной кислоты:. 1. Самородная сера S 2. Пирит (серный колчедан) FeS2 3.Сероводород H2S 4. Сульфиды цветных металлов ...Производство серной кислоты контактным способом.
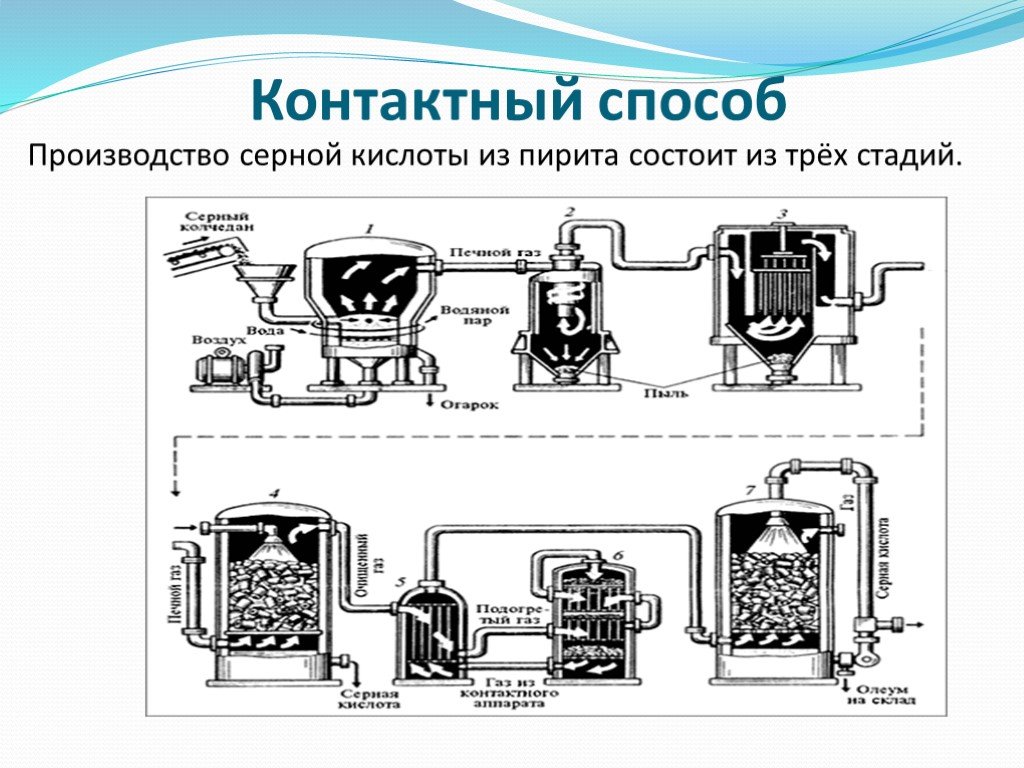
газ. Сжигание серного колчедана, при этом образуются печной газ SO2 и огарок Fe2O3 : 4FeS2 +11O2→2Fe2O3+8SO2. Печь для обжига в кипящем слое. Циклон ...Производство серной кислоты
Исторические сведения. Серная кислота известна с древности. Первое упоминание о кислых газах, получаемых при прокаливании квасцов или железного купороса ...Жевательная резинка: польза или вред?
Актуальность исследования заключается в том, что множество людей, большинство из которых дети, употребляют жевательную резинку. Цель работы: изучение ...Пить или не пить? Вред энергетических напитков. Или польза
В каких ситуациях незаменимы энергетические напитки? Что содержится в энергетических напитках, и какой вред может быть причинён организму энергетическими ...Чипсы - вред или польза?
Цель:. С помощью химического анализа и теоретического исследования соизмерить степень полезных и вредных компонентов в составе чипсов, определить ...Полимеры: польза или вред?
Полимеры - это вещества, молекулы которых состоят из большого числа повторяющихся группировок, или мономерных звеньев, соединенных между собой химическими ...Спирты. Польза и вред
Метанол. Метанол втягивает воду, что является причиной засорения систем подачи топлива в виде желеобразных ядовитых отложений. Метанол, как и этанол, ...Химические свойства серной кислоты
Ход урока:. Повторение предыдущей темы: 1. Что такое кислота с точки зрения ЭД. 2. Формула серной кислоты, валентность атома серы и степень окисления. ...Воздействие серной кислоты на углеводы
Углеводы. Углеводы – органические вещества, молекулы которых состоят из атомов углерода, водорода и кислорода, причем водород и кислород находятся ...Нитрозный способ получения серной кислоты
Реагенты. Медь Азотная кислота Сульфит натрия Раствор серной кислоты 70%. Приборы. Две колбы Вюрца Трехгорлая колба 2 газоотводных шланга Штативы ...Спирты. Польза и вред
Метанол втягивает воду, что является причиной засорения систем подачи топлива в виде желеобразных ядовитых отложений.Метанол, как и этанол, повышает ...Серная кислота, свойства серной кислоты
Состав. Кислоты - это сложные вещества, в молекулах которых содержат атомы водорода и кислотный остаток H-R, где R-кислотный остаток При электролитической ...Мыло: польза или вред?
Гипотеза: мыло не всегда полезно…. Цель работы: выяснить - полезно ли мыло на самом деле? Содержание: Раздел 1. Производство мыла. а) В старину. б) ...Производство биоэтанола
Растущий рынок биоэтанола. Биоэтанол: потенциал использования. В настоящее время во всем мире растёт интерес к различным видам жидкого биотоплива, ...Производство аммиака
Цели работы:. Изучить процесс производства аммиака Изучить условия протекания реакции Изучить пользу и вред производства. Аммиак — NH3, нитрид водорода, ...Конспекты
Производство серной кислоты
Производство серной кислоты. . Сырьё для получения:. самородная ромбическая сера, пирит (серный колчедан, железный колчедан), сульфиды цветных ...Производство серной кислоты контактным способом
Салищева О. льга Георгиевна. . Федеральное государственное казенное общеобразовательное учреждение «СОШ №3» г. Приозерск. . учитель химии. ...Окислительные свойства концентрированной серной кислоты
Дата_____________ Класс_______________. Тема: Окислительные свойства концентрированной серной кислоты. Цели урока:. ознакомиться с окислительными ...Химические свойства серной кислоты
Урок химии, 9 класс, 45 мин. разработан учителем химии МОУ «Рамешковская СОШ» Габлиной В.И. Тема: Химические свойства серной кислоты. Цели: Сформировать ...Химические свойства серной кислоты
. Химические свойства серной кислоты. Данный урок- презентация по теме « Химические свойства серной кислоты» позволяет реализовать ...Свойства серной кислоты
Свойства серной кислоты. Девиз: "Наши знания суть зерна наших творений". . . Г. Бюффон. Цели. : повторить строение молекулы серной кислоты, ...Приключения серной кислоты
Урок - сказка «Приключение Серной Кислоты». (9 класс). Цели урока: Закрепить и проверить знания учащихся по теме «Подгруппа кислорода», сравнить ...Производство азотной кислоты
ПЛАН-КОНСПЕКТ УРОКА. «Производство азотной кислоты. ». . 1. ФИО:. Семёнычева Лариса Витальевна. 2. Место работы:. МОУ СОШ №12. 3. Должность:. ...Окислительные свойства серной кислоты
Конспект урока. Данные об учителе: Загребина Анастасия Павловна. учитель МБОУ Июльской СОШ, 1 категория, запрашиваемая 1 категория. Предмет. : химия. ...Польза и вред витамином в пище человека
Муниципальное автономное образовательное учреждение «Средняя общеобразовательная школа №107» г. Перми. Технологическая характеристика урока по ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:2 декабря 2018
Категория:Химия
Содержит:20 слайд(ов)
Поделись с друзьями:
Скачать презентацию