Презентация "Производство аммиака" по химии – проект, доклад
Презентацию на тему "Производство аммиака" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 17 слайд(ов).
Слайды презентации
Список похожих презентаций
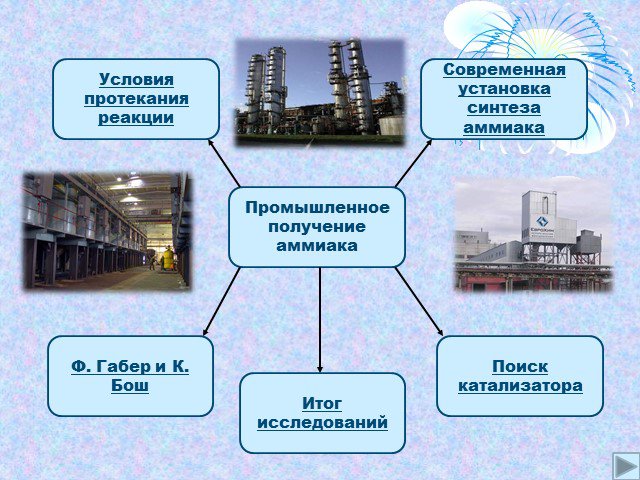
Производство аммиака
Изучить научные принципы производства аммиака. Цель. Задачи. Разработать оптимальные условия синтеза аммиака. Составить технологическую схему производства. ...Производство стекла
Основным сырьем для производства стекла является сода. Сода - сырье относительно дорогое и имеющее огромный спрос со стороны различных отраслей народного ...Производство стекла
Уже на ранней стадии изготовления стекла люди использовали приемы, которые, являются зачатками сегодняшней технологии. Это установлено в результате ...Производство серной кислоты контактным способом.
газ. Сжигание серного колчедана, при этом образуются печной газ SO2 и огарок Fe2O3 : 4FeS2 +11O2→2Fe2O3+8SO2. Печь для обжига в кипящем слое. Циклон ...Производство серной кислоты контактным способом
Сырьё, используемое для производства серной кислоты:. 1. Самородная сера S 2. Пирит (серный колчедан) FeS2 3.Сероводород H2S 4. Сульфиды цветных металлов ...Производство серной кислоты (польза и вред)
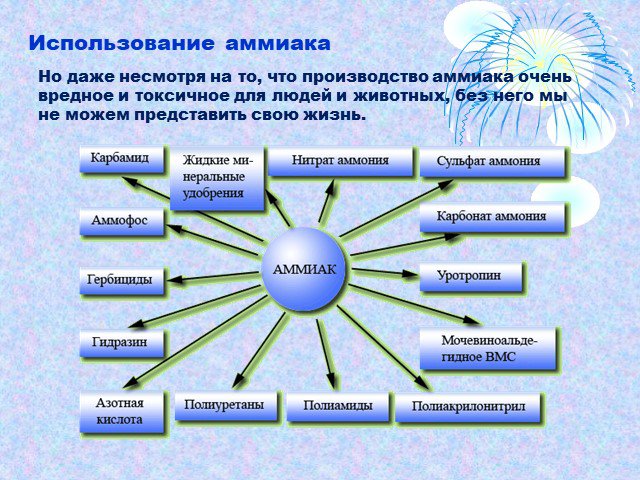
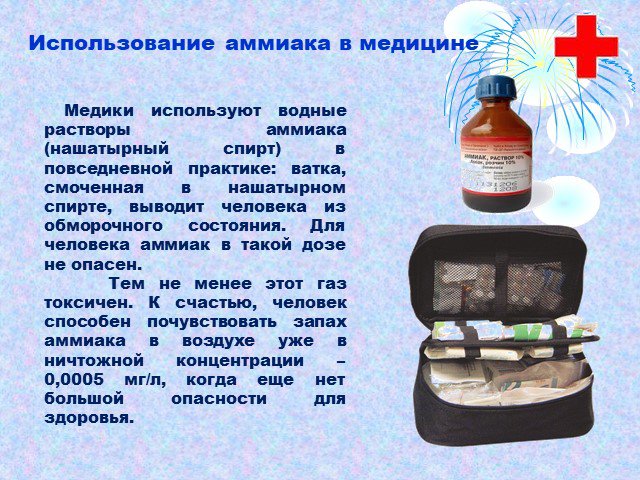
Цель работы:. Узнать: из чего получают серную кислоту; как получают серную кислоту; для чего получают серную кислоту; вредно ли производство серной ...Применение аммиака
Использование в сельском хозяйстве. Использование. Мировое производство аммиака составило в 1980 году более 90 млн. тонн. До образования Украины на ...Строение молекулы аммиака
Строение молекулы аммиака. Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине; Атом азота образует с тремя атомами водорода ...Производство серной кислоты
Сырьё. FeS2 - пирит, серный колчедан, железный колчедан S8 самородная ромбическая сера H2S – сероводород Сu2S; ZnS; PbS – сульфиды цветных металлов ...Производство серной кислоты
Сернокислотные заводы. Пирит обыкновенный. Черный пирит. Самородная сера. Сероводород. Сульфиды цветных металлов. Подготовка сырья. Измельчение пирита. ...Производство серной кислоты
Исторические сведения. Серная кислота известна с древности. Первое упоминание о кислых газах, получаемых при прокаливании квасцов или железного купороса ...Производство мыла
Знать – хорошо, но уметь – лучше. Гейбель ИСТОРИЯ 1. «ВОПРОСИТЕЛЬНАЯ» В этом учебном году мы начали изучать органическую химию и перед нами открылся ...Производство биоэтанола
Растущий рынок биоэтанола. Биоэтанол: потенциал использования. В настоящее время во всем мире растёт интерес к различным видам жидкого биотоплива, ...Производство алюминия
ПЛАН ИЗУЧЕНИЯ АЛЮМИНИЯ: 1. Алюминий – химический элемент 1.1. Положение в ПСХЭ; 1.2. Строение атома. 2. Алюминий – простое вещество. 2.1 Нахождение ...Производство стекла
История стекла (технологии). Долгое время первенство в открытии стеклоделия признавалось за Египтом, чему несомненным свидетельством считались глазурованные ...Производство серной кислоты
Цель: обобщить сведения о стадиях и принципах, используемых при промышленном производстве серной кислоты. Рифмованные строчки. Для закрепления сейчас ...Производство чугуна и стали
Производство чугуна. Чугун и сталь – главные сплавы железа. 24.12.2017. При просмотре слайда ответьте на вопросы: Какие руды используются в производстве ...Производство серной кислоты
Серная кислота. H2SO4 cуществует в природе как самостоятельное химическое соединение, представляет собой бесцветную маслянистую жидкость без запаха ...Химические опасные аварии с выбросом хлора и аммиака
Понятие АХОВ. Под аварийными химически опасными веществами (АХОВ) понимают химические вещества или соединения, которые при проливе или выбросе из ...Конспекты
Производство серной кислоты контактным способом
Салищева О. льга Георгиевна. . Федеральное государственное казенное общеобразовательное учреждение «СОШ №3» г. Приозерск. . учитель химии. ...Производство серной кислоты
Производство серной кислоты. . Сырьё для получения:. самородная ромбическая сера, пирит (серный колчедан, железный колчедан), сульфиды цветных ...Практическая работа №3 Получение аммиака и изучение его свойств
Дата_____________ Класс_______________. Тема:. . Практическая работа №3 Получение аммиака и изучение его свойств. Цели урока:. закрепить умения ...Производство азотной кислоты
ПЛАН-КОНСПЕКТ УРОКА. «Производство азотной кислоты. ». . 1. ФИО:. Семёнычева Лариса Витальевна. 2. Место работы:. МОУ СОШ №12. 3. Должность:. ...Аммиак. Физические и химические свойства аммиака, получение, применение
Дата_____________ Класс_______________. Тема:. . Аммиак. Физические и химические свойства аммиака, получение, применение. Цели урока:. знать ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:25 апреля 2015
Категория:Химия
Содержит:17 слайд(ов)
Поделись с друзьями:
Скачать презентацию