Презентация "Строение молекулы аммиака" по химии – проект, доклад
Презентацию на тему "Строение молекулы аммиака" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 22 слайд(ов).
Слайды презентации
Список похожих презентаций
Электронное и пространственное строение молекулы метана
Электронная формула и графическая схема атома углерода. +6 С 1s 2s 2p. Электронная формула и графическая схема атома углерода в молекуле метана. 2 ...Арены. Бензол. Строение молекулы бензола
1)Углеводороды с общей формулой СnН2n+2 2) Частица с одним свободным электроном 3) Суффикс, который используется в названиях органических веществ ...Строение молекулы бензола
Цель урока. Изучить состав и строение молекулы бензола, рассмотреть гомологический ряд аренов, выяснить физические свойства бензола. Задача №1 Анализ ...Строение газообразных, жидких и твердых тел
Содержание:. Газы Газообразное состояние. Газы. Газ (газообразное состояние) (от нидерл. gas) — агрегатное состояние вещества, характеризующееся очень ...Строение вещества
АТОМЫ И ЭЛЕМЕНТЫ. Окружающий нас мир состоит из веществ, а вещества образованы мельчайшими частицами: кристаллами, молекулами и атомами. При этом ...Строение Бензола
Бензол С6Н6 – родоначальник ароматических углеводородов. Каждый из шести атомов углерода в его молекуле находится в состоянии sp2-гибридизации и связан ...Строение атомов
План изучения. Важность познания атома. Модели строения атома. Опыт Эрнеста Резерфорда. Ядерная модель строения атома. Протонно-нейтронная модель ...Строение атома. Периодический закон Д.И.Менделеева в свете теории строения атома
Родители атома. Демокрит (460 до н. э. — 370 до н. э.). Джозеф Джон Томсон (1856–1940 г). Эрнест Резерфорд (1871–1937г). Джеймс Чедвик (1891–1974г). ...Химические опасные аварии с выбросом хлора и аммиака
Понятие АХОВ. Под аварийными химически опасными веществами (АХОВ) понимают химические вещества или соединения, которые при проливе или выбросе из ...Производство аммиака
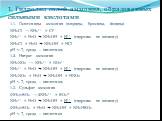
Цели работы:. Изучить процесс производства аммиака Изучить условия протекания реакции Изучить пользу и вред производства. Аммиак — NH3, нитрид водорода, ...Применение аммиака
Использование в сельском хозяйстве. Использование. Мировое производство аммиака составило в 1980 году более 90 млн. тонн. До образования Украины на ...Подготовка к ЕГЭ "Строение атома"
Число электронов во внешнем электронном слое атома, ядро которого содержит 8 протонов, равно. 1) 8 2) 2 3) 6 4) 4. Число электронов в ионе железа ...Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома
ДЕВИЗ УРОКА:. Чтобы стать настоящим химиком, надо знать, уметь, думать!". ЭПИГРАФ УРОКА:. «… Другого ничего в природе нет, Ни здесь, ни там, в космических ...Органические молекулы- углеводы
Впервые термин «углеводы» предложил русский химик из Дерпта (ныне Тарту) К.Шмидт в 1844 году. Цели урока:. Дать общее понятие об углеводах, как о ...Строение и свойства предельных и непредельных углеводородов
Разминка. I I Вариант. 1.Углеводороды, содержащие. только простые связи. 2.Вещесва, сходные по строению, но отличающие на одну или несколько групп ...Производство аммиака
Изучить научные принципы производства аммиака. Цель. Задачи. Разработать оптимальные условия синтеза аммиака. Составить технологическую схему производства. ...Строение и функции белков
Элементарный состав белков. С (углерод) – 50-55%; О (кислород) – 21-24%; N (азот) – 15-17% (≈ 16%); Н (водород) – 6-8%; S (сера)– 0-2%. Азот - это ...Сложные эфиры. Жиры Строение, получение, свойства
Сложные эфиры. При взаимодействии карбоновых кислот со спиртами (реакция этерификации) образуются сложные эфиры: O O R1- C + R2 – OH R1- C +2H2O O ...Строение периодической таблицы Д.И. Менделеева
Металлы Неметаллы. Металлические свойства усиливаются, а неметаллические ослабевают; Увеличиваются заряды атомных ядер; Постоянно число электронов ...Конспекты
Азот. Строение атома и молекулы, свойства простого вещества
Тема урока. «. Азот. Строение атома и молекулы, свойства простого вещества. » 9-й класс. . Цель урока:. . . изучение строения атома и молекулы ...Аммиак. Строение молекулы. Физические и химические свойства. Получение, применение
ПЛАН-КОНСПЕКТ УРОКА Аммиак. Строение молекулы. Физические и химические свойства. Получение, применение. ФИО:. Исмаилова Венера Владимировна. ...Азотная кислота. Строение молекулы и получение
Дата_____________ Класс_______________. Тема:. . Азотная кислота. Строение молекулы и получение. Цели урока:. знать строение, свойства и применение ...Азот положение в ПСХЭ. Строение атома и молекулы. Физические и химические свойства
Опорный конспект по теме: «Азот положение в ПСХЭ. . Строение атома и молекулы. Физические и химические свойства. I. .Положение азота в ПСХЭ:. ...Строение атома
Урок по теме: «Строение атома». Задачи урока:. Образовательные. : сформировать представления о строении атома; дать понятие протон, электрон, ...Химическая связь. Строение вещества
Тема: Систематизация и обобщение знаний по теме «Химическая связь. Строение вещества». (стр. флипчарта 1 скрыть / показать). Цель:. . обобщить и ...Строение, способы получения и свойства алканов
Тема урока: Строение, способы получения и свойства алканов. . . Цель урока:. Изучить. . способы получения, физические и химические свойства, ...Строение предельных одноатомных спиртов. Изомерия и номенклатура
Урок 10 класса. . (по учебнику Г.Е. Рудзитиса). Тема: Строение предельных одноатомных спиртов. . . Изомерия и номенклатура. Цель:. . 1. ...Строение вещества
Автор: Теплов Сергей Евгеньевич. Место работы: МБОУ ООШ №30, г. Сургут. Должность: учитель физики. 7 класс. Тема урока: «Строение вещества». ...Строение атома. Химическая связь
Учитель: Язрикова Л.М. Предмет Химия. Класс 8 класс. Тема урока Обобщение по теме: «Строение атома. Химическая связь». Место темы в учебном ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:9 января 2019
Категория:Химия
Содержит:22 слайд(ов)
Поделись с друзьями:
Скачать презентацию