Презентация "Строение атома и атомного ядра" по химии – проект, доклад
Презентацию на тему "Строение атома и атомного ядра" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 20 слайд(ов).
Слайды презентации
Список похожих презентаций
Строение атомного ядра
Ядро. Ядро представляет собой центральную часть атома (см. также АТОМА СТРОЕНИЕ). В нем сосредоточены положительный электрический заряд и основная ...Химическая связь и строение атома
Понятие о химической связи. Химическая связь – это связь между атомами, обеспечивающая существование веществ с четко определенным составом. При образовании ...Изменения в составе ядра атома
Что означают записи:. 3CO2, 2K, O2, 3O2, 4H2O, 5H2SO4, O3. Разделите указанные вещества вещества на 2 группы. Запишите с помощью химических формул. ...Строение атома. Периодический закон Д.И.Менделеева в свете теории строения атома
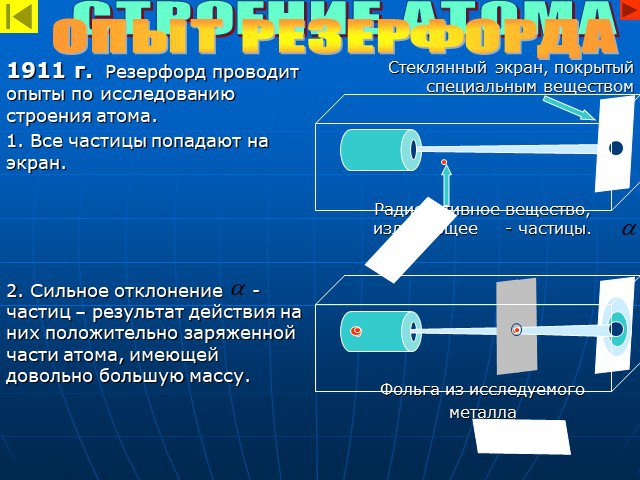
Родители атома. Демокрит (460 до н. э. — 370 до н. э.). Джозеф Джон Томсон (1856–1940 г). Эрнест Резерфорд (1871–1937г). Джеймс Чедвик (1891–1974г). ...Таблица Менделеева и строение атома
Элементы, атомы которых легко отдают ē для получения завершённого электронного уровня наз. металлами. Na + 11 8ē 1ē Mg ē. В. Что легче отдать 7ē или ...Подготовка к ЕГЭ "Строение атома"
Число электронов во внешнем электронном слое атома, ядро которого содержит 8 протонов, равно. 1) 8 2) 2 3) 6 4) 4. Число электронов в ионе железа ...Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома
ДЕВИЗ УРОКА:. Чтобы стать настоящим химиком, надо знать, уметь, думать!". ЭПИГРАФ УРОКА:. «… Другого ничего в природе нет, Ни здесь, ни там, в космических ...Строение атома Химическая связь
Девиз урока:. Дорога к знанию? Ну, что же, ее легко понять. Ответить можно сразу: Вы ошибаетесь и ошибаетесь, И ошибаетесь опять, но меньше, меньше, ...Строение атома, химическая связь
Цель урока:. Обобщить и систематизировать знания по теме «Строения атома, химическая связь». Задание № 1 Определите химический элемент по распределению ...Строение атома
СТРОЕНИЕ АТОМА. Студент должен:. Знать: Основные положения теории строения атома (ядра и состояния электронов), формулировку периодического закона ...Строение атома и его свойства
Атом какого химического элемента имеет приведенную ниже схему строения? 1) аргона 2) кислорода 3) серы 4) кальция. . Сколько электронов находится ...Строение атома
Маленькая точка, сделанная карандашом, состоит из огромного количества атомов, большего, чем количество жителей на Земле ! Демокрит. В основе философии ...Строение атома
Химический элемент-это определенный вид атомов. Модель атома Резерфорда. протоны электроны нейтроны. Характеристики элементарных частиц. Количество ...Строение атома
Планетарная модель атома. электрон +. Общий заряд атома равен 0. - 3. Сравнение размеров ядра и электрона. Распределение электронов по электронным ...Строение атома и периодическая система
Какие открытия сделали ученые? 1. И.В. Деберейнер 2. А. Шанкуртуа 3. Л. Мейер 4. Д. Ньюлендс 5. М. Складовская - Кюри 6. А. Беккерель 7. Э. Резерфорд ...Строение атома и периодическая система химических элементов
Е 1s 3s 4s 3p 4p 3d n = 1 n = 2 n = 3 n = 4. Энергетическая диаграмма АО для многоэлектронных атомов. Многоэлектронные атомы. 1s. Порядок заполнения ...Строение атома углерода
↓ ↓↑. Валентность углерода IV. Валентность углерода II. Строение атома углерода. 6 С 2е4е 1S2 2S2 2P2 6 С 2е4е 1S2 2S1 2P3. Гибридизация. Гибридизация ...Периодическая система химических элементов Д.И. Менделеева и строение атома
Цель:. Повторить основные теоретические вопросы программы 8 класса; Закрепить знания о причинах изменения свойств химических элементов на основании ...Состав атомного ядра. Изотопы
1932 г. протонно-нейтронная модель ядра. Иваненко Дмитрий Дмитриевич (29.07.1904 – 1994)- Советский физик-теоретик, Доктор физико-математических наук. ...Строение Бензола
Бензол С6Н6 – родоначальник ароматических углеводородов. Каждый из шести атомов углерода в его молекуле находится в состоянии sp2-гибридизации и связан ...Конспекты
Состав и строение атома
Тема: Состав и строение атома. Образовательная. : сформировать представления о строении атома; дать понятие протон, электрон, нейтрон. Развивающая. ...Азот положение в ПСХЭ. Строение атома и молекулы. Физические и химические свойства
Опорный конспект по теме: «Азот положение в ПСХЭ. . Строение атома и молекулы. Физические и химические свойства. I. .Положение азота в ПСХЭ:. ...Азот. Строение атома и молекулы, свойства простого вещества
Тема урока. «. Азот. Строение атома и молекулы, свойства простого вещества. » 9-й класс. . Цель урока:. . . изучение строения атома и молекулы ...Фосфор. Положение в п.с. Строение атома. Физические и химические свойства
Тема. Фосфор. Положение в п.с. Строение атома. Физические и химические свойства. Фосфор как элемент и простое вещество. Тип урока. – Комбинированный, ...Алюминий. Строение атома, физические и химические свойства простого вещества
ПЛАН-КОНСПЕКТ УРОКА. Тема: Алюминий. Строение атома, физические и химические свойства простого вещества. . . ФИО (полностью). . Иванова ...Строение атома
Контрольная работа по теме «Строение атома». Часть А. 1. Определите химический элемент по составу его атома - 18 p. +. , 20 n. 0. , 18 e. -. :. ...Строение атома. Электронные оболочки атомов
Урок повторение по теме:. «Строение атома. Электронные оболочки атомов». Учитель химии высшей категории Жансеитова Ф.М.,. . сш№ 9, г. Тараз. ...Строение атома
Урок химии в 8 классе. Тема: «Строение атома». Цель урока:. формировать понятия -атом, орбиталь, изотопы, протон, нейтрон, электрон, умение работать ...Строение атома. Химическая связь
Учитель: Язрикова Л.М. Предмет Химия. Класс 8 класс. Тема урока Обобщение по теме: «Строение атома. Химическая связь». Место темы в учебном ...Строение атома
Тема урока: “Строение атома”. Тип урока:. урок ознакомления с новым материалом. . . Цель:. дать понятие о составе атома и составе атомного ядра; ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:15 января 2015
Категория:Химия
Содержит:20 слайд(ов)
Поделись с друзьями:
Скачать презентацию