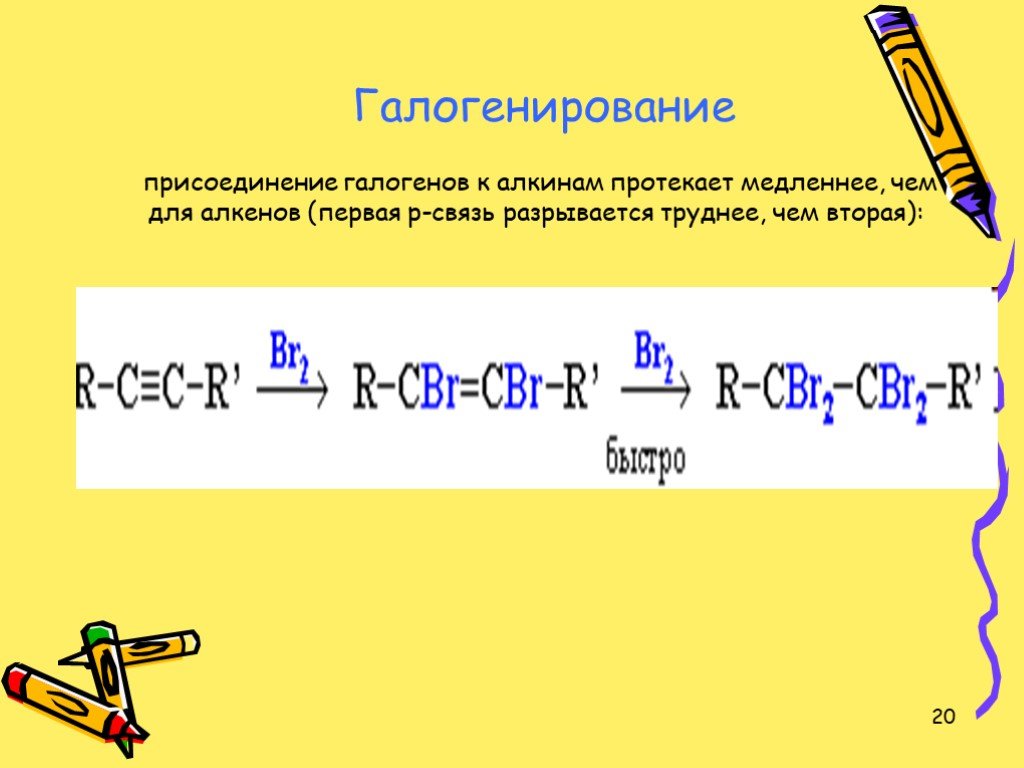
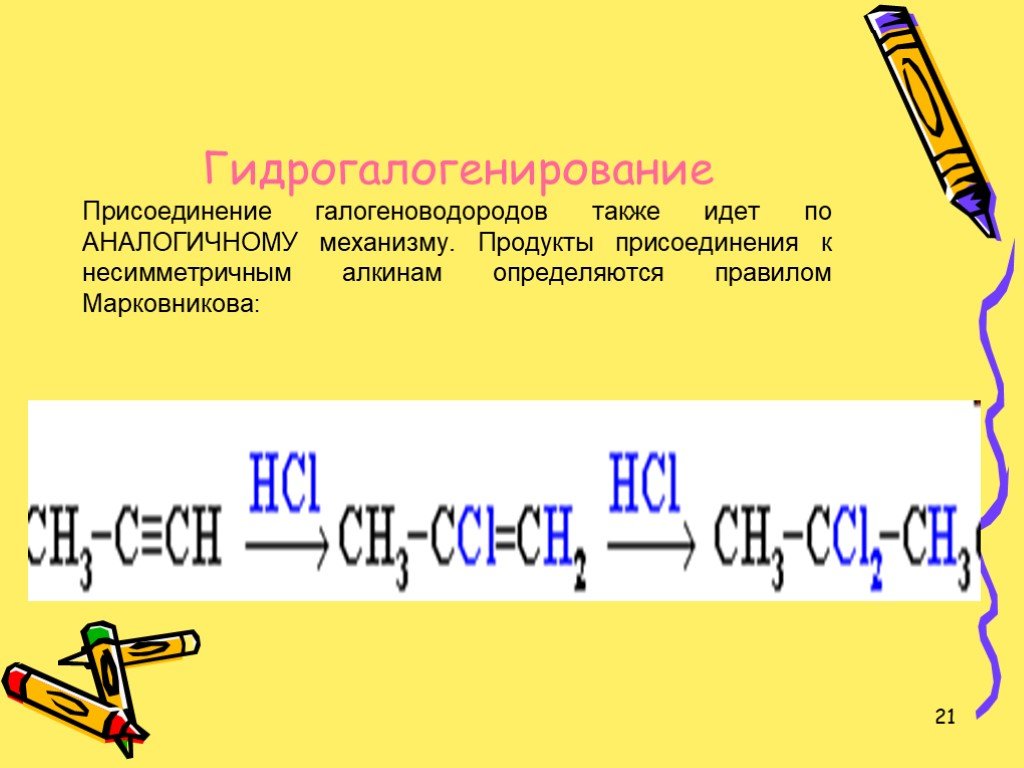
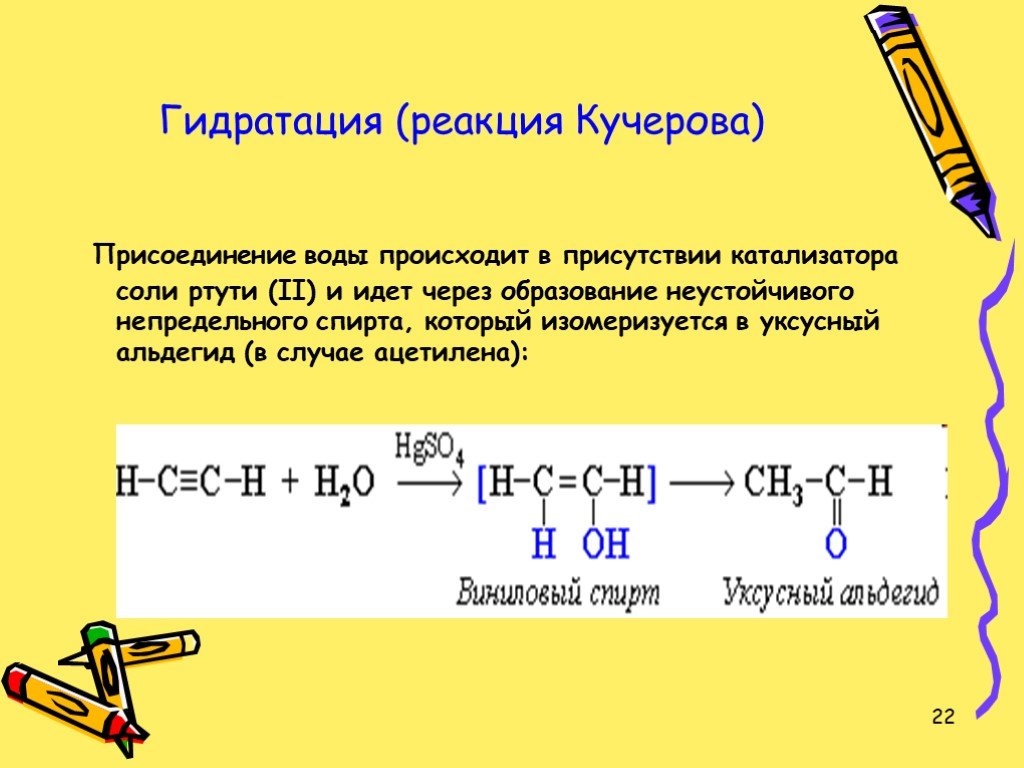
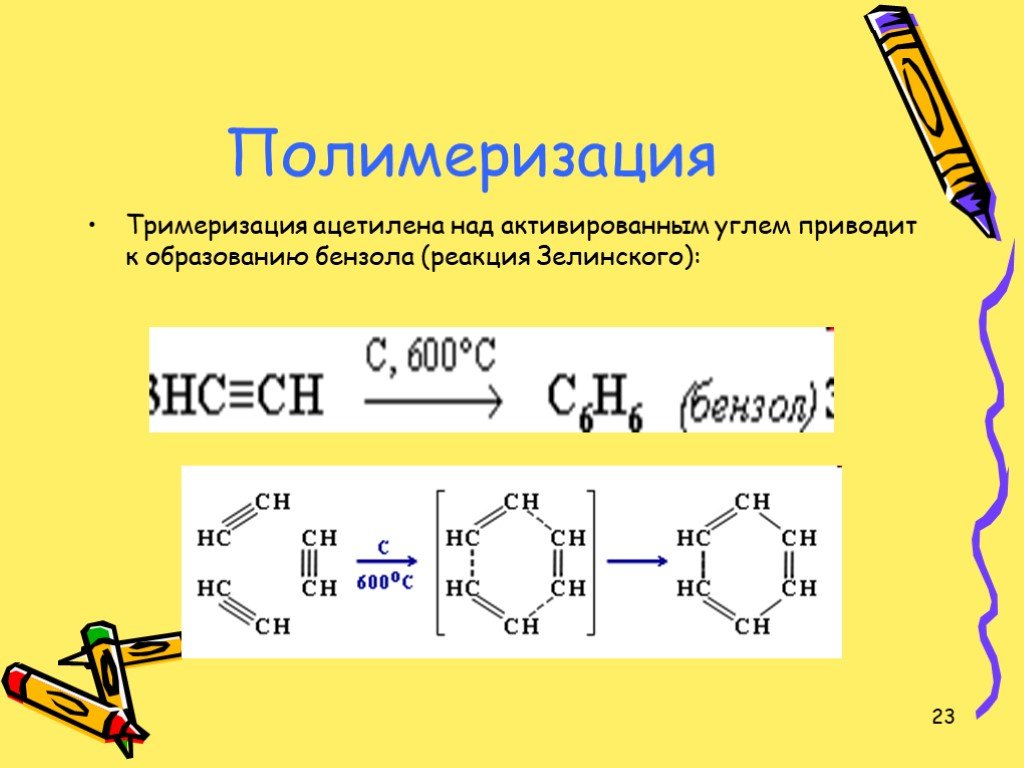
Презентация "Ацетилен и его гомологи" по химии – проект, доклад
Презентацию на тему "Ацетилен и его гомологи" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 35 слайд(ов).
Слайды презентации
Список похожих презентаций
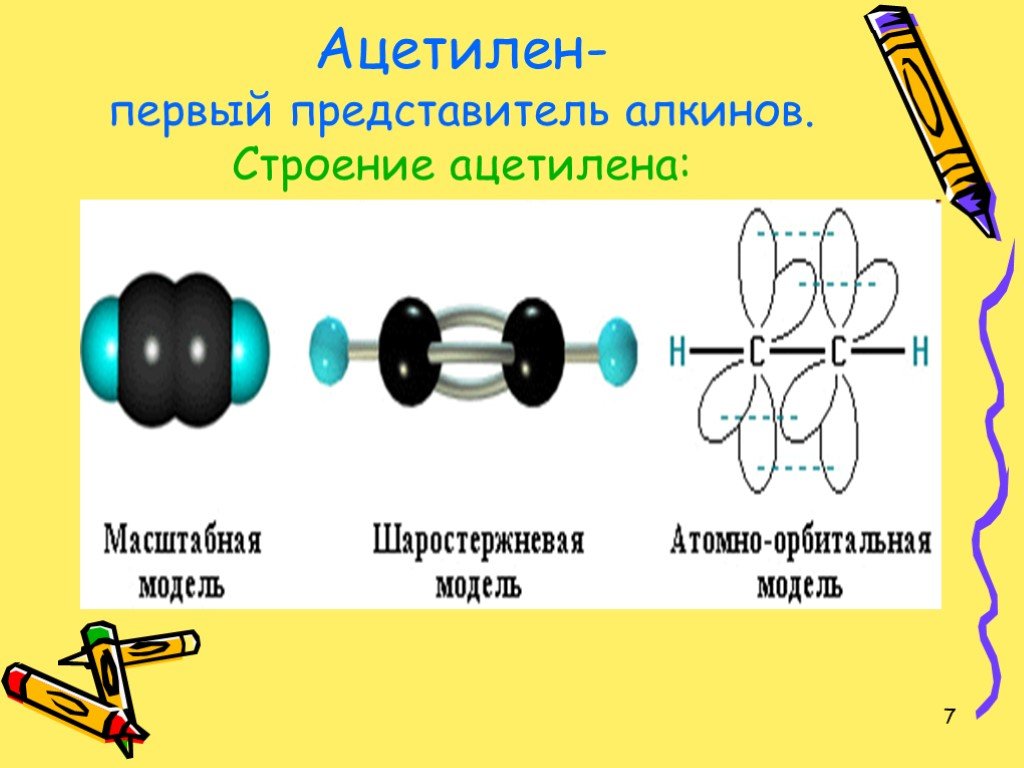
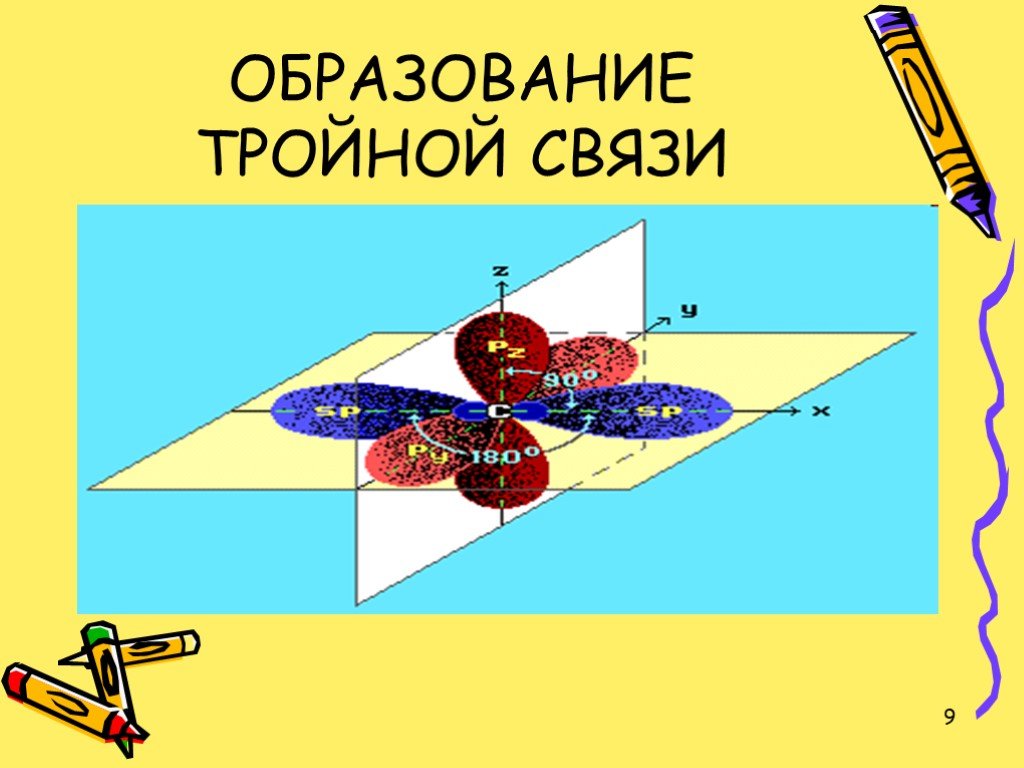
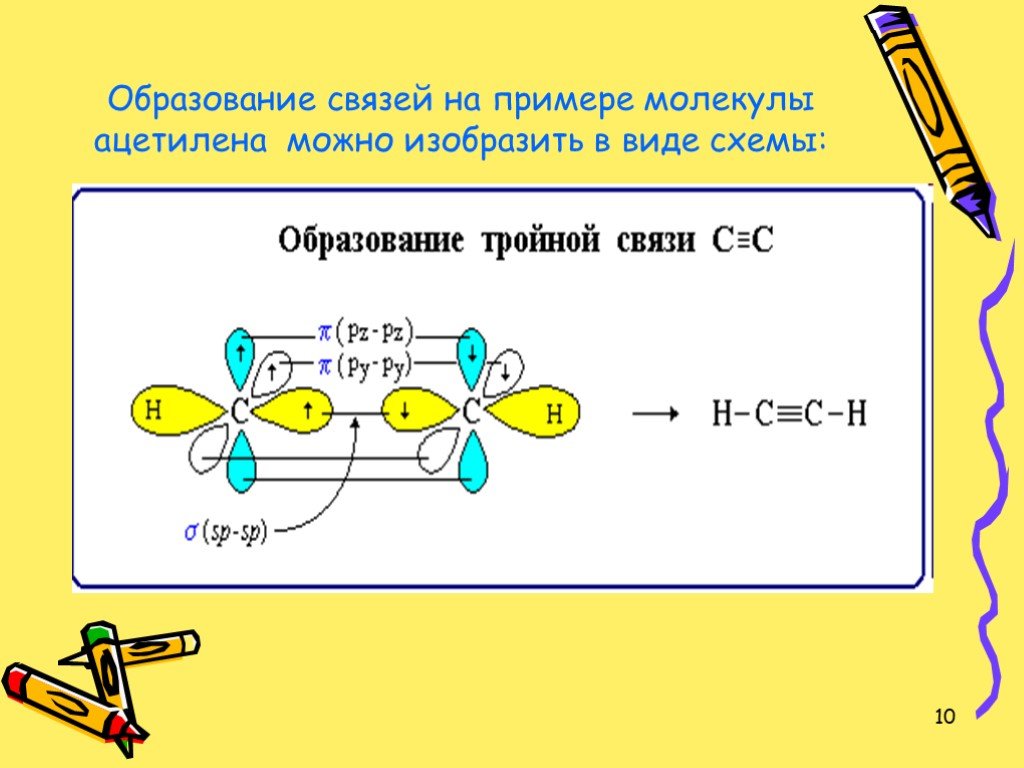
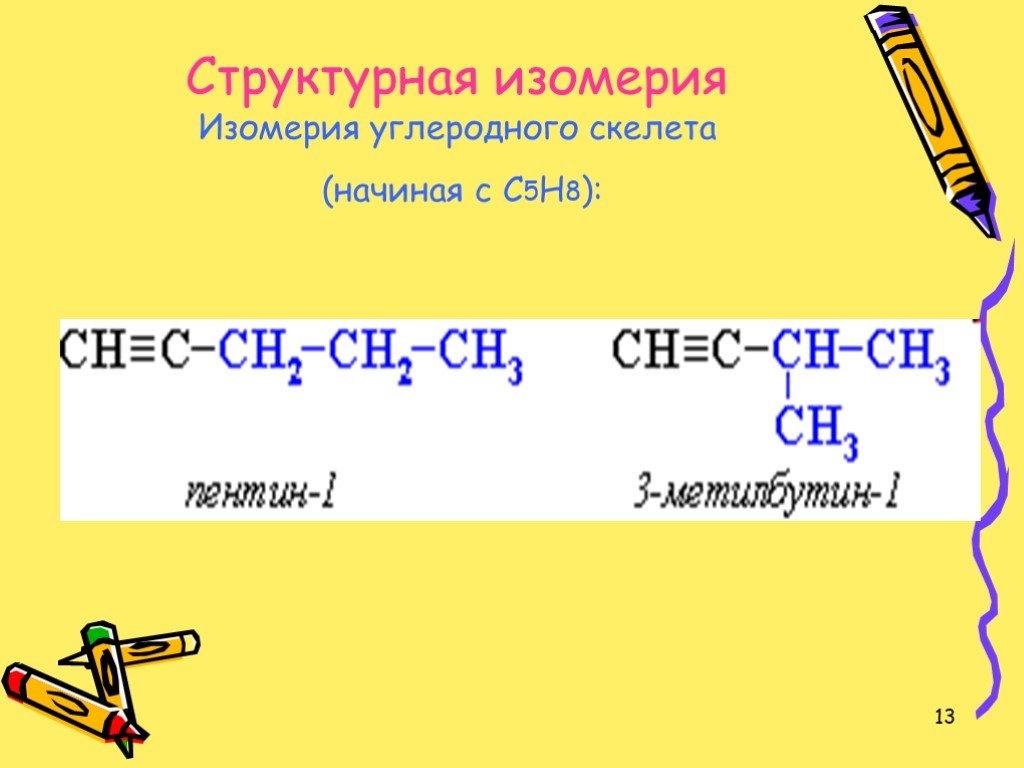
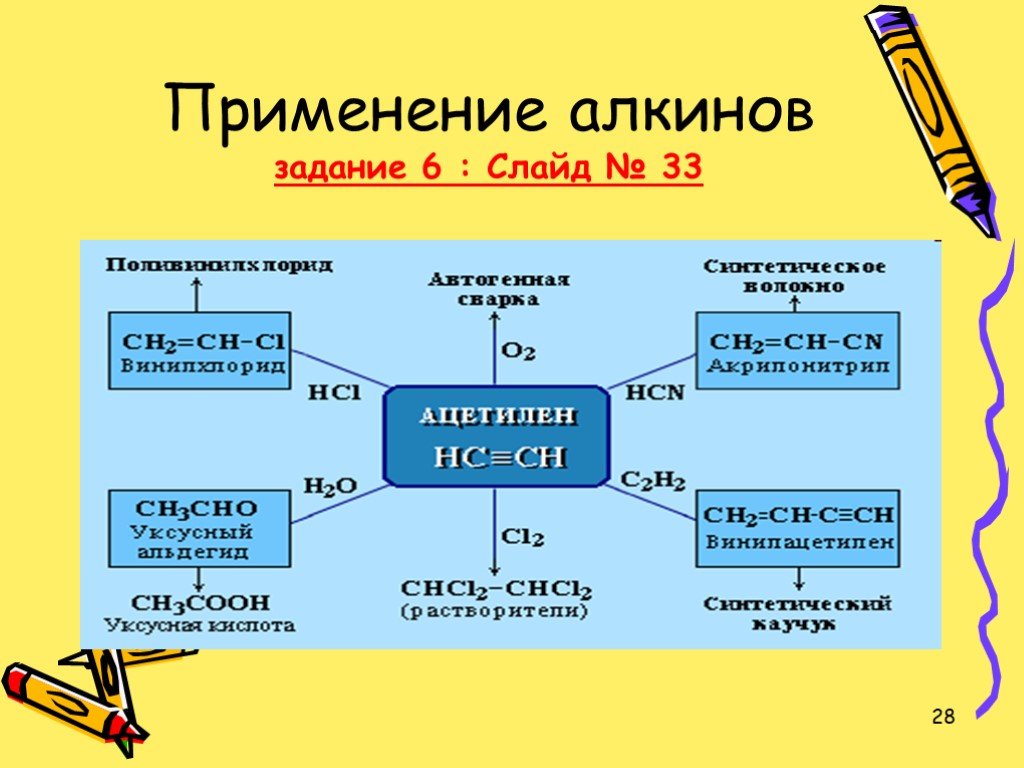
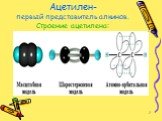
Ацетилен и его гомологи
Цели урока:. Познакомить учащихся с гомологическим рядом, изомерией и номенклатурой алкинов, с электронным и пространственным строением ацетилена. ...Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева
Закономерности изменения некоторых свойств химических элементов в ПС. 1. Положение элемента в ПС и строение его атома. ПЛАН ХАРАКТЕРИСТИКИ ХИМ. ЭЛЕМЕНТА. ...Фосфор и его соединения
«Чудовище лежало перед нами… Его огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза обведены огненными кругами. Я ...Углерод и его соединения
Необходимо вспомнить. Положение химического элемента в таблице Д.И.Менделеева. Электронная формула атома углерода. Какие высшую и низшую степени окисления ...Строение атома и его свойства
Атом какого химического элемента имеет приведенную ниже схему строения? 1) аргона 2) кислорода 3) серы 4) кальция. . Сколько электронов находится ...Магний и его сплавы
Свойства магния (сплавов магния). Магний является химически активным металлом: образующаяся на воздухе оксидная пленка МдО в силу более высокой плотности, ...Кремний и его соединения
Нахождение в природе. SiO2 кремнезём (песок). Al2O3∙ 2SiO2∙2H2O каолинит (глина). По распространенности занимает второе место после кислорода (26%). ...Алюминий и его свойства
Алюминий и его свойства. ППС. Химическая активность. Взаимодействие с простыми веществами. Взаимодействие с сложными веществами. получение лабораторное ...Алкины. Ацетилен – представитель алкинов
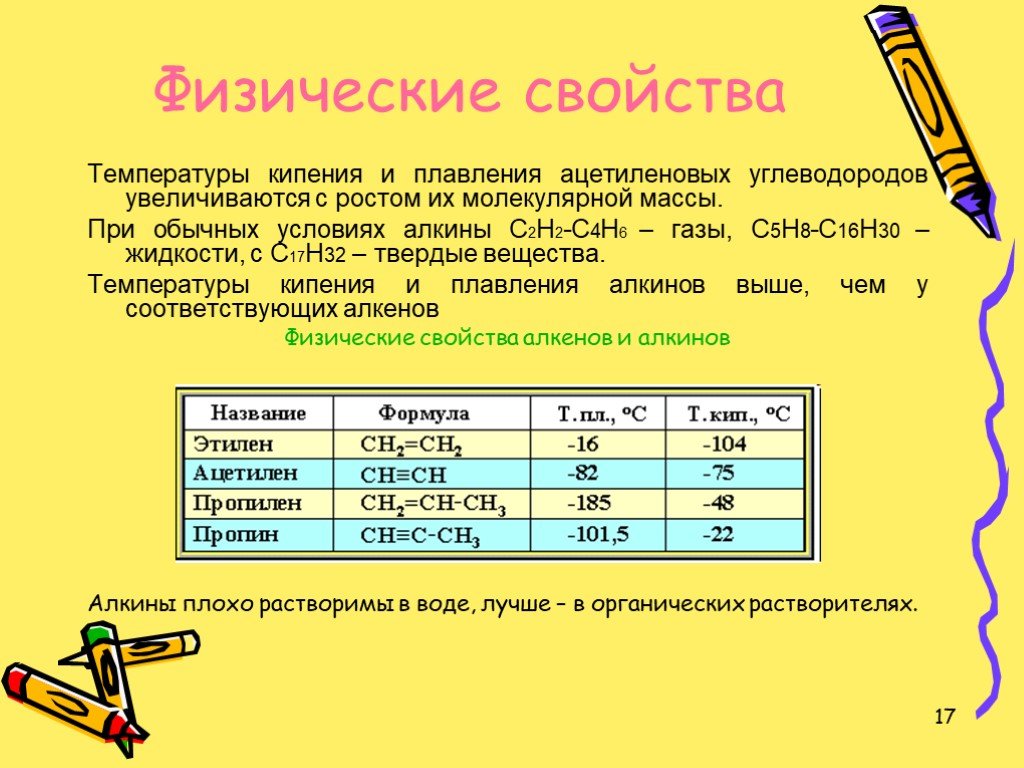
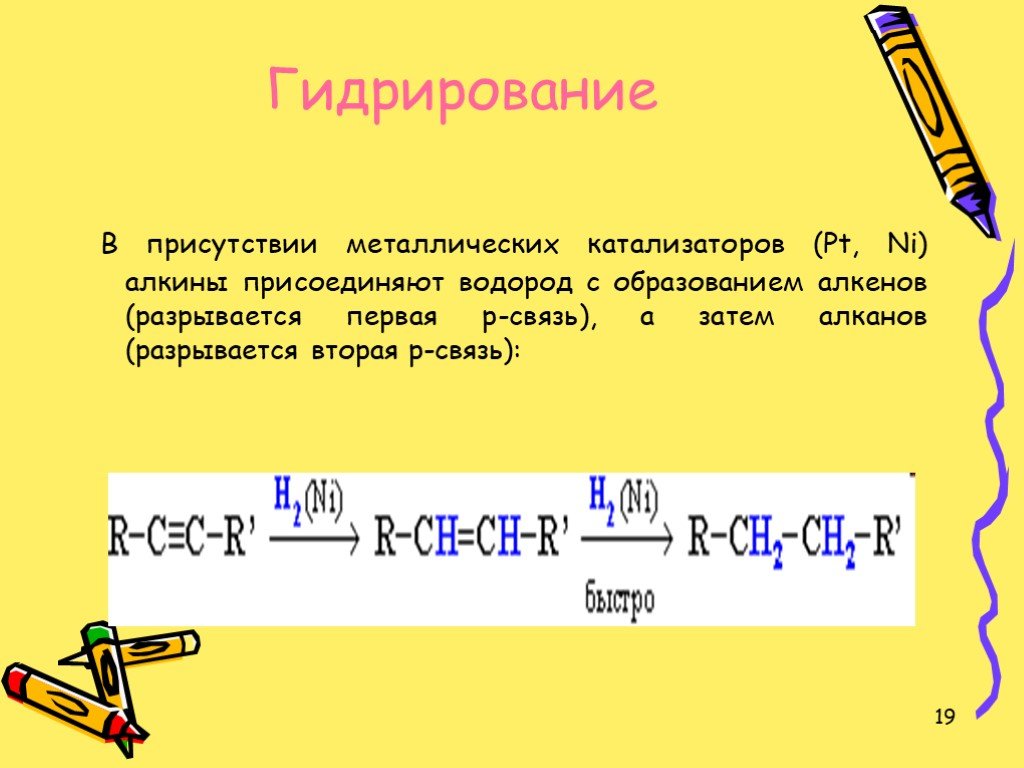
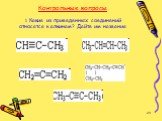
Цели:. Ознакомиться с гомологическим рядом, изомерией, номенклатурой алкинов. Рассмотреть способы получения ацетилена, изучить физические и химические ...Алкины. Ацетилен
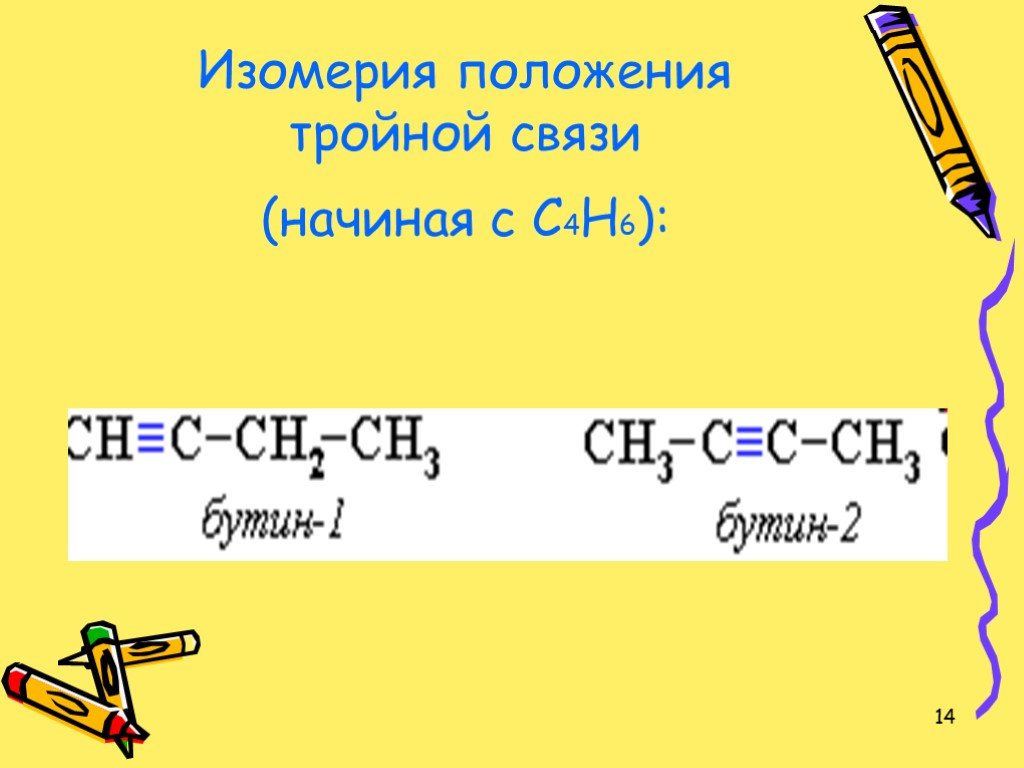
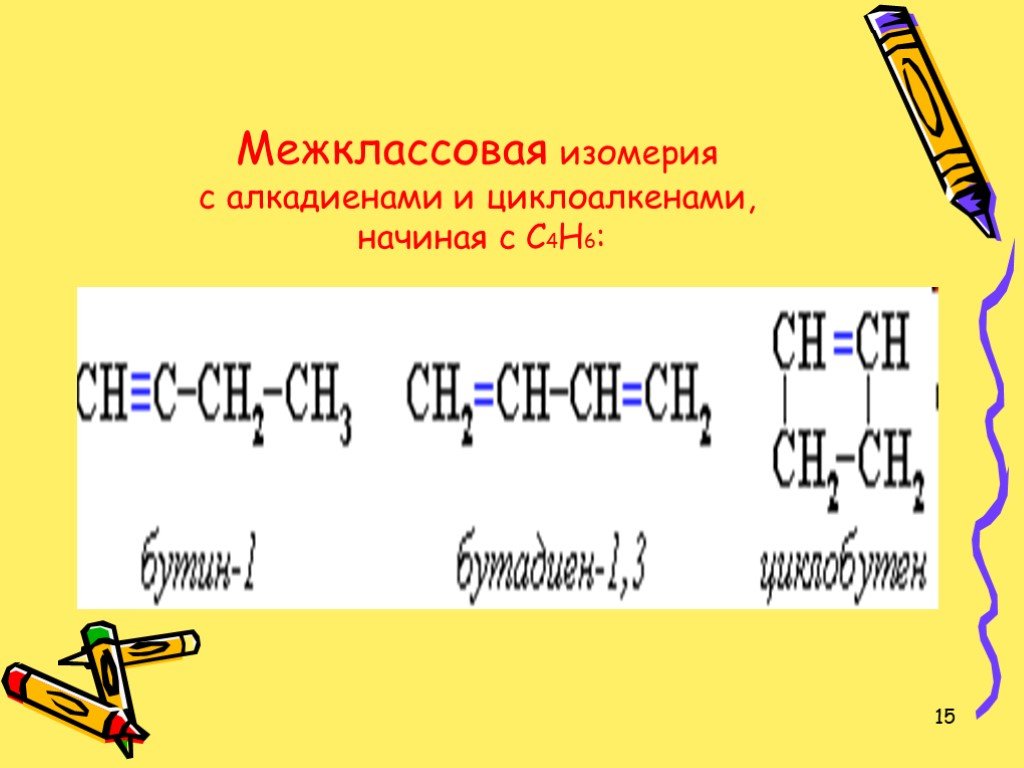
1. СН3 - СН3 2. СН2 = СН2 3. СН ≡ СН 4. СН2 = СН - СН = СН2. Среди указанных веществ выберите вещество, которое не относится ни к одному из изученных ...Алкадиены: строение, номенклатура, гомологи, изомерия
Познакомиться с понятием «алкадиены», их номенклатурой, изомерией, химическими свойствами и способами получения. Совершенствовать умения составлять ...Алексей Евграфович Фаворский и его вклад в победу СССР
Биография. Происходил из православного духовенства: его отец Евграф Андреевич Фаворский – был священником, брат адвоката Андрея Фаворского, дядя известного ...Азот и его соединения
Содержание. Открытие Происхождение названия Круговорот азота в природе Азот в природе Получение Свойства Соединения азота Применение. Открытие. В ...Азот и его свойства
История открытия азота:. В 1772 г. Англичанин Д. Резерфорд установил, что воздух, оставшийся под колоколом, где жила несколько дней мышь, освобожденный ...Кобальт и его соединения
Аннотация. Кобальт – это белый, слегка желтоватый металл с розоватым или синеватым отливом. Существует в двух кристаллических модификациях:. α-Co ...Алюминий и его соединения
Положение в Периодической системе. Алюминий располагается в 3 периоде, в главной подгруппе 3 группы. Порядковый номер элемента – 13 Относительная ...Кремний и его соединения
Дать общую характеристику элементу кремний. Рассмотреть природные соединения кремния. Провести сравнительный анализ с соединениями углерода. Изучить ...Алюминий и его соединения
Стартовое задание. Выполнение задания А оценивается одним баллом. Выполнение задания В оценивается 2 баллами. Выполнение задания С оценивается 3 баллами. ...Метан и его свойства
Предельные углеводороды. Метан. Алканы. Общая формула предельных углеводородов. CnH2n+2 где n≥1. При образовании связей атома углерода с водородом ...Конспекты
Отклоняющееся поведение и вещества, его вызывающие
Конспект урока по химии. «Отклоняющееся поведение и вещества, его вызывающие». . Цели:. . 1.Образовательная. :. раскрыть сущность таких явлений, ...Практическая работа №5 Получение оксида углерода(IV) и изучение его свойств. Распознавание карбонатов
Дата_____________ Класс_______________. Тема:. . Практическая работа №5 Получение оксида углерода(IV) и изучение его свойств. Распознавание карбонатов. ...Кремний и его соединения
Т.В.Кузнецова,учитель химии, школа № 53. . ПЛАН-КОНСПЕКТ УРОКА. . «Кремний и его соединения». (тема урока). . ФИО Кузнецова Татьяна ...Кремний и его соединения. Стекло. Цемент
Дата_____________ Класс_______________. Тема:. . Кремний и его соединения. Стекло. Цемент. Цели урока:. знать состав, строение, свойства оксидов ...Фосфор и его соединения
Тема урока: «Фосфор и его соединения». . Цель урока:. . • продолжить формирование понятий «элемент» и «вещество», а также показать многообразие ...Хлор и его поражающие действия. Алгоритм действий при авариях на химически опасных объектах
Конспект урока в 8 классе. по теме. «Хлор и его поражающие действия. . . Алгоритм действий при авариях на химически опасных объектах». Цели ...Алюминий. Положение алюминия в периодической системе и строение его атома. Нахождение в природе
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ. ОБЩАЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА № 81. Алюминий. Положение алюминия в периодической ...Фосфор и его свойства
МОУ «Средняя общеобразовательная школа № 4. г. Железногорска Курской области. УРОК В 9 КЛАССЕ ПО ТЕМЕ. «. Фосфор и его ...Алюминий, его физические и химические свойства
План – конспект урока. Тема урока:. Алюминий, его физические и химические свойства. Тип урока:. изучение нового материала. Цель:. обучающиеся ...Алюминий, его физические и химические свойства. Применение алюминия
. . Тема урока «Алюминий, его физические и химические свойства. Применение алюминия». Цель урока. . *продолжить формирование ключевых компетенций: ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:18 октября 2018
Категория:Химия
Содержит:35 слайд(ов)
Поделись с друзьями:
Скачать презентацию