Презентация "Щелочноземельные металлы" по химии – проект, доклад
Презентацию на тему "Щелочноземельные металлы" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 19 слайд(ов).
Слайды презентации
Список похожих презентаций
Щелочноземельные металлы
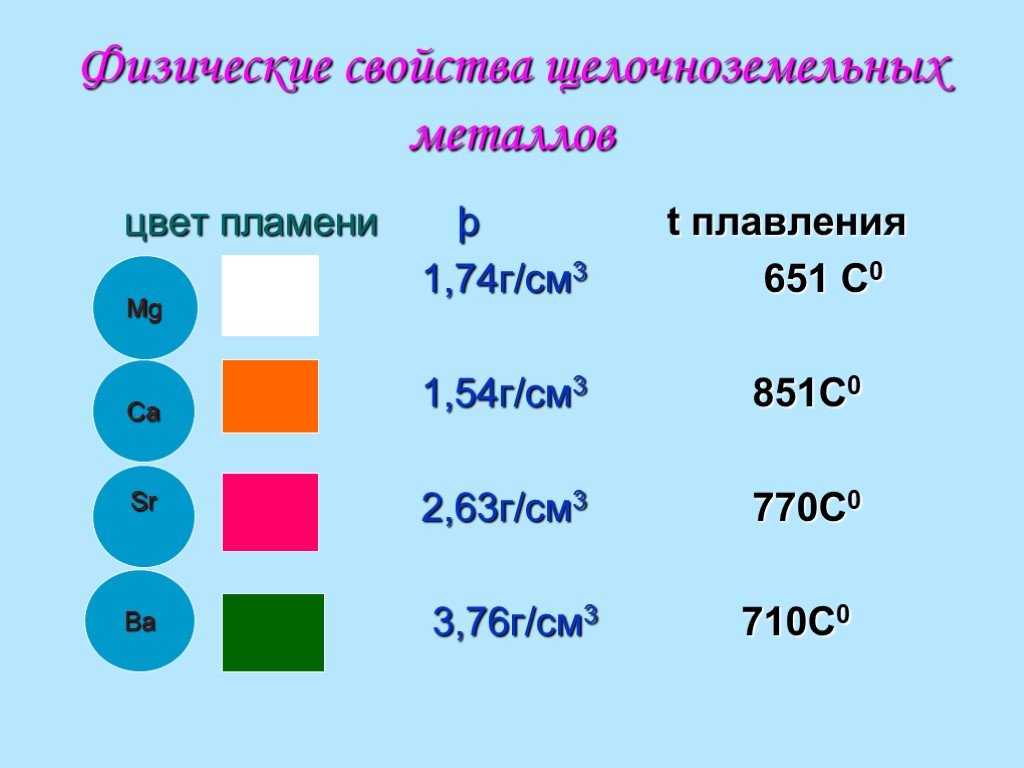
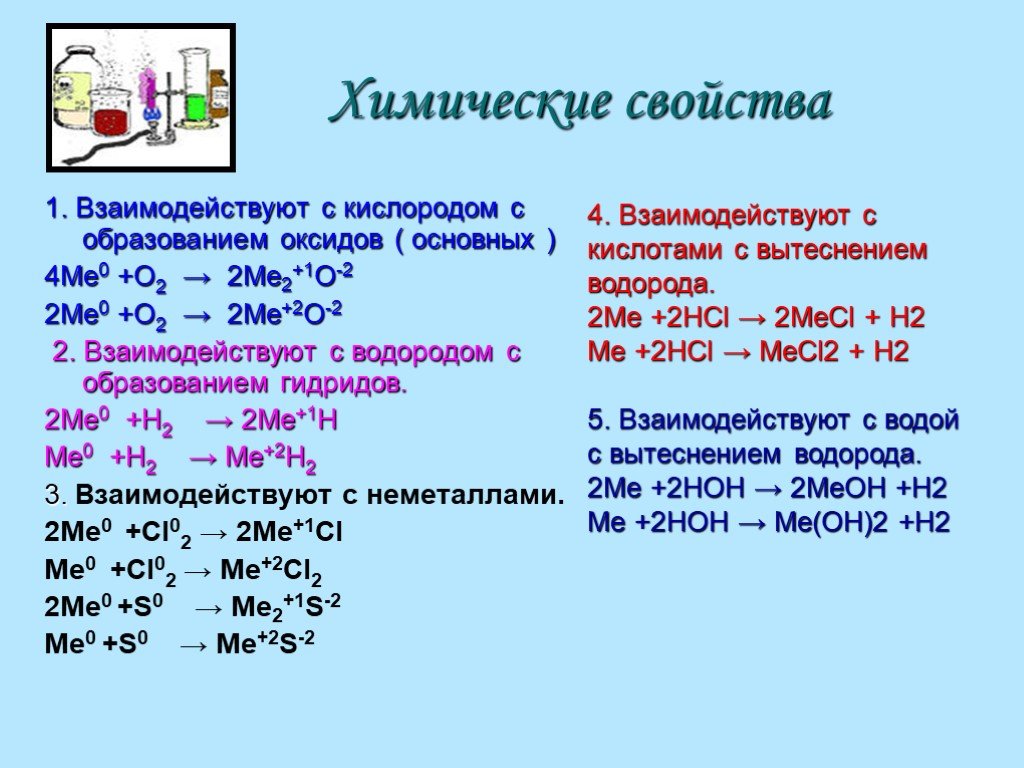
Щелочноземельные металлы. Хочу узнать. Физические свойства ЩЗ металлов; Химические свойства ЩЗ металлов; Применение. Цели урока:. Изучить физические, ...Щелочноземельные металлы
Цель:. Изучение строения атомов щелочноземельных металлов, физических и химических свойств. Положение в периодической таблице. Be Mg Ca Sr Ba Ra. ...Бериллий, магний и щелочноземельные металлы
Ве - амфотерный металл, Mg – металл, Сa, Sr,Ba - щёлочноземельные металлы Ra –радиоактивный элемент. Одинаковое строение внешнего электронного слоя ...Щелочные и щелочноземельные металлы
Щелочные металлы – элементы IA группы. Перечислите известные вам щелочные металлы. Сколько электронов на внешнем энергетическом уровне у атомов всех ...Щелочные металлы - элементы I группы главной подгруппы
Li Na K Rb Cs Fr. Физические свойства щелочных металлов:. Серебристого цвета Мягкие, легко режутся ножом Твердость от Li → Na → K → Rb → Cs → Fr уменьшается: ...Щелочные металлы
В одном царстве-государстве Жили-были, не тужили Галогены удалые И металлы щелочные. Скупых галогенов-окислителей В народе прозвали грабителями. А ...Щелочные металлы
Щелочные металлы. Периодическая система химических элементов Д.И.Менделеева. Группы элементов I III II VIII IV V VI VII 2 1 4 5 6 7 10 F фтор 9 18.9984 ...Щелочные металлы
Химические элементы главной подгруппы IА группы периодической системы элементов Д. И. Менделеева: Li, Na, К, Rb, Cs, Fr. Название получили от гидрооксидов ...Щелочные металлы
Щелочны́е мета́ллы — элементы главной подгруппы I группы Периодической системы химических элементов Д. И. Менделеева: литий Li, натрий Na, калий K, ...Тяжёлые металлы
РАССМОТРЕТЬ ВЛИЯНИЕ ТЯЖЕЛЫХ МЕТАЛЛОВ НА ОРГАНИЗМ ЧЕЛОВЕКА И ИСПОЛЬЗОВАТЬ ПОЛУЧЕННЫЕ ЗНАНИЯ В ДАЛЬНЕЙШЕЙ ЖИЗНИ. ТЯЖЕЛЫЕ МЕТАЛЛЫ. ЦЕЛЬ:. ОБЪЕКТ ИССЛЕДОВАНИЯ:. ...Простые вещества: металлы и неметаллы
I Стадия «Вызова». Верите ли вы в то, что: Среди известных химических элементов большая часть – металлы? (да) Металлы бывают жидкие (да) «Оловянная ...Простые вещества металлы
Цель урока:. Рассмотреть свойства металлов во взаимосвязи с областью их применения Продолжить работу по формированию интереса к предмету, расширению ...Простые вещества металлы
медь. серебро. ртуть. Металлы, простые вещества, обладающие в обычных условиях, характерными физическими и химическими свойствами. 1. Характерные ...Простые вещества - металлы и неметаллы
Цель урока:. Повторение основных сведений о простых веществах – металлах и неметаллах, путём выполнения различных заданий. Вопросы для обсуждения:. ...Металлы IА-группы щелочные металлы
14.11.2018 Что узнаем…. Положение щелочных металлов в Периодической системе Изменение свойств в группе История названия Нахождение в природе Физические ...Благородные металлы на службе у человека
Цель урока:. Рассмотреть и сравнить с разных точек зрения Химии и экологии; Литературы и философии; Географии и истории Самые популярные металлы окружающие ...Щелочные металлы
Цель урока:. познакомиться с историей открытия и распространением щелочных металлов в природе и живых организмах; изучить физические и химические ...Химические элементы металлы и здоровье человека
Ионы этого металла входят в состав вещества, употребляемого в пищу и называемого «белой смертью». Существенными источниками этого элемента являются ...Щелочные металлы
Цель урока:. Дать общую характеристику щелочным металлам. Рассмотреть их электронное строение, сравнить физические и химические свойства. Узнать о ...Химия металлы
Положение металлов в Периодической системе Строение атомов Кристаллические решётки Общие физические свойства Металлы в природе Способы получения металлов ...Конспекты
Бериллий, магний, щелочноземельные металлы
Разработка урока химии, 9 класс по теме «Бериллий, магний, щелочноземельные металлы» к учебнику О.С.Габриелян, Химия 9 класс: учебник для общеобразовательных ...Бериллий, магний и щелочноземельные металлы
«Бериллий, магний и щелочноземельные металлы». Цель: дать общую характеристику металлов главной подгруппы. II группы. Рассмотреть основные физические ...Щелочные металлы
. Урок химии в 9 классе. Щелочные металлы. Цели урока:. Дать общую характеристику ЩМ. Рассмотреть их атомное строение, основные физические, ...Щелочные металлы
МБОУ «СОШ № 36». учитель химии. . Курган Юлия Сергеевна. Тема урока: Щелочные металлы. Задачи урока:. Образовательная – ознакомить ...Щелочные металлы
Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». Конспект урока по химии в 9 классе. тема урока " Щелочные ...Щелочные металлы
Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». Конспект урока по химии в 9 классе. тема урока " Щелочные ...Удивительные металлы
Удивительные металлы. Цель урока:. Повторить и обобщить сведения о металлах. . как химических элементах , и как простых веществах. Задачи ...Способы классификации химических элементов. Понятие про щелочные металлы и галогены
Тема:. . Способы классификации химических элементов. Понятие про щелочные металлы и галогены. . . Цель:. . Закрепить знания учащихся о ...Простые вещества – металлы
Нижнекамский муниципальный район. г. Нижнекамск. Муниципальное бюджетное образовательное учреждение. «Средняя общеобразовательная школа №10. ...Простые вещества - металлы
Муниципальное казенное образовательное учреждение. . «Куйбышевская средняя общеобразовательная школа». . Среднеахтубинского района Волгоградской ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:2 октября 2018
Категория:Химия
Содержит:19 слайд(ов)
Поделись с друзьями:
Скачать презентацию