Презентация "Все о спиртах" по химии – проект, доклад
Презентацию на тему "Все о спиртах" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 41 слайд(ов).
Слайды презентации
Список похожих презентаций
Все о предельных одноатомных спиртах
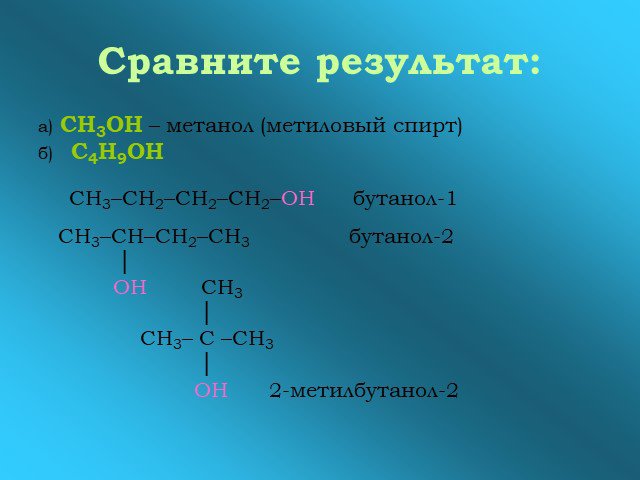
Определение спиртов Классификация спиртов Номенклатура Изомерия Физические свойства Химические свойства Физиологическое действие спиртов Применение ...Все о многоатомных спиртах
Цели урока:. Закрепить полученные знания об одноатомных спиртах. Познать новое (многоатомные спирты) в сравнении с одноатомными, найти в общем частное, ...проект: Все для фронта, все для Победы
«Наука есть источник высшего блага человечества в период труда. Но она и самое грозное оружие защиты и нападения во время войны» Н.Д.Зелинский Справедливо ...Все об алюминии
АЛЮМИНИЙ. нахождение в природе. Алюмосиликаты: Глина – Al2O3*nSiO2*mH2O Бокситы – Al2O3*nH2O. Строение атома. 27+13Al 2 8 3 1s22s22p1 *3 3 Al°-3ê ...Все о чае
История. Первоначально чай использовался в качестве лекарственного средства. Его употребление в качестве напитка широко распространилось во время ...Все о природном и попутном газе
Классификация газов. добывают из газовых месторождений. растворены в нефти и добываются вместе с ней. 23.02.2019. . Мировая добыча природного газа ...Все о пищевых добавках класса Е
С древних времён люди понимали важность питания для здоровья: «Ты есть то, что ты ешь», говорили они. Главные питательные вещества нашей пищu. Как ...Все о нуклеиновых кислотах
Проблемный вопрос. Подумайте и выскажите ваши предположения: А) Почему (в силу каких причин) именно молекулы ДНК, а не РНК выполняют функцию хранения ...Все о железе и его соединения
Урок-проект в 9 классе подготовила Яскевич В.А. учитель химии МОУ «Кадетская школа «Патриот» г.Энгельса 2010 г. План изучения вещества. Железо как ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Хасанова Р.Г. учитель химии
Содержит:41 слайд(ов)
Поделись с друзьями:
Скачать презентацию
















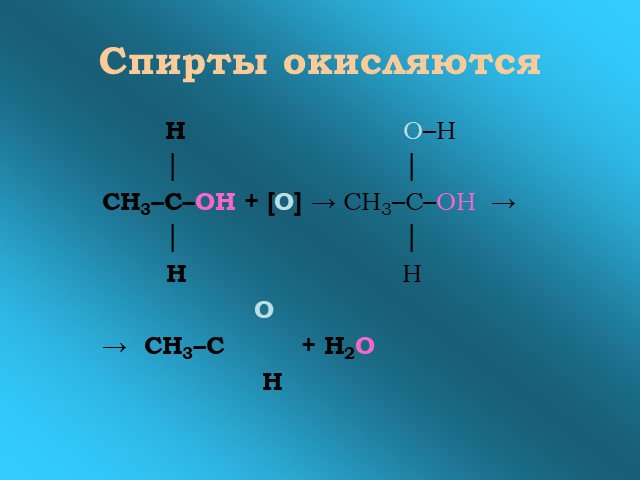

























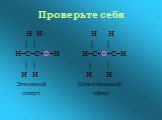













![Спирты окисляются. Н О–Н │ │ СН3–С–ОН + [О] → СН3–С–ОН → │ │ Н Н О → СН3–С + Н2О Н Спирты окисляются. Н О–Н │ │ СН3–С–ОН + [О] → СН3–С–ОН → │ │ Н Н О → СН3–С + Н2О Н](https://prezentacii.org/upload/cloud/14/09/4618/images/thumbs/screen19.jpg)

![СН3–СН2–СН2–ОН + [О] → О → СН3–СН2–С + Н2О Н СН3–СН2–СН2–ОН + [О] → О → СН3–СН2–С + Н2О Н](https://prezentacii.org/upload/cloud/14/09/4618/images/thumbs/screen22.jpg)