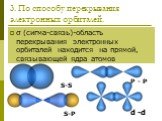
Презентация "Ковалентная связь и ее принципы" по химии – проект, доклад
Презентацию на тему "Ковалентная связь и ее принципы" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 21 слайд(ов).
Слайды презентации
Список похожих презентаций
Ковалентная связь: полярная и неполярная
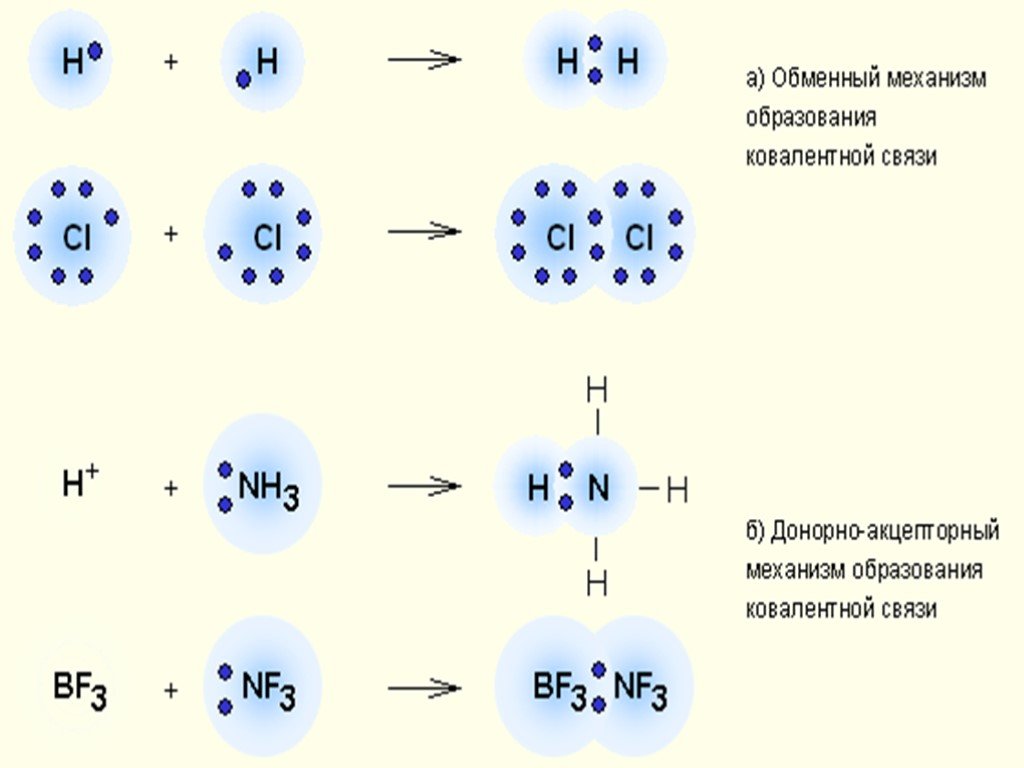
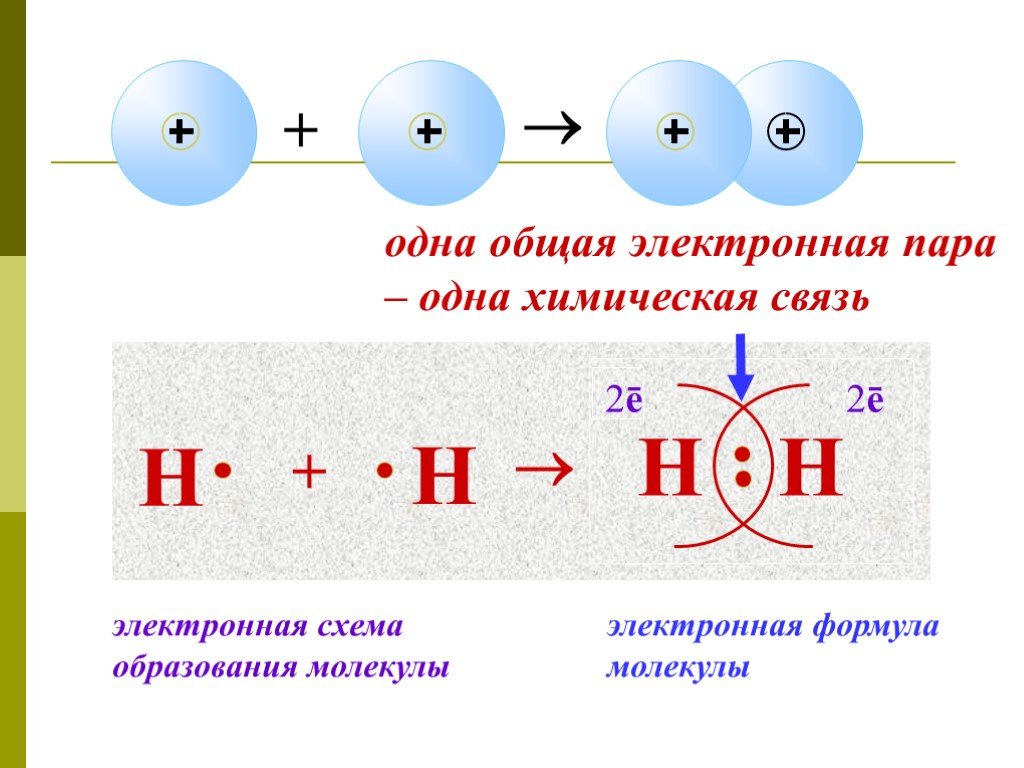
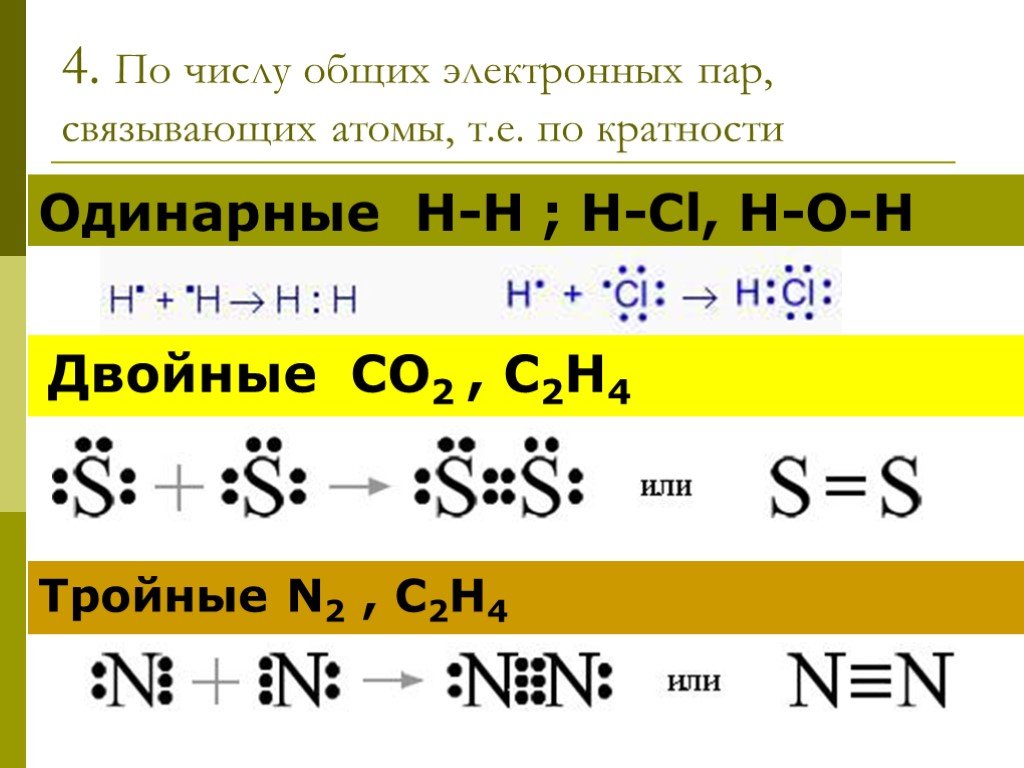
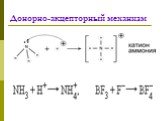
ОПРЕДЕЛЕНИЕ \ВЫУЧИТЬ\. КОВАЛЕНТНАЯ СВЯЗЬ-ЭТО ХИМИЧЕСКАЯ СВЯЗЬ МЕЖДУ АТОМАМИ,ОСУЩЕСТВЛЯЕМАЯ С ПОМОЩЬЮ ОБЩИХ ЭЛЕКТРОННЫХ ПАР. ОБРАЗОВАНИЕ КОВАЛЕНТНОЙ ...Ковалентная химическая связь
Химический диктант.Валентность – это ……. Валентные электроны – это Высшая валентность по кислороду равна ……….. Низшая валентность по водороду равна ...
Ковалентная полярная связь
Мы условно разделили элементы на металлы и неметаллы. Рассмотрели, как образуются связи между атомами металлов и неметаллов (как называется такой ...Ковалентная полярная химическая связь
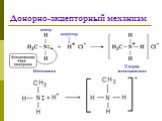
29/01/19. Тема: Ковалентная полярная химическая связь. I. Ковалентная связь. Химическая связь, возникающая в результате образования общих электронных ...Ковалентная неполярная связь
. VIIIB He Гелий 2 4,0026 1 H Водород 1,00794 Li Литий 6,939 Be Бериллий 4 9,012 В Бор 5 10,811 С Углерод 6 12,011 N Азот 7 14,0067 О Кислород 8 15,9994 ...Ковалентная полярная и неполярная связь
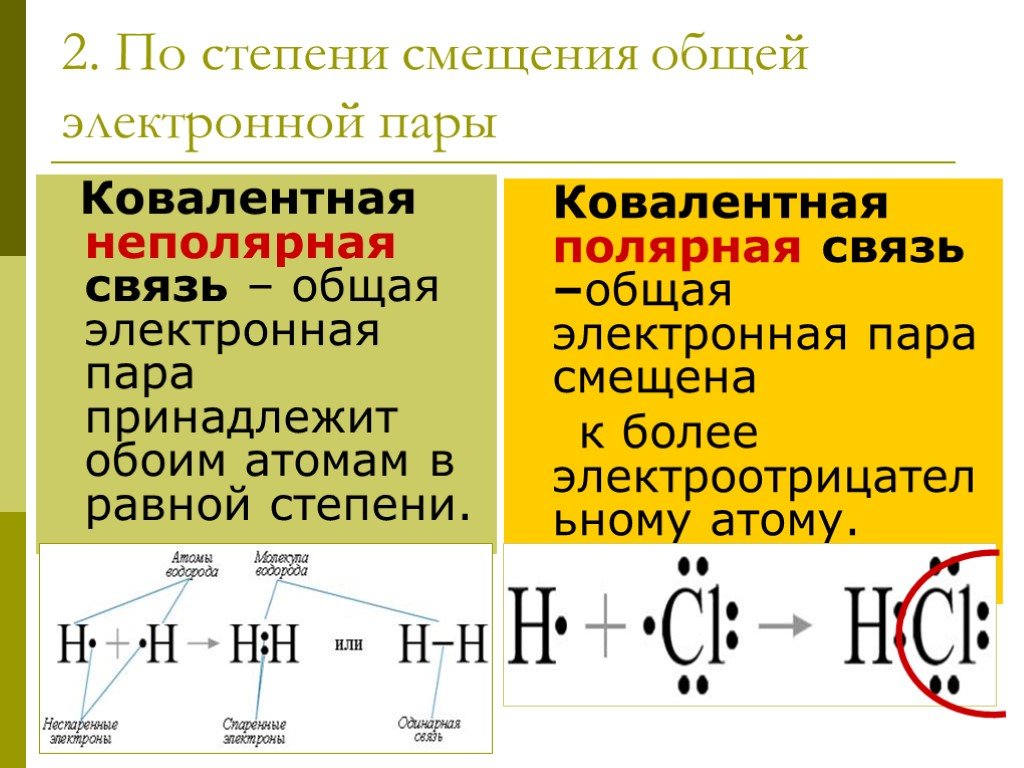
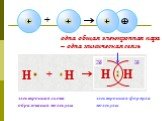
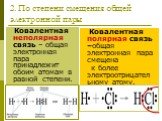
Ковалентная связь. неполярная полярная. Молекула образована атомами одного элемента, и общая электронная пара принадлежит обоим атомам в равной степени. ...Понятие о валентности и химической связи. Ковалентная химическая связь
Химическая связь – это силы взаимодействия, которые соединяют отдельные атомы в молекулы, ионы, кристаллы. Способность атома элемента образовывать ...Металлическая связь и ее свойства
Это связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке СХЕМА ...Раздел химии. Вода и ее свойство
Тема 2.1. Раздел химии. Вода и ее свойство. Вопрос 1. Введение в химию. Теоретические основы химии. В зависимости от того, какие вещества изучает ...Генетическая связь между классами неорганических вещ-в
Генетический ряд меди. Генетический ряд кремния. ЗАПИСАТЬ МОЛЕКУЛЯРНЫЕ УРАВНЕНЯ ПЕРЕХОДОВ. Литература:. 1.О.С.Габриелян Химия 8 , Дрофа 2009 2. О.С.Габриелян ...Нефть и способы ее переработки
Повторение – мать учения. Задание №1 1- Какие типы углеводородов существуют? В чем у них разница? 2- Какие группа углеводородов существуют? И описать. ...Нефть и ее переработка
горюча корисна копалина, складна суміш вуглеводнів різних класів з невеликою кількістю органічних кисневих, сірчистих і азотних сполук, що являє собою ...Химическая связь и строение атома
Понятие о химической связи. Химическая связь – это связь между атомами, обеспечивающая существование веществ с четко определенным составом. При образовании ...Вода и ее химические свойства
Молекулярное строение воды. Молекула воды состоит из 2 молекул водорода и 1 молекулы кислорода, которые находятся друг относительно друга под углом ...Ионная связь как химическая связь
ХИМИЧЕСКАЯ СВЯЗЬ -. сила, связывающая атомы в молекулы или другие частицы. - совокупность электростатических сил притяжения, связывающих атомы друг ...Изучение состава жевательной резинки и ее влияние на развитие семян
Цель и задачи:. Изучить влияние веществ, входящих в состав жевательной резинки на развитие зародыша семян пшеницы. Выяснить употребление жевательной ...Генетическая связь между неорганическими соединениями
Есть на свете наука, без которой сегодня невозможно воплотить в жизнь самые фантастические проекты и сказочные мечтания. это Х И М И Я. Задание 1. ...Генетическая связь между неорганическими веществами
Что? Почему? Как? « - Поиграй со мной, - попросил Маленький принц. – Мне так грустно … - Не могу я с тобой играть, - сказал Лис. – Я не приручен. ...Генетическая связь между классами неорганических веществ
А13-6-2009. В схеме превращений веществом «X2» является 1) Fe2O3 2) FeO 3) FeCl3 4) FeCl2. А13-2-2009. В схеме превращений веществами «X1» и «X2» ...Генетическая связь между классами неорганических веществ
Взаимосвязь между классами веществ выражается генетическими цепочками. Генетический ряд – это осуществление химических превращений, в результате которых ...Конспекты
Ковалентная связь
Методическая разработка. Ф.И.О. автор. . Шурыгина Валентина Сергеевна. Место работы. . МБСКОУ СКОШ № 34 VII. вида. г. Озерск, Челябинской ...Ковалентная химическая связь
Г. Гуково Ростовской области. Конспект урока по химии. . 8 класс. Тема урока «Ковалентная химическая связь». Подготовила Берлизова Юлия ...Ковалентная полярная связь
. Муниципальное бюджетное общеобразовательное учреждение. . Журавенская средняя общеобразовательная школа. . Методическая разработка ...Ковалентная полярная химическая связь
Конспект урока химии. Тема 11:. . Ковалентная полярная химическая связь. . . Цель урока:. изучить механизм образования ковалентной неполярной ...ПЗ и ПСХЭ Д.И.Менделеева. Химическая связь
9 класс Дата_________. Урок 1. Тема урока: ПЗ и ПСХЭ Д.И.Менделеева. Химическая связь. . Цель: 1. Обобщить, повторить, закрепить теоретические ...Положение металлов в периодической системе химических элементов Д. И. Менделеева. Металлическая связь
Дата_____________ Класс_______________. Тема:. . Положение металлов в периодической системе химических элементов Д. И. Менделеева. Металлическая ...Ковалентная химическая связь
Муниципальное Автономное Образовательное Учреждение. . Ветлужская Основная Общеобразовательная Школа. Конспект урока химии. ...Положение металлов в периодической системе Д.И.Менделеева. Металлическая связь
План – конспект. урока химии в 9в классе. «Положение металлов в периодической системе Д.И.Менделеева. Металлическая связь». Учитель: Кубусиди ...Вода и ее свойства. Твердое состояние
Муниципальное бюджетное дошкольное образовательное учреждение. «Детский сад №147 «Улыбка» комбинированного вида». города Чебоксары Чувашской Республики. ...Жесткость воды и способы ее устранения
". Жесткость воды и способы ее устранения". . . Цели урока:. образовательная:. сформировать представление о составе природных вод;. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:24 ноября 2018
Категория:Химия
Содержит:21 слайд(ов)
Поделись с друзьями:
Скачать презентацию