Презентация "Химические реакции" по химии – проект, доклад
Презентацию на тему "Химические реакции" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 17 слайд(ов).
Слайды презентации
Список похожих презентаций
Химические реакции. Мир химии
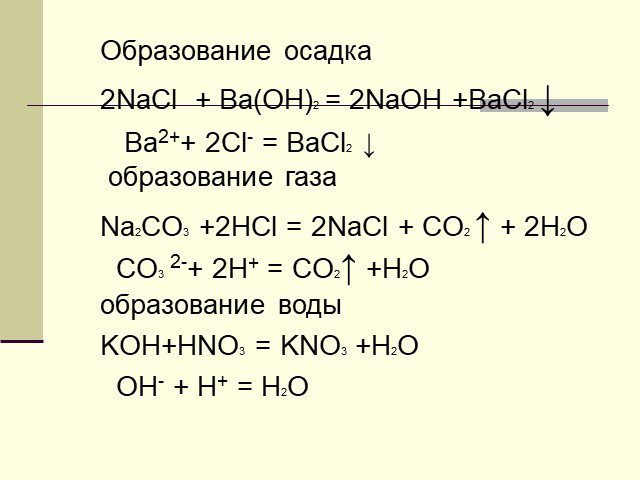
Признаки химической реакции! 1 Выделение газа. 2 Выделение теплоты. 3 Образование осадка. 4 Изменение цвета. 5 Выделение запаха. Реакции! Химическая ...Химические реакции
Химические реакции. Химический диктант. 1.почернение медной пластинки при нагревании, 2.плавление металла 3.Кипение воды 4.выделение пузырьков газа ...Химические реакции. Составление уравнений химических реакций
Цели и ожидаемые результаты. Повторить понятия как простые и сложные вещества, составление химической формулы вещества, химические реакции. Научиться ...Химические реакции в органической химии
Тест Напиши формулы углеводородов:. 1. Бутан 6. Метан 2. Этан 7. Гексан 3. Нонан 8. Декан 4. Гептан 9. Октан 5. Пропан 10. Пентан. Реакции горения:. ...Химические реакции и явления, которые их сопровождают
Растет дерево Замерзает вода Ржавеет металл. Растворяется сахар в чае. Извергается вулкан. Скисает молоко. Тема урока: Физические и химические явления. ...Химические реакции
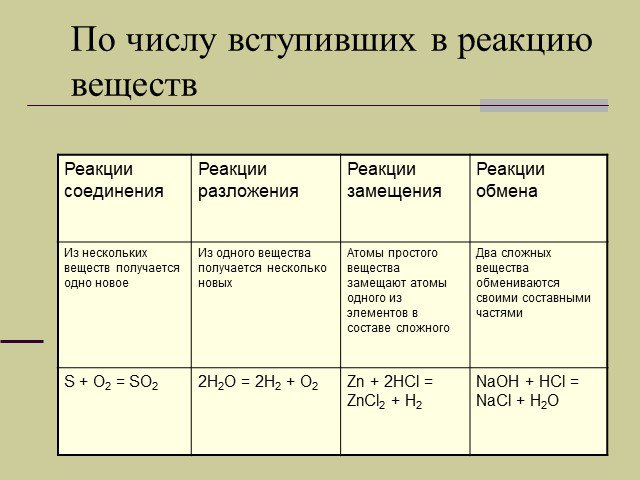
Типы химических реакций. По числу вступивших в реакцию веществ По тепловому эффекту По обратимости По изменению степени окисления По агрегатному состоянию ...Химические реакции
План урока. 1. Физические и химические явления. 2. Признаки химических реакций. 3. Условия протекания реакций. 4. Значение химических реакций. Как ...Химические реакции
Цели 1. Образовательная: Повторить основные свойства веществ. Повторить основные типы химических реакций. 2. Развивающая: Продолжать развитие наблюдательности ...Применение ацетилена. Химические реакции, лежащие в основе применения
Химические реакции, лежащие в основе применения ацетилена. Реакции получения и горения ацетилена CaC2 + 2H2O → Ca(OH)2 + C2H2 2C2H2 + 5O2 → 4CO2 +2H2O ...Химические реакции
Оглавление:. ВВЕДЕНИЕ КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ: По числу и составу реагирующих веществ По изменению степеней окисления химических элементов ...Химические реакции
Разминка. НСl Н2SО4 НNО3 Н3РО4 СаСl2 Н2SiО3 Мg(NO3)2 НI К3РО4 НNO2 Cu(OH)2. Серная кислота Соляная кислота Азотная кислота. Ортофосфорная кислота. ...Почему протекают химические реакции
Первый закон термодинамики – закон сохранения энергии. Энергия не возникает из ничего и не исчезает бесследно, а только переходит из одной формы в ...Химические уравнения. Реакции обмена
24.05.2019 Лебедева Л.В.Повторим изученный материал.
Какое слово зашифровано в таблице?
2Na+2HCl=2NaCl +H2↑ 2Al + 3S = Al2S3 Al(OH)3 = Al2O3 + ...
Почему протекают химические реакции
План урока. Закон сохранения массы и энергии. Тепловой эффект химической реакции. Экзотермические и эндотермические реакции. Термохимия. Законы термохимии. ...Почему протекают химические реакции
На бумаге можно написать уравнение любой химической реакции («бумага все стерпит»), а возможна ли такая реакция практически? В одних случаях (например, ...Окислительно – восстановительные реакции
Окислительно – восстановительные реакции. … – реакции, протекающие с изменением степени окисления элементов. Два антипода парою ходят, Первый – теряет; ...Химические свойства галогенов
Гипотеза. Молекулы простых веществ, образуемых атомами галогенов двухатомны. С увеличением радиуса атомов в ряду F, Cl, Br, I, At возрастает поляризуемость ...Химические свойства карбоновых кислот
Разминка. Номенклатура. Изомерия. Химические свойства КК, общие с неорганическими кислотами. Проверь себя! Цель урока:. изучить химические свойства ...Окислительно - восстановленные реакции
Окислительно-восстановительные реакции (ОВР) – реакции, сопровождающиеся изменением степени окисления элементов (атомов). Степень окисления (СО) – ...Химические свойства алкенов. Получение
Прогноз реакционной способности алкенов. – наличие двойной связи позволяет отнести алкены к ненасыщенным соединениям. Превращение их в насыщенные ...Конспекты
Химические реакции. Признаки химических реакций
Тема: Химические реакции. Признаки химических реакций. Тип урока. : изучение нового материала и первичного закрепления знаний. Вид урока. : ...Химические реакции. Электролиз
ПЛАН-КОНСПЕКТ УРОКА Тема урока. : Электролиз. . ФИО. . . Хубиева Людмила Руслановна. . . . Место работы. . МБОУ СОШ ...Химические реакции
8 класс. Урок по теме «Химические реакции». Цель:. обобщить и систематизировать знания по теме «Химические реакции». Задачи: 1) образовательная:. ...Химические реакции
«Химическое путешествие. Обобщение знаний учащихся по теме «Химические реакции»». Задачи урока. Образовательные:. повторить и обобщить знания ...Химические реакции
Практическое занятие №2 «Примеры проектов уроков с использованием интерактивного оборудования и Интернет-ресурсов». Проект урока химии урока в ...Химические реакции
Министерство общего и профессионального образования Свердловской области. Муниципальное общеобразовательное учреждение. «Средняя общеобразовательная ...Физические и химические явления. Химические реакции
Урок химии в 8 классе на тему. :. Физические и химические явления. Химические реакции. . . Савинская Татьяна Андреевна. учитель химии и биологии. ...Химические реакции
Химические реакции. Цели урока:. Повторить отличия химических явлений от физических. . Познакомить с признаками и условиями течения химических ...Физические и химические явления. Химические реакции
« Химия». Тема урока: «Физические и химические явления. Химические реакции». Предмет: Химия Класс :8. Занозина Елена Владимировна , учитель химии ...Химические свойства солей
. Зайчикова Ирина Николаевна. МБОУ «Пригородная СОШ». Учитель химии, биологии. Разработка урока по химии в 8 классе «Химические свойства ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Болгова Е.Д., преподаватель химии
Содержит:17 слайд(ов)
Поделись с друзьями:
Скачать презентацию