Обобщение по теме "Металлы" презентация, проект, доклад
Презентацию на тему "Обобщение по теме "Металлы"" (9 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 10 слайд(ов).
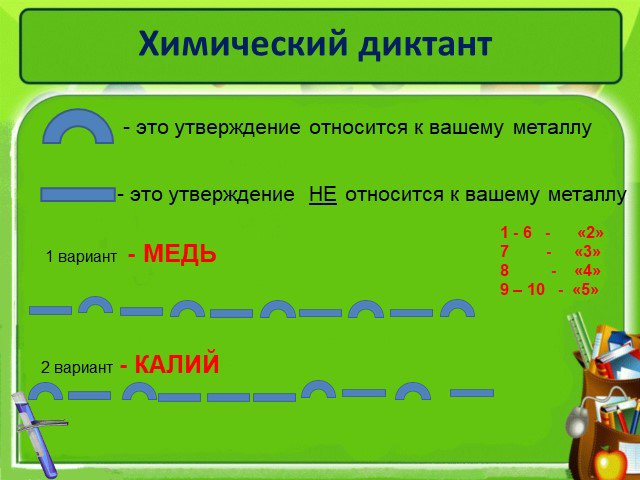
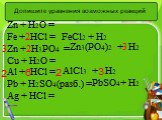
Слайды презентации
Список похожих презентаций
«Систематизация и обобщение знаний по теме «Типы химических реакций»»
1) Что называют химической реакцией? 2) По каким признакам можно утверждать, что произошла или происходит химическая реакция? 3) Какие условия необходимы ...8 класс Обобщение знаний по теме СЛОЖНЫЕ ВЕЩЕСТВА
Вещества Простые Сложные Металлы Неметаллы Оксиды Основания Кислоты Соли. ЭnОm. Сложные вещества, состоящие из двух элементов, один из которых кислород ...Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам курса неорганической химии
Х И М И Ч Е С К А Я В И К Т О Р И Н А «Знаешь ли ты это? 11 класс. ТЕМА: «Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам ...Обобщающий урок-тест по химии "Металлы"
Вопрос №1. Какой металл занимает первое место в земной коре среди металлов: 1) железо 2) медь 3) алюминий 4) цинк. Вопрос №2. Какой из металлов при ...Металлы в периодической системе
Задачи урока 28.12.2017. Повторить известное: металлическая связь, образование и характеристика. Узнать новое: положение металлов в периодической ...Металлы в природе. Общие способы их получения
Распространенность металлов в природе. Содержание некоторых металлов в земной коре: Алюминий 8,2% Железо 5,0% Кальций 4,1% Натрий 2,3% Магний 2,3% ...Беземская И.В._Презентация к уроку_по теме Вода
А Б В Г. « Просто знать – еще не все, знания нужно уметь использовать» Гете. «Просто знать – еще не все, знания нужно уметь использовать» Гете. Бинарными ...Металлы в периодической системе
Количество металлов среди всех химических элементов. История открытия металлов человеком. с древних времён и до нашей эры. средние века XVIII век. ...Металлы
положение металлов в периодической системе Д. И. менделеева. Условная граница между элементами-металлами и элементами-неметаллами проходит по диагонали: ...Металлы
Мета́ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как ..."Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Содержание химии очень обширно и часто предстает копилкой огромного числа формул, уравнений, фактов и законов, запомнить которые не просто трудно, ...Методические рекомендации по подготовке к ЕГЭ по химии
Кодификатор. Программа элективного курса «окислительно-восстановительные реакции». H2O2 H2SO4. «окислительно-восстановительные реакции в органической ...Металлы и неметаллы
Классификация веществ по составу:. Простые вещества состоят из атомов одного химического элемента. Сложные вещества состоят из атомов разных химических ...Металлы в организме человека
Человек – это мыслящий орган природы, другого значения он не имеет. Посредством человека материя стремится познать саму себя. В этом – всё. М. Горький. ...Металлы IА-группы щелочные металлы
14.11.2018 Что узнаем…. Положение щелочных металлов в Периодической системе Изменение свойств в группе История названия Нахождение в природе Физические ...Викторина по химии "Что это?"
РЕБЯТА!!! ЗА МНОЙ!!! К ВИКТОРИНЕ «ЧТО ЭТО?». ОПРЕДЕЛЯЕМ, О КАКИХ ВЕЩЕСТВАХ ИДЕТ РЕЧЬ??? 1 2 4 5 6 7 8 9 10 11 12 ВЫБИРАЙ!! Трудно представить, что ...Викторина по химии
1.Газ, который применили во время первой мировой войны в качестве химического оружия. 2. Единственный жидкий металл. 3.Русский учёный - энциклопедист. ...Викторина «Своя игра» по химии
Вопрос. Отечественный ученый, назвавший человека – «мощной геологической силой, способной изменить лик Земли»? Как называется нарушение природной ...Анализ результатов ЕГЭ по химии 2010 (окружной семинар учителей химии)
Результаты ЕГЭ 2010. Граница минимального балла -33 тестовых балла (12 первичных баллов). Уровни оценивания: неудовлетворительный – 0–32 / 0–11; удовлетворительный ...Анализ ЕГЭ по химии 2011
Уровни выполнения экзаменационной работы. неудовлетворительный – 0–31 / 0–12, удовлетворительный –32–56 / 13–35, хороший – 57–77 / 36–56, отличный ...Конспекты
Обобщение и систематизация знаний по теме « Чистые вещества и смеси, массовая и объемная доли
Конспект урока по теме «Обобщение и систематизация знаний по теме « Чистые вещества и смеси, массовая и объемная доли»». Цель урока:. . 1) Обобщить ...Повторение и обобщение по теме: «Классификация сложных неорганических соединений
Сценарный план урока. «Повторение и обобщение по теме: «Классификация сложных неорганических соединений». Цели и задачи урока:. . . Образовательная:. ...Металлы главных подгрупп периодической системы элементов Д.И.Менделеева
Модуль 1. Тема: «Металлы главных подгрупп периодической системы элементов Д.И.Менделеева». номер. учебного. элемента. (УЭ). Учебный материал ...Общая характеристика металлов. Металлы главных и побочных подгрупп. Щелочные металлы и их важнейшие соединения
План учебного занятия № 10. Дата Предмет. химия. группа. Ф.И.О. преподавателя. : Кайырбекова И.А. . І. Тема занятия:. Общая характеристика металлов. ...Металлы на пути к Победе
Урок на тему «Металлы на пути к Победе». Открытый урок посвященный 70 летию Победы в ВОВ. Подготовила и провела учитель химии сш.№9 Жансеитова ...Расследование по теме
I Региональный конкурс профессионального мастерства педагогов. «Мой лучший урок» (ЕСТЕСТВЕННО-НАУЧНОЕ направление). Чернышёва Татьяна Викторовна, ...Задачи по теме «Галогены
Задачи по теме «Галогены». №1. Сколько миллилитров раствора с массовой долей соляной кислоты 36 % (пл. 1,2 г/мл) необходимо для взаимодействия 0,1 ...Металлы побочных подгрупп. Железо-металл 19 века
Урок составлен: учитель химии МКОУ Дракинская СОШ Лискинского района Воронежской области. Баранова Виктория Владимировна. Тема: Металлы побочных ...Обобщение знаний по классам неорганических соединений
Тема урока. . Обобщение знаний по классам неорганических соединений. ( урок для учащихся 8 классов по неорганической химии, изучаемый в разделе « ...Металлы – простые вещества с использованием ИКТ на уроке
Конспект урока химии (по программе О.С. Габриеляна) в 8 классе на тему «Металлы – простые вещества с использованием ИКТ на уроке». Автор: Карачева ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:8 мая 2016
Категория:Химия
Классы:
Содержит:10 слайд(ов)
Поделись с друзьями:
Скачать презентацию