Презентация "Металлы в природе. Общие способы их получения" по химии – проект, доклад
Презентацию на тему "Металлы в природе. Общие способы их получения" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 22 слайд(ов).
Слайды презентации
Список похожих презентаций
Нахождение металлов и их соединений в природе
«Человек не может обойтись без металлов. Если бы не металлы, человек влачил бы самую жалкую жизнь среди диких зверей» Г. Агрикола XVI век. Альманах ...НЕМЕТАЛЛЫ природные соединения применения продуктов их переработки
Элементы в природе. Нахождение в природе. Самородные элементы. Сера Графит С Алмаз С. Азот и кислород, инертные газы в составе воздуха. Нахождение ...Неметаллы и их характеристика
Разгадайте ребусы и назовите три химических элемента названия которых здесь зашифрованы:. уГ+лес,Т=Д , газ + , ,,,+. К какой группе относятся эти ...Натрий.Способы получения
Электролиз расплава хлорида натрия (поваренной соли) 2NaCl → 2Na + Cl₂ Для получения расплава кристаллы хлорида натрия необходимо нагреть до 500 – ...Алкины-способы получения и химические свойства
Тема и цели урока:. Тема: «Ацетилен. Алкины». Цель урока: Дать представления об углеводородах с тройной связью. О их физико-химических свойствах и ...Металлы и сплавы -материал для древних и современных олимпийских наград
Олимпийская медаль— знак отличия за спортивные достижения в соревнованиях на Олимпийских играх. Олимпийские медали всегда были больше, чем простые ...Круговорот химических элементов в природе
Цель и задачи проекта. Цель: Задачи:. Рассмотреть круговороты веществ и взаимодействие их между собой. 1) Изучить литературу по данной теме. 2) Изучить ...Круговорот химических веществ в природе
Содержание:. Круговорот веществ Углерод в природе Круговорот углерода в природе Процессы в круговороте углерода Азот в природе Круговорот азота Круговорот ...Металлы и их соединения
Определите металл. 1. Этот металл легче свинца в 5 раз, а золота – в 20 раз. Стержень этого металла пишет по бумаге. 2. «Зелёное золото» содержит ...«Твердые тела и их свойства»
Твердые тела – тела, сохраняющие форму и объем в течение длительного времени. Аморфные тела. Кристаллические тела. Монокристаллы Поликристаллы. Кристаллические ...Аминокислоты. История их открытия
История открытия. К началу XIX столетия появляются первые работы по химическому изучению белков. Уже в 1803 г. Дж. Дальтон дает первые формулы белков ...Металлы и неметаллы
Классификация веществ по составу:. Простые вещества состоят из атомов одного химического элемента. Сложные вещества состоят из атомов разных химических ...Металлы в периодической системе
Задачи урока 28.12.2017. Повторить известное: металлическая связь, образование и характеристика. Узнать новое: положение металлов в периодической ...Металлы в жизни человека
Содержание. Цель Проблемные вопросы Гипотеза Первые металлы Металлические находки Что же такое сплавы Получение сплавов Сплавы и их свойства Использование ...Металлы
«Новогоднее Приключение Маши и Вити». Эпиграф:. «Человек не может обойтись без металлов… Если бы не было металлов, люди влачили бы самую омерзительную ...Металлы
Классификация металлов. Все металлы делятся на четыре группы: s-металлы (все s-элементы, кроме Н и Не), р-металлы (элементы гр. IIIа, кроме В, а также ...Влияние тепловой кулинарной обработки овощей и хранения их в горячем состоянии на содержание витамина С
Проблема Как при тепловой кулинарной обработке овощей и хранения их в горячем состоянии сохранить витамин С ? Цель Определить степени изменения содержания ...Вещества и их свойства
Физические тела – любые предметы, имеющие форму и объем. Например, физическими телами являются самые разнообразные предметы: алюминиевая ложка, гвоздь, ...Вещества в природе
1. Какими бывают тела по происхождению? Ответ: живые и неживые. 2. Как называются вещества без примесей? Ответ: чистые. 3. Из чего состоят вещества? ...Вещества – экорегуляторы в природе
Какие-то невидимые нити Связали воедино все вокруг. Они влекут необъяснимой силой Шмелей, жуков и бабочек на луг. Разводят врозь и сталкивают вместе ...Конспекты
Вода в природе. Потребление воды в быту и на производстве. Жесткость воды и способы его устранения. Минеральные воды, их использование столовых и лечебных целях
Тема:. . Вода в природе. Потребление воды в быту и на производстве. Жесткость воды и способы его устранения. Минеральные воды, их использование ...Общие способы получения металлов
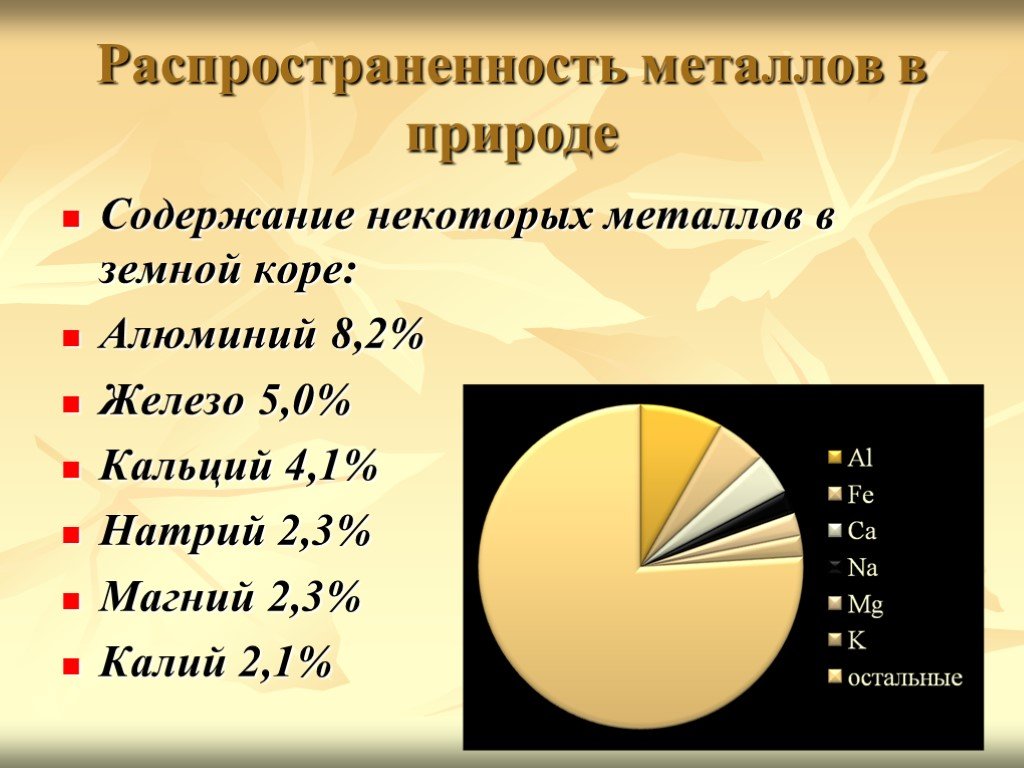
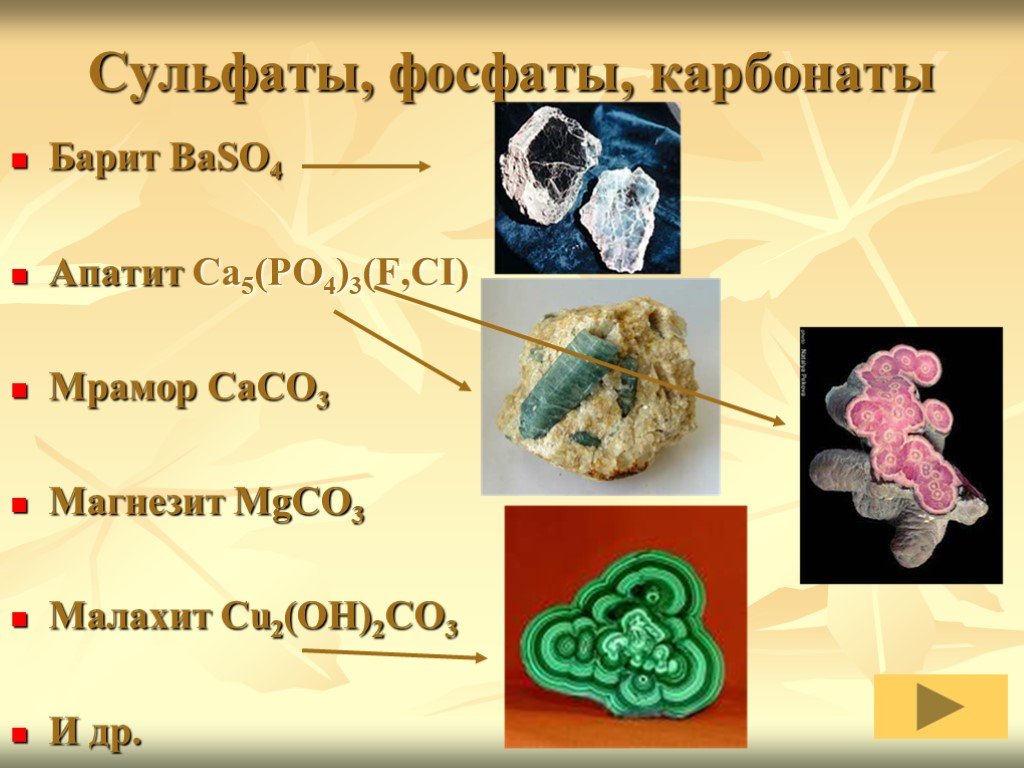
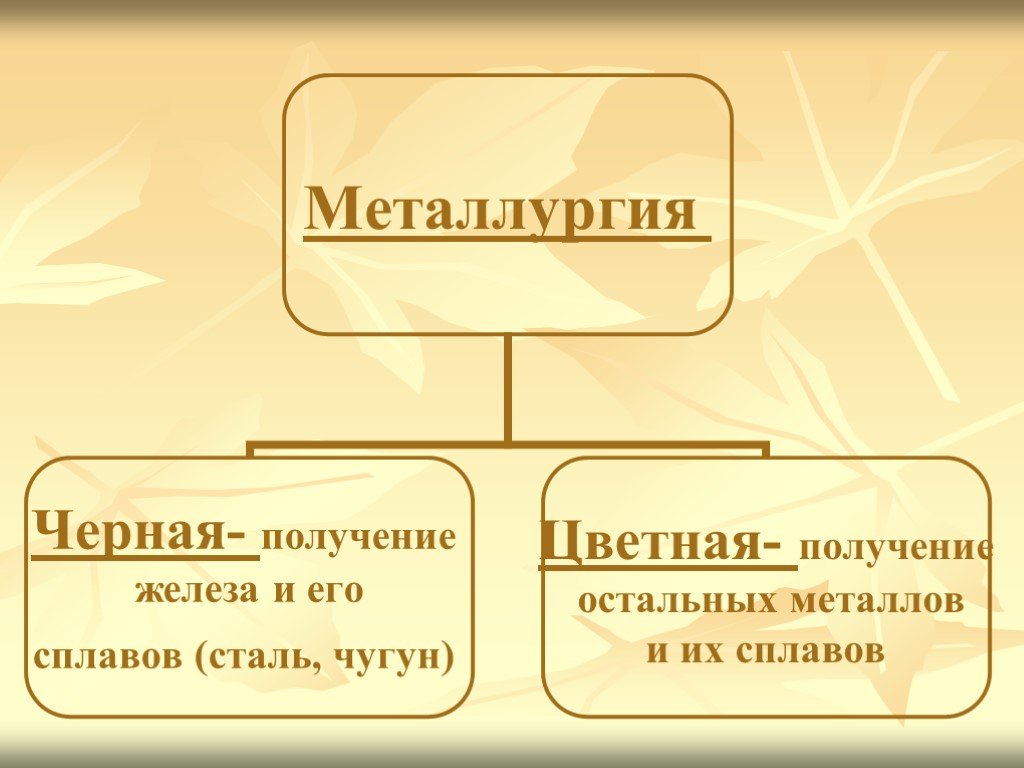
Тема:. "Общие способы получения металлов" 9-класс. Цель урока. :. познакомить с природными соединениями металлов и с самородными металлами; дать ...Понятие о металлургии. Способы получения металлов. Сплавы (сталь, чугун, дюралюминий, бронза). Проблема безотходных производств в металлургии и охрана окружающей среды
Дата_____________ Класс_______________. Тема:. Понятие о металлургии. Способы получения металлов. Сплавы (сталь, чугун, дюралюминий, бронза). Проблема ...Азотсодержащие органические соединения и их нахождение в живой природе
Рекомендации по изучению темы. «Азотсодержащие органические соединения и их нахождение в живой природе». . . 1. . Амины. . Понятие об ...Общая характеристика металлов. Металлы главных и побочных подгрупп. Щелочные металлы и их важнейшие соединения
План учебного занятия № 10. Дата Предмет. химия. группа. Ф.И.О. преподавателя. : Кайырбекова И.А. . І. Тема занятия:. Общая характеристика металлов. ...Переходные металлы и их качественные реакции
Методическая разработка урока по химии. Султанова Наталья Викторовна,. преподаватель ГБОУ СПО «Краевой политехнический колледж». г. Чернушка, ...Важнейшие классы бинарных соединений – оксиды, их роль в природе и жизни человека
Урок химии в 8 классе по теме:. «Важнейшие классы бинарных соединений – оксиды, их роль в природе и жизни человека». Цели урока:. Предметные. ...Кислоты, их состав, классификация, общие свойства
Информационный план-проспект урока. №. . Описание. . . . Тип урока. . Урок изучения нового материала с использованием химического ...Нахождение металлов в природе. Применение металлов, их значение для живых организмов
Урок химии в 9 классе. Тема: «Нахождение металлов в природе. Применение металлов, их значение для живых организмов». Цель:. Углубление знаний ...Понятие о жесткости воды и способы их устранения. Биологическая роль кальция. Генетическая связь соединений кальция
УРОК. № 35. ТЕМА УРОКА:. Понятие о жесткости воды и способы их устранения. Биологическая роль кальция. . Генетическая связь соединений кальция. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:12 декабря 2018
Категория:Химия
Содержит:22 слайд(ов)
Поделись с друзьями:
Скачать презентацию




















![Металлы в природе. Общие способы их получения. Учитель – Чуйкова Т. А. Лицей № 273 [263-489-004]. 11.12.2018 Металлы в природе. Общие способы их получения. Учитель – Чуйкова Т. А. Лицей № 273 [263-489-004]. 11.12.2018](https://prezentacii.org/upload/cloud/18/12/82599/images/thumbs/screen1.jpg)













































