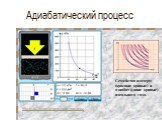
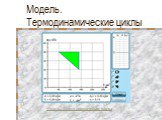
Презентация "Основы термодинамики" по физике – проект, доклад
Презентацию на тему "Основы термодинамики" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Физика. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 21 слайд(ов).
Слайды презентации
Список похожих презентаций
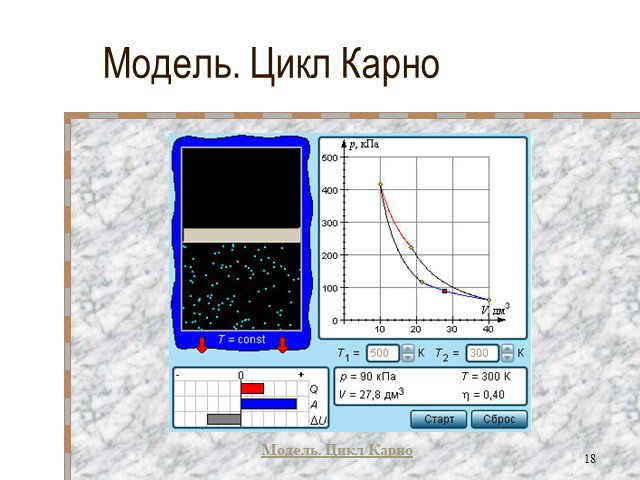
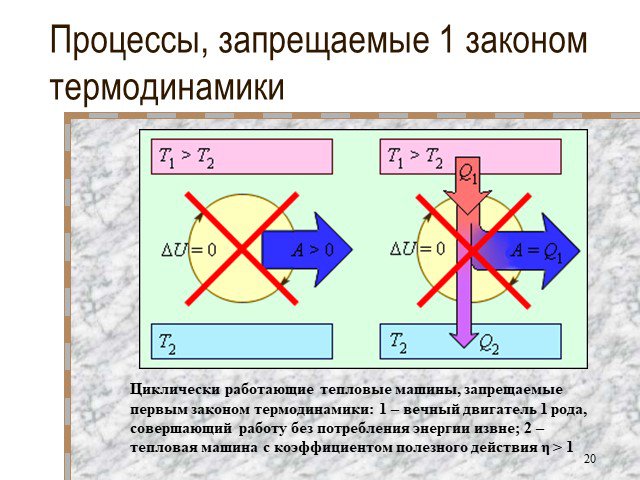
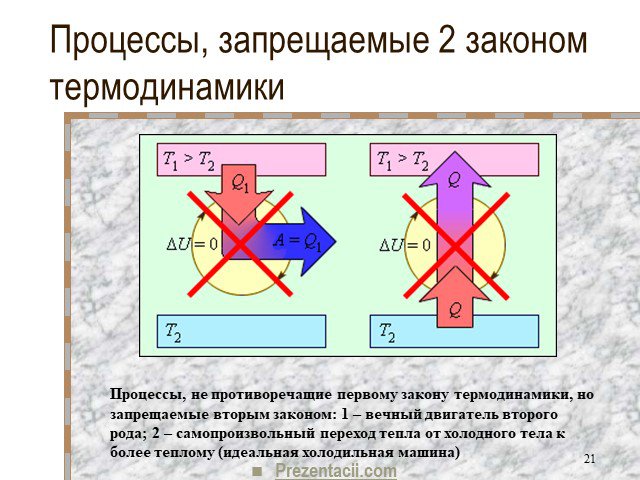
Основы термодинамики
Во всем мне хочется дойти До самой сути. В работе, в поисках пути, В сердечной смуте. « Основы термодинамики». Игра № 1. (Вопросы до 2 баллов.) 1. ...Основы термодинамики Решение задач
Цели урока:. Повторить основные формулы. Научиться применять полученные знания для решения задач. Провести анализ полученных результатов. Основные ...Основы термодинамики необратимых процессов
Основные понятия термодинамики. Термодинамическая система – совокупность тел, способных энергетически взаимодействовать между собой и с другими телами ...Основы термодинамики
Основы термодинамики Раздел физики, название которого происходит от греческих слов "терме" - "теплота" и "динамис" - "сила". Изучает он превращение ...Основы термодинамики
Цели урока:. Сформировать основные понятия термодинамики Сформулировать первый закон термодинамики Рассмотреть принцип действия тепловых двигателей ...Основы термодинамики
56 III ТЕРМОДИНАМИКА ТЕМА 5 Основы термодинамики. 1-ый закон ТД для изобарического процесса. 57 III ТЕРМОДИНАМИКА ТЕМА 5 Основы термодинамики. Исследование ...Основы телевидения
Телевидение – это передача изображения на расстояние с помощью электронных устройств. При передаче изображения формируются электрические сигналы элементов ...Основы строения вещества
Физика! Какая ёмкость слова! Физика для нас не просто звук! Физика- опора и основа Всех без исключения наук! Итак : "В некотором царстве, в некотором ...Применение первого закона термодинамики к изопроцессам
Внутренняя энергия газа зависит от температуры газа. Газ может совершать работу при любых происходящих с ним процессах. При изобарном расширении газ ...Первый закон термодинамики
Изучить закон сохранения энергии, распространённый на тепловые явления – первый закон термодинамики. Рассмотреть изопроцессы в газах с энергетической ...Первый закон термодинамики
Изменение потенциальной энергии системы равно работе, совершаемой над системой при перемещении ее из одного места силового поля в другое. Внутренняя ...Основы ядерной физики
1.1. Строение атома. Понятие радиоактивности. АТОМ – самая маленькая часть химического элемента, сохраняющая все его свойства, его размеры 10-8 см, ...Основы физики
Предмет физики. Методы физического познания: наблюдение, опыт, эксперимент, гипотеза, теория. Физика как культура моделирования. Математика и физика. ...Из истории законов термодинамики
Каждый выдающийся исследователь вносит своё имя в историю науки не только собственными открытиями, но и теми открытиями, к которым он побуждает других. ...Законы термодинамики в геологических процессах
Внутренняя энергия. 1. Согласно первому закону термодинамики, все системы, находящиеся в одном и том же состоянии, имеют одну и ту же внутреннюю энергию, ...Законы термодинамики
НУЛЕВОЕ НАЧАЛО ТЕРМОДИНАМИКИ. Нулевое начало термодинамики сформулированное всего около 50 лет назад , по существу представляет собой полученное «задним ...Законы термодинамики
Первый закон термодинамики постулирует существование внутренней энергии – некоторой функции состояния[1] , такой, что если к системе подводится тепло ...Второй закон термодинамики
1. Два положения второго закона термодинамики. Различные формы передачи энергии неравноценны. Энергия теплового движения стремиться в большей степени, ...Второй закон термодинамики
Цель занятия: знать второй закон термодинамики, принцип работы теплового двигателя. Уметь приводить примеры тепловых двигателей и определять КПД. ...Второй закон термодинамики
Обратимый процесс. Это процесс, который может происходить как в прямом, так и в обратном направлении Обратимый процесс – это идеализация реального ...Конспекты
Первое начало термодинамики
. Урок разработала:. Свириденко Ольга Владимировна – учитель физики МОУ «СОШ р.п. Красный Текстильщик Саратовского района Саратовской области». ...Первый закон термодинамики
Урок по теме «Первый закон термодинамики». 10 класс. Цели урока:. . образовательные:. ввести первый закон термодинамики как закон сохранения ...Основы молекулярно – кинетической теории
Цикл уроков физики в 10 классе. Тема: Основы молекулярно – кинетической теории (5 часов). В процессе работы над модулем вы должны изучить. :. ...Основы электродинамики
Дата. 08.10.2014. класс. 11А предмет. физика. . . Тема раздела:. Основы электродинамики(продолжение). . . . . Тема. : Явление электромагнитной ...Основы МКТ
Барышенская Е. Н. МОУ «Дубовская СОШ Белгородского района Белгородской области». . КОНТРОЛИРУЕМ ЗНАНИЯ УЧАЩИХСЯ. Барышенская Е. Н. Данный ...Основы МКТ
Разработка открытого урока по физике в 10 классе по теме «Основы МКТ». Учитель Аверина С.Г. (2011-2012 уч.год). Цель. : проверить уровень усвоения ...Основы механики
Игра. «Угадайка». по теме. «Основы механики». ( по принципу телевизионной игры «Угадай мелодию»). Правила игры:. 1,2 туры играются по нижеприведенным ...Основы кинематики и динамики
Основы кинематики и динамики. Вариант 1. Часть 1. В каком случае можно считать автомобиль материальной точкой? . 1)Автомобиль движется по ...Основы динамики Ньютона
Тематическая аттестация по физике, «Основы динамики Ньютона», 10 класс. . . Сколько вариантов зачётной работы используют преподаватели при тематической ...Исследование первого закона термодинамики к различным изопроцессам
Открытый урок по физике в 10 классе. Тема урока. «Исследование первого закона термодинамики к различным изопроцессам». Тип урока –. интегрированный, ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:15 января 2015
Категория:Физика
Содержит:21 слайд(ов)
Поделись с друзьями:
Скачать презентацию