Презентация "Современное представление о строении атома. Готовимся к ЕГЭ и ОГЭ!" по химии – проект, доклад
Презентацию на тему "Современное представление о строении атома. Готовимся к ЕГЭ и ОГЭ!" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 18 слайд(ов).
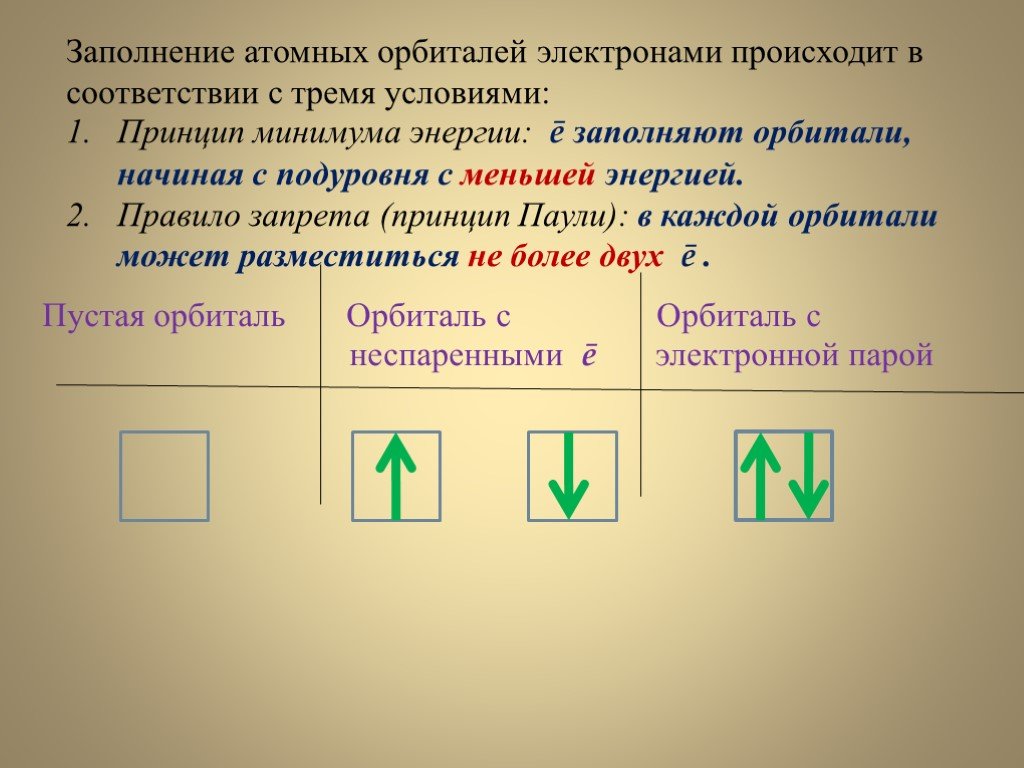
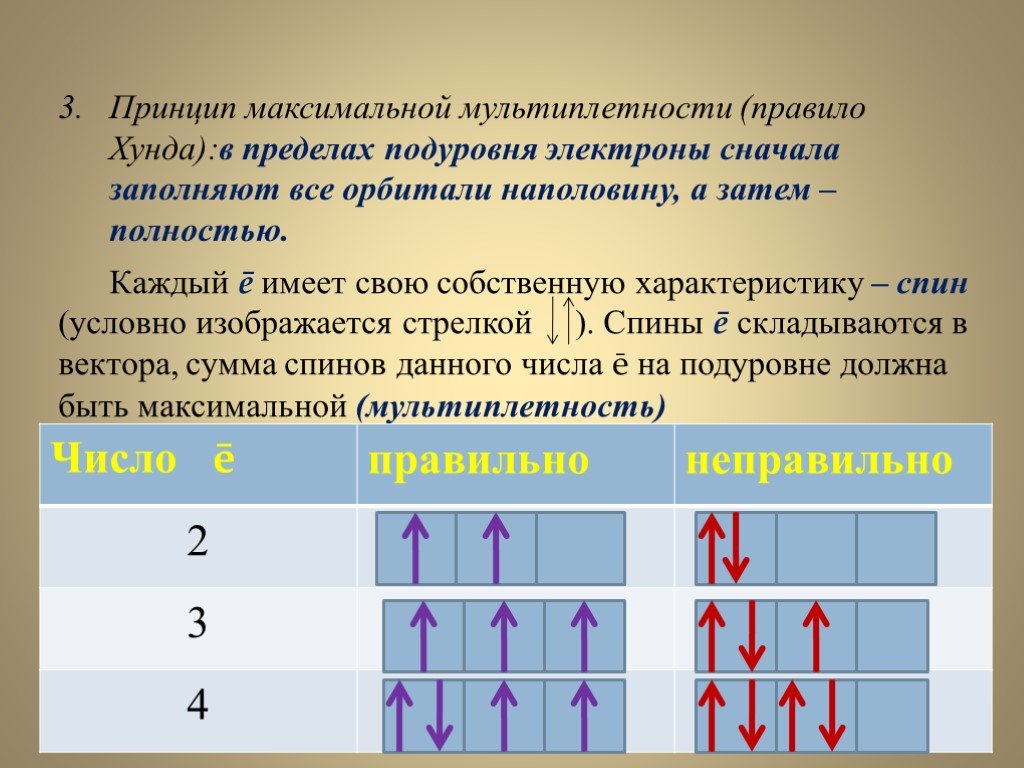
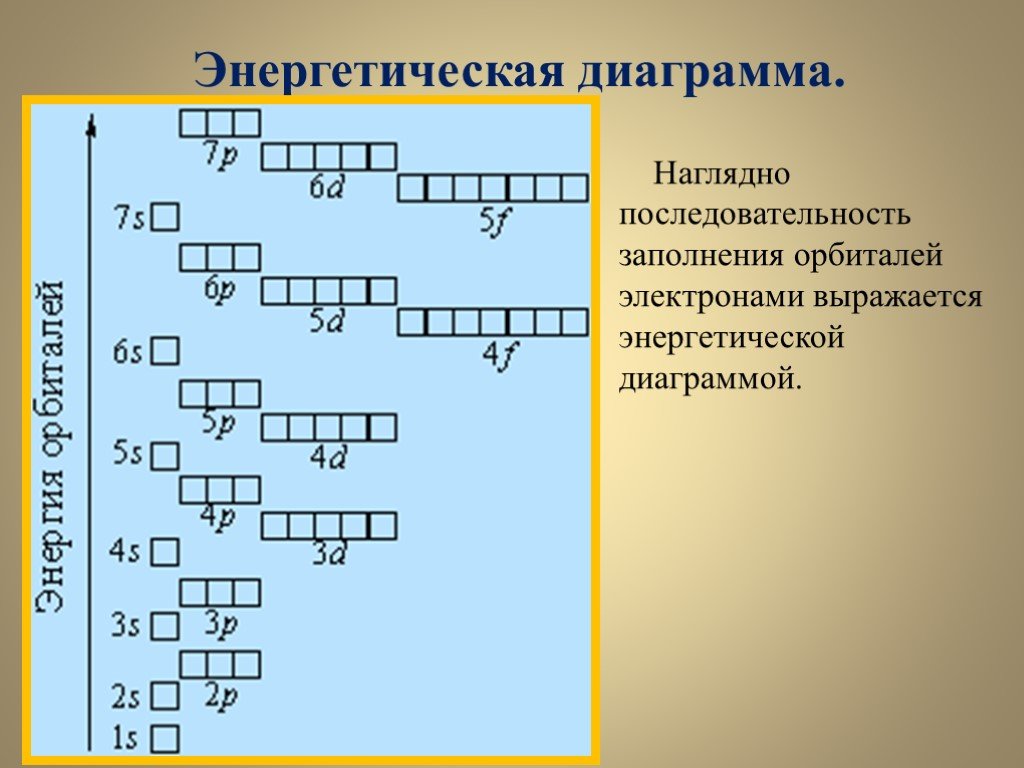
Слайды презентации
Список похожих презентаций
"Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Содержание химии очень обширно и часто предстает копилкой огромного числа формул, уравнений, фактов и законов, запомнить которые не просто трудно, ..."Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Химическая среда. Сама вода является очень слабым электролитом. При её электролитической диссоциации образуются катионы водорода и гидроксид-ионы ...Химия. Готовимся к ЕГЭ. Степень окисления.
Аннотация. Ресурс по химии адресован учащихся 8,9,11-классов для организации самостоятельной работы в период подготовки к итоговой аттестации, а также ...Основные сведения о строении атома
I вариант II вариант. 1) Запишите названия химических элементов, разделив их на металлы и неметаллы, укажите значения Аr для элементов, названия которых ...Подготовка к ЕГЭ "Строение атома"
Число электронов во внешнем электронном слое атома, ядро которого содержит 8 протонов, равно. 1) 8 2) 2 3) 6 4) 4. Число электронов в ионе железа ...Готовимся к ЕГЭ по химии
Перечень учебных пособий, разработанных с участием ФИПИ по химии. ГИА-2010. Экзамен в новой форме. Химия. 9 класс/ ФИПИ авторы составители: А.А. Каверина, ...Типичные ошибки при выполнении заданий ЕГЭ по химии
Статистические данные ЕГЭ показывают, что каждый год у выпускников возникают определенные трудности, связанные со слабым знанием одних и тех же тем. ...Текстовые задачи в ЕГЭ
№1 В 2литровый водный раствор с 60% содержанием кислоты добавили 4 л чистой воды. Определите процентное содержание кислоты в новом растворе. №1 Решение: ...Структура ячейки на примере атома железа
Периоды Группы 1 3 4 5 6 7 I II III IV V VII VIII VI малые большие А Б. Условная граница от бора до астата. Бор Кремний Мышьяк Теллур Астат Металлы ...Строение атома, химическая связь
Цель урока:. Обобщить и систематизировать знания по теме «Строения атома, химическая связь». Задание № 1 Определите химический элемент по распределению ...Строение атома углерода
↓ ↓↑. Валентность углерода IV. Валентность углерода II. Строение атома углерода. 6 С 2е4е 1S2 2S2 2P2 6 С 2е4е 1S2 2S1 2P3. Гибридизация. Гибридизация ...Строение атома
Маленькая точка, сделанная карандашом, состоит из огромного количества атомов, большего, чем количество жителей на Земле ! Демокрит. В основе философии ...Консультация экспертов ЕГЭ по химии 2012 год
С1. Cr2(SO4)3 + Br2 + NaOH = = Na2CrO4 + NaBr + Na2SO4+ H2O. 2 Cr+3 – 3e- → Cr+6 ок-е 3 Br2 + 2e- → 2Br -1 в-е. 3 6 16 8. C2-2012. Демо-2012. Соль, ...Методические рекомендации по подготовке к ЕГЭ по химии
Кодификатор. Программа элективного курса «окислительно-восстановительные реакции». H2O2 H2SO4. «окислительно-восстановительные реакции в органической ...Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам курса неорганической химии
Х И М И Ч Е С К А Я В И К Т О Р И Н А «Знаешь ли ты это? 11 класс. ТЕМА: «Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам ...Изменения в составе ядра атома
Что означают записи:. 3CO2, 2K, O2, 3O2, 4H2O, 5H2SO4, O3. Разделите указанные вещества вещества на 2 группы. Запишите с помощью химических формул. ...ЕГЭ ПО ХИМИИ
Структура части С КИМов по химии в 2006 году. С1. Окислительно-восстановительные реакции С2. Составление возможных уравнений реакций С3. Цепочки превращений ...ЕГЭ по химии
Количество участников и итоги 2011 г. В СПб Зарегистрировано - 3703 Явились - 2671 (72,1%) Неудовлетворительно – 156 чел. (5,84%) Средний балл – 54,43 ...Готовимся к экзамену по химии
Часть А. 1 2 4 5. Какое количество электронов содержит атом серы? 1)15 2)16 3)32 4)6. Число электронов в атоме равно. 1)Атомной массе 2)Порядковому ...Химическая связь и строение атома
Понятие о химической связи. Химическая связь – это связь между атомами, обеспечивающая существование веществ с четко определенным составом. При образовании ...Конспекты
Периодический закон и периодическая система в свете учения о строении атома. Характеристика химического элемента
. План урока химии. 8 класс (2 часа). Тема занятия:. . . Периодический закон и периодическая система в свете учения о строении атома. ...Основные сведения о строении атома
Урок по химии 8 класс. «Основные сведения о строении атома». Запольская Елена Николаевна учитель химии и биологии. . МБОУ «СОШ№3 г.Мамадыш». ...Основные сведения о строении атома
лицей № 9. имени заслуженного учителя школы Российской Федерации А.Н.Неверова Дзержинского района г. Волгограда. Конспект ...Основные сведения о строении атома
Унковская Светлана Андреевна. МБОУ СОШ №18 г.Ставрополь. учитель химии. Тема урока: «Основные сведения о строении атома». Цель урока. ...Состав и строение атома
Тема: Состав и строение атома. Образовательная. : сформировать представления о строении атома; дать понятие протон, электрон, нейтрон. Развивающая. ...Современное состояние и охрана воздуха
Тема: Современное состояние и охрана воздуха, 9 класс. (интегрированный урок по химии и биологии). Учитель химии и биологии высшей кв. категории ...Путешествие в мир атома
Конспект урока химии в 8 классе. Учитель Сергеева Галина Борисовна. Тема урока « Путешествие в мир атома». Цель: изучение основных сведений о ...Периодическая система химических элементов Д.И.Менделеева и строение атома
Тема:. Повторение и обобщение знаний по теме: «Периодическая система химических элементов Д.И.Менделеева и строение атома». Цель:. . повторить ...Азот. Строение атома и молекулы, свойства простого вещества
Тема урока. «. Азот. Строение атома и молекулы, свойства простого вещества. » 9-й класс. . Цель урока:. . . изучение строения атома и молекулы ...Строение атома
Урок по теме: «Строение атома». Задачи урока:. Образовательные. : сформировать представления о строении атома; дать понятие протон, электрон, ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:8 ноября 2018
Категория:Химия
Содержит:18 слайд(ов)
Поделись с друзьями:
Скачать презентацию






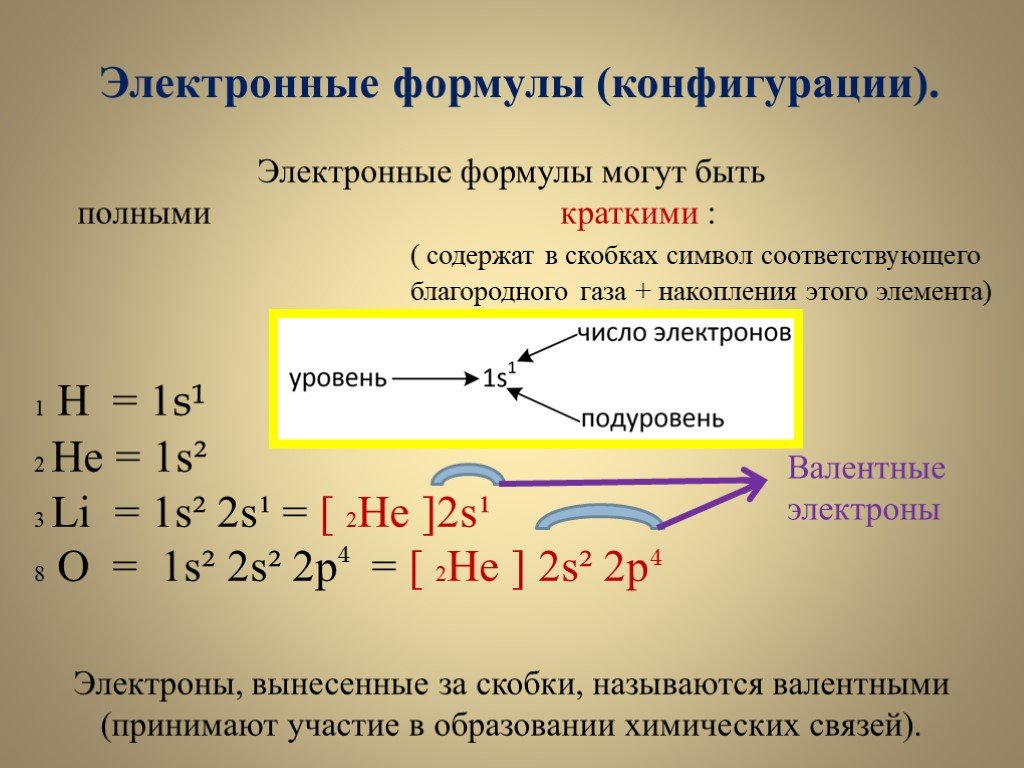
















![Электронные формулы (конфигурации). Электронные формулы могут быть полными краткими : ( содержат в скобках символ соответствующего благородного газа + накопления этого элемента). 1 Н = 1s¹ 2 He = 1s² 3 Li = 1s² 2s¹ = [ 2He ]2s¹ 8 O = 1s² 2s² 2p = [ 2He ] 2s² 2p. 4. Электроны, вынесенные за скобки, н Электронные формулы (конфигурации). Электронные формулы могут быть полными краткими : ( содержат в скобках символ соответствующего благородного газа + накопления этого элемента). 1 Н = 1s¹ 2 He = 1s² 3 Li = 1s² 2s¹ = [ 2He ]2s¹ 8 O = 1s² 2s² 2p = [ 2He ] 2s² 2p. 4. Электроны, вынесенные за скобки, н](https://prezentacii.org/upload/cloud/18/11/98672/images/thumbs/screen13.jpg)



































