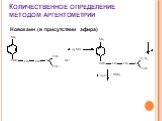
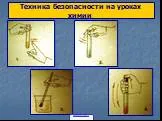
Презентация "Методы количественного анализа, применяемые в фармацевтической химии" – проект, доклад
Презентацию на тему "Методы количественного анализа, применяемые в фармацевтической химии" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 45 слайд(ов).
Слайды презентации
Список похожих презентаций
Методы обучения химии
Урок – это зеркало общей и педагогической культуры учителя, мерило его интеллектуального богатства, показатель его кругозора и эрудиции. В. Сухомлинский. ...Методы познания химии
09.09.2018. Метод (от греческого слова «методос» — путь к чему-либо) означает совокупность приемов и операций практического и теоретического освоения ...Подготовка к олимпиадам по химии
ЦЕЛИ ТУРНИРА:. ВЫЯВИТЬ НАИБОЛЕЕ ПОДГОТОВЛЕННЫХ УЧАЩИХСЯ, ИМЕЮЩИХ ОСОБЫЕ СПОСОБНОСТИ И СКЛОННОСТИ К ПРЕДМЕТУ ХИМИЯ. ПОДДЕРЖАТЬ И РАЗВИТЬ ПОЗНАВАТЕЛЬНЫЕ ...Предмет органической химии
Органические вещества. Вещества. Органические Получены из продуктов жизнедеятельности рас- тительных и животных Организмов (сахар, жи- ры, масла, ...Основные понятия и законы химии
стратегия успеха. посещение, работа на лабораторных занятиях и своевременное оформление отчетов. посещение, восприятие и записывание материала лекций. ...Открытия в химии
Химия. одна из важнейших и обширных областей естествознания наука о веществах, их свойствах строении и превращениях, происходящих в результате химических ...Техника безопасности на уроках химии
(Писатель – фантаст и учёный – биохимик Айзек Азимов ). «Химия – это смерть, упакованная в банки и коробки». школьник, помни ты всегда, Знай, любая ...«Своя игра» по химии
Необходим в составе костей скелета. Меню. Лечебные элементы 20. Дезинфектор ран. Лечебные элементы 40. Избыток ионов этого элемента может вызвать ...Безопасность на уроке химии
Пробовать вещества на вкус, есть и пить в химическом кабинете. Осторожно направляйте к себе газ рукой. ЗАПРЕЩАЕТСЯ. . . . . ЗАПРЕЩАЮЩИЕ ЗНАКИ. Запрещается ...Роль органической химии в жизни человека
Органические вещества. Одни органические вещества известны человеку многие десятки лет, другие находятся на стадии изучения, а третьи только еще ...Анализ ЕГЭ по химии 2011
Уровни выполнения экзаменационной работы. неудовлетворительный – 0–31 / 0–12, удовлетворительный –32–56 / 13–35, хороший – 57–77 / 36–56, отличный ...Анализ результатов ЕГЭ по химии 2010 (окружной семинар учителей химии)
Результаты ЕГЭ 2010. Граница минимального балла -33 тестовых балла (12 первичных баллов). Уровни оценивания: неудовлетворительный – 0–32 / 0–11; удовлетворительный ...Алгоритм решения задач по химии
Алгоритм решения задач по химии:. Записать краткое условие задачи; *В случае необходимости произвести предварительный расчет; Перевести величины, ...Активизация обучающихся на уроках химии как показатель развития их мыслительной деятельности.
Приёмы активизации мыслительной деятельности обучающихся:. Приём стимулирующих звеньев Приём реконструкции Приём прогнозирования. Приём стимулирующих ...Азотная кислота по химии
Тема: «Азотная кислота» Цель урока: Рассмотреть свойства азотной кислоты и области ее применения. План урока: 1. Проверка Д/З (письменная работа); ...Применение ИКТ на уроке химии при изучении темы «Соли».
Проект урока по теме «Соли». Комбинированный урок- практикум. Цели урока:. Знать классификацию солей. Уметь доказывать химические свойства солей, ...Великие учёные, внёсшие значительный вклад в развитие химии
Дмитрий Иванович Менделеев. Родился в Тобольске в семье директора гимназии. После окончания гимназии он поступил в Главный педагогический институт ...Путешествие по континенту Химия, познавательная игра по химии, 8 класс
“Наши знания не могут иметь конца именно потому, что предмет познания бесконечен” (Паскаль). Государство № 1 «Врата учёности». Ответ Be N Si Al P ...Вещество в химии
Сегодня мы начинаем изучать одну из самых древних из важных наук- химию. А что же изучает химия? Химия – это наука о веществах, их свойствах и превращениях. ...Сложные вопросы ЕГЭ по химии
«Чтобы избегать ошибок, надо набираться опыта; чтобы набираться опыта, надо делать ошибки». С1. Используя метод электронного баланса, составьте уравнение ...Конспекты
Основы химического анализа
Муниципальное образование. . «Ленский район». Конспект урока для 9 класса. «Основы химического анализа. ». . ...Школьный кабинет химии
Урок-экскурсия «Школьный кабинет химии». Цели мероприятия:. Предметная:. познакомить с новой наукой - химией, что она изучает;. Методологическая:. ...Белки. На перекрестках химии и биологии
Урок в 10 классе «Белки. На перекрестках химии и биологии». Цель урока:. систематизация и углубление знаний учащихся по теме «Белки». Образовательные ...Решение экспериментальных задач по органической химии
Конспект открытого урока . Практическая работа №4 «Решение экспериментальных задач по органической химии». Класс:10. УМК: Рудзитис Г.Е., ФельдманФ.Г. ...Тренировка памяти на уроках химии
. Муниципальное бюджетное общеобразовательное учреждение. «Основная общеобразовательная школа №6». г.Топки Кемеровской области. Мастер-класс ...Предмет органической химии
Муниципальное бюджетное общеобразовательное учреждение. Орловская средняя общеобразовательная школа №3. Открытый урок. по теме «Предмет ...Развитие познавательной самостоятельности на уроках химии через составление химических задач
Развитие познавательной самостоятельности на уроках химии через составление химических задач. «Не мыслям надо учить, а мыслить…». . И.Кант. ...Использование опорных схем на уроках химии
Муниципальное образовательное автономное учреждение средняя общеобразовательная школа с углубленным изучением отдельных предметов №1 г. Белогорск, ...Лабораторные опыты по неорганической химии (свойства кислот, оснований, солей)
III. . . . Технологическая карта урока. ЭТАПЫ УРОКА. ДЕЯТЕЛЬНОСТЬ УЧИТЕЛЯ. . ДЕЯТЕЛЬНОСТЬ УЧЕНИКА. . 1.Организационный. . момент. ...Именные реакции в органической химии
Урок обобщения: "Именные реакции в органической химии" 10 класс. Максимова И.Н. учитель химии и биологии. . МБОУ «Среднекибечская СОШ» Канашского ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:25 августа 2018
Категория:Химия
Содержит:45 слайд(ов)
Поделись с друзьями:
Скачать презентацию






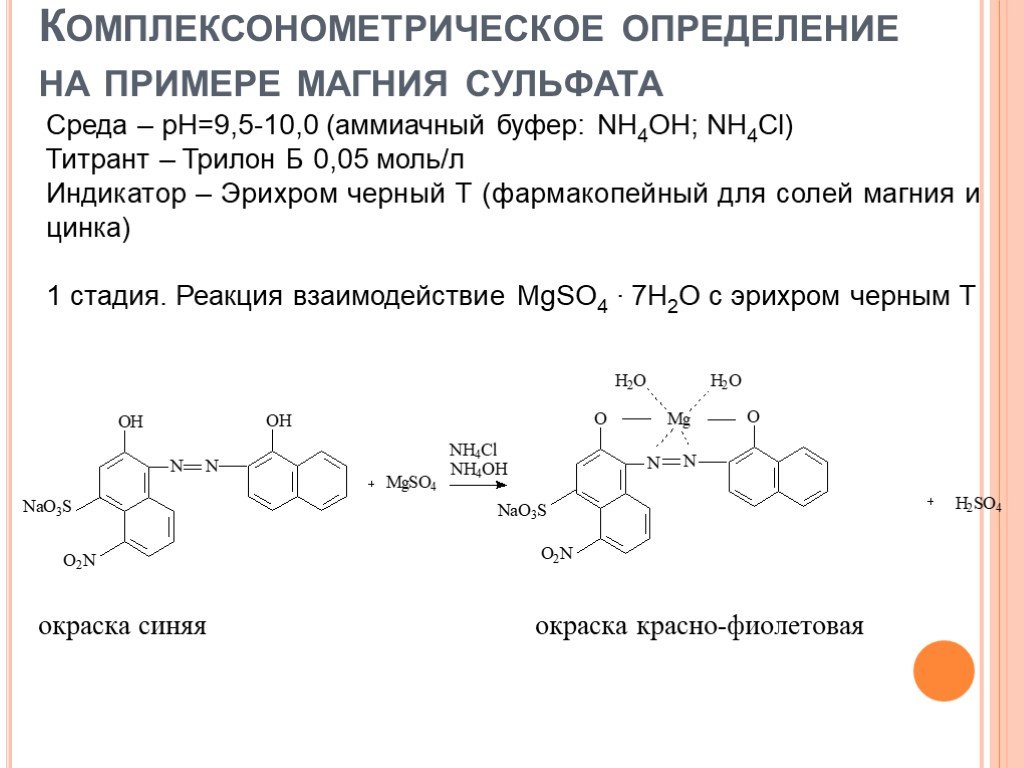
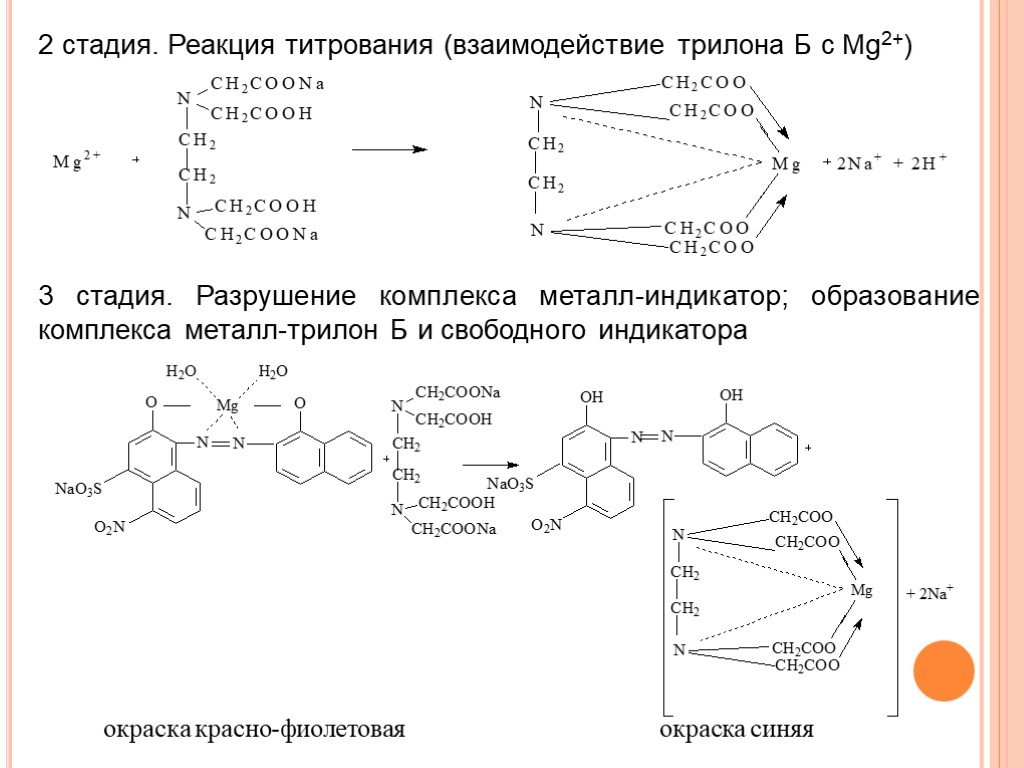




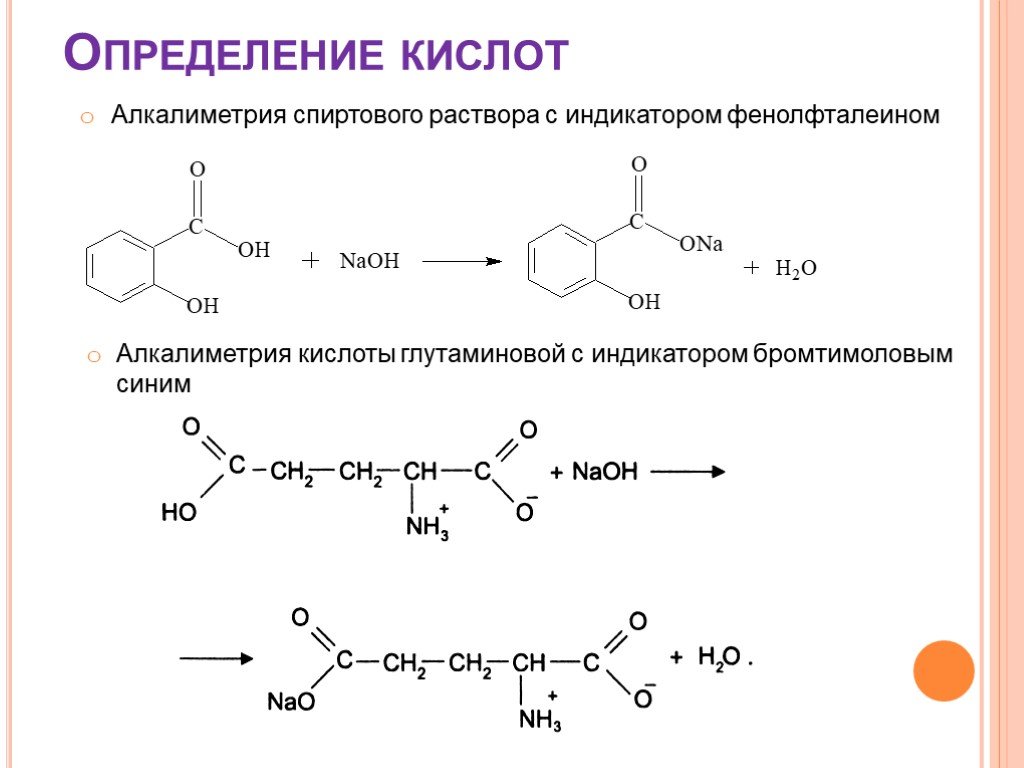
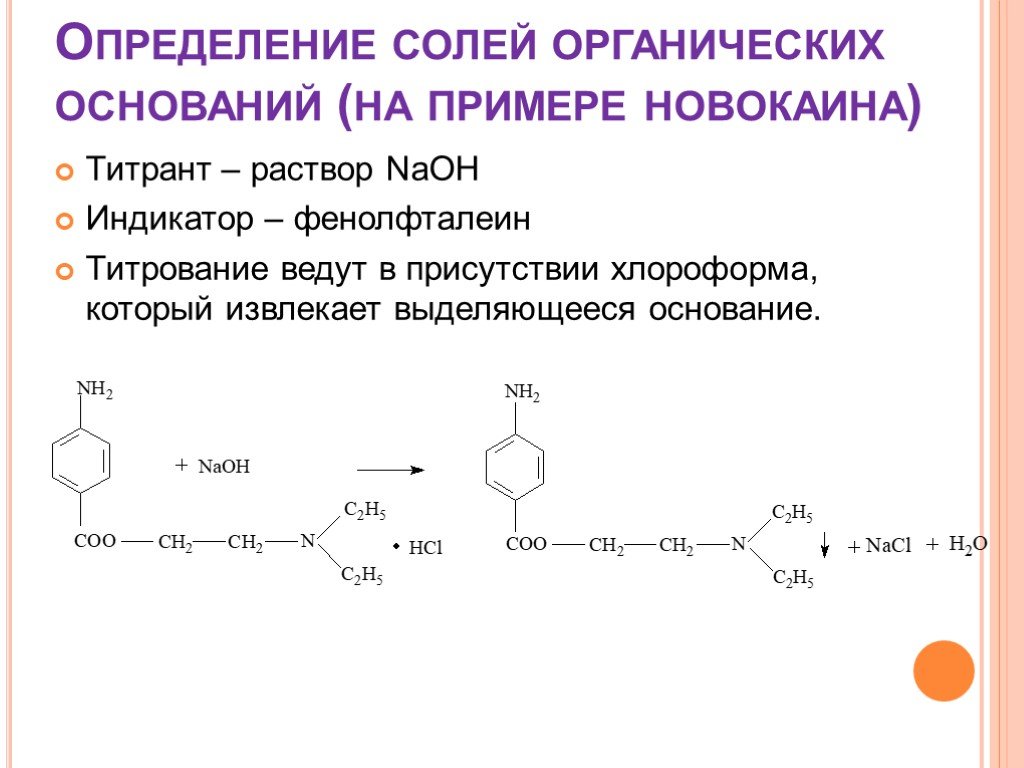
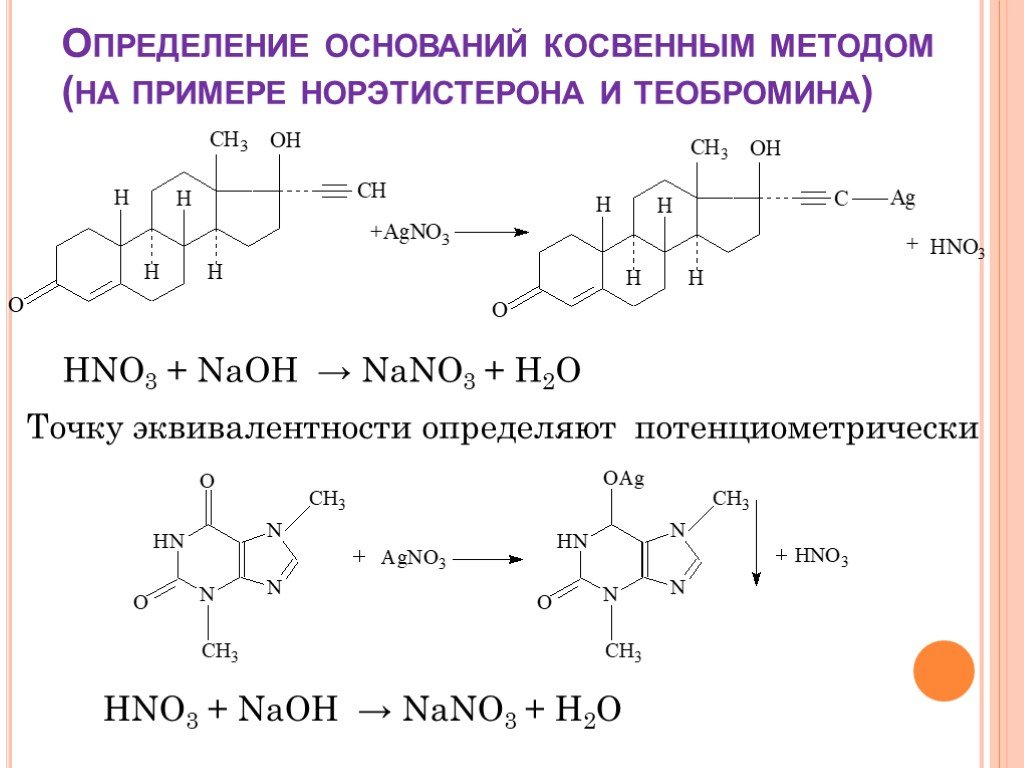
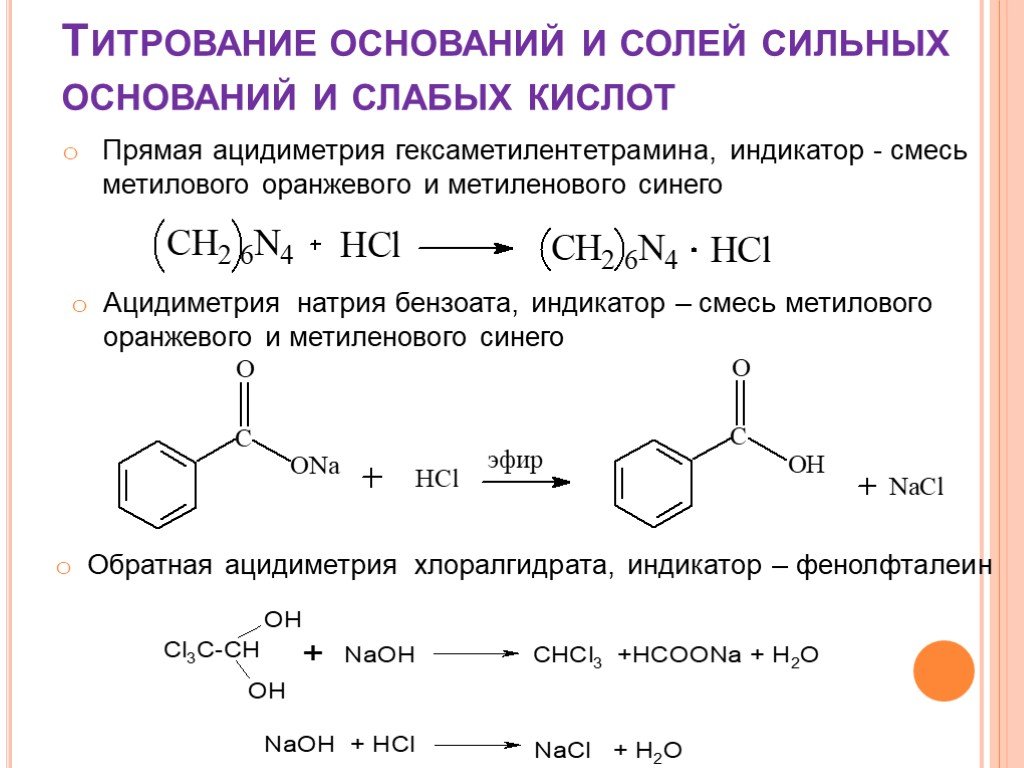


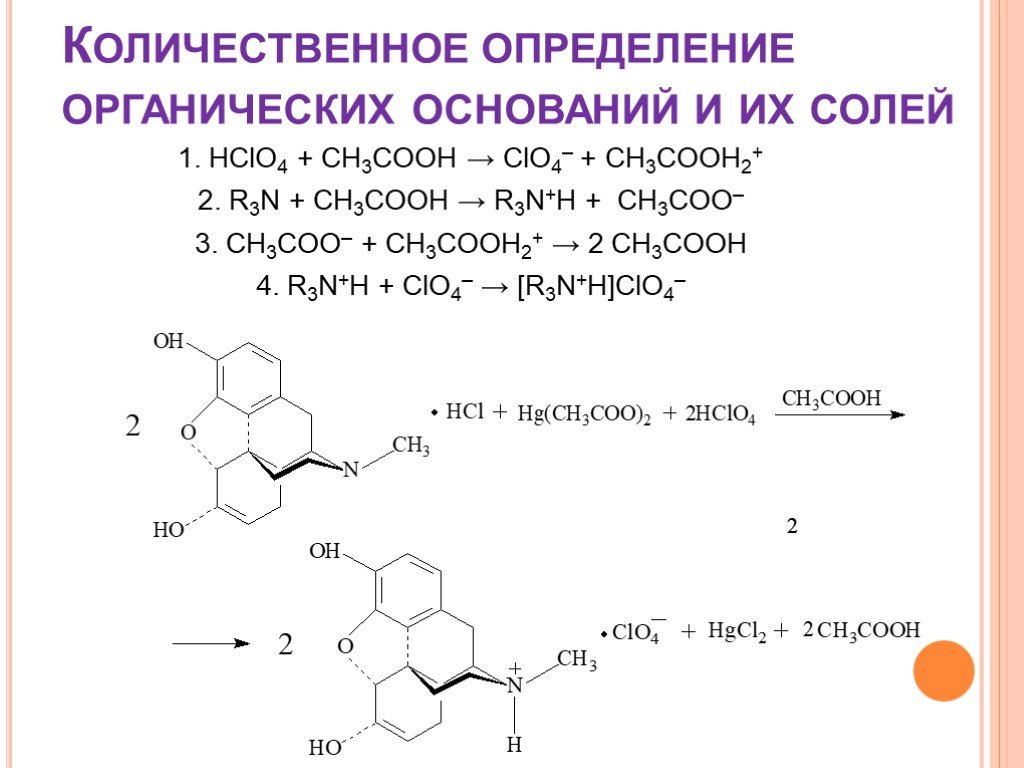
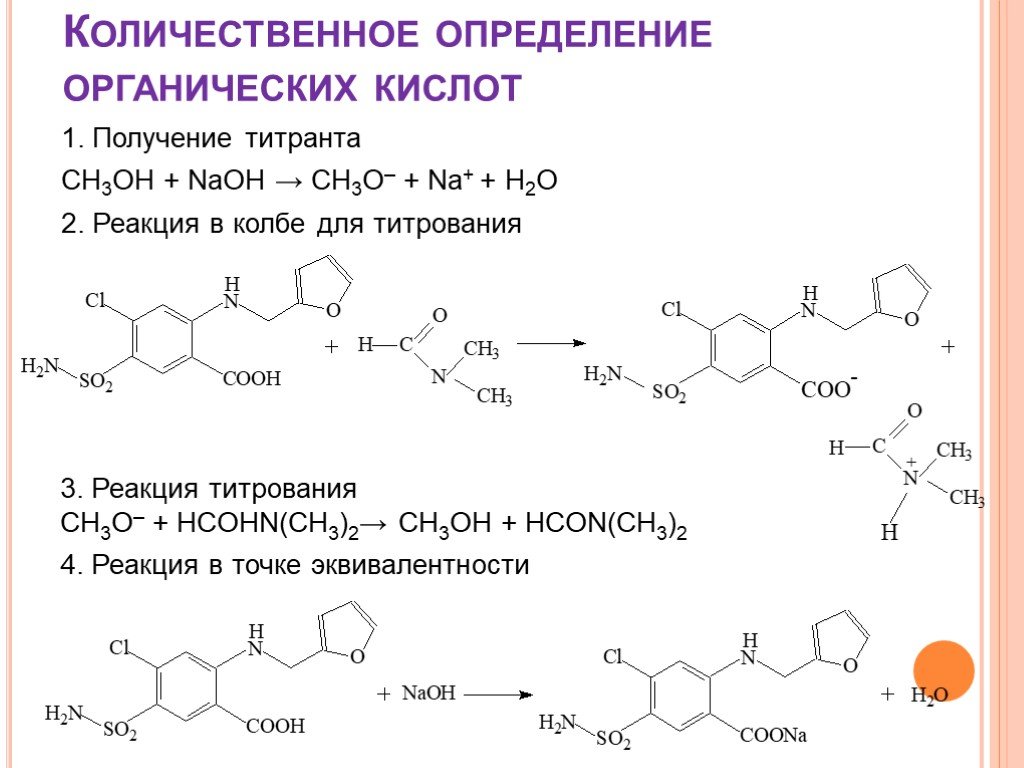



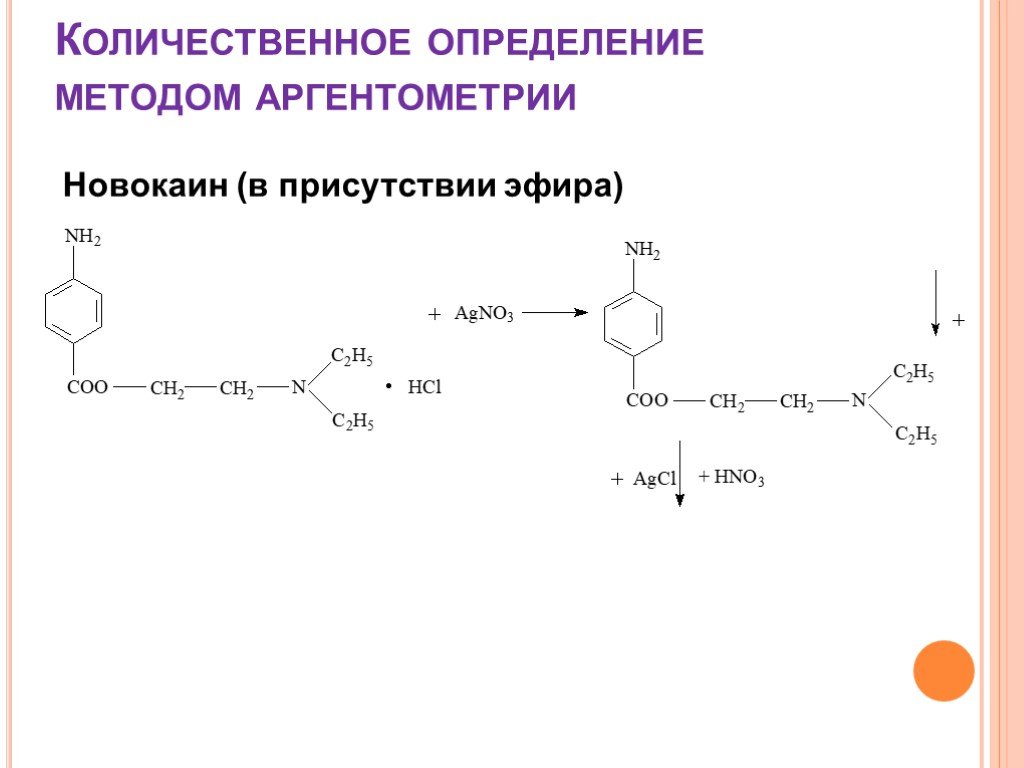






















![Количественное определение органических оснований и их солей. 1. HClO4 + CH3COOH → ClO4– + CH3COOH2+ 2. R3N + CH3COOH → R3N+H + CH3COO– 3. CH3COO– + CH3COOH2+ → 2 CH3COOH 4. R3N+H + ClO4– → [R3N+H]ClO4– Количественное определение органических оснований и их солей. 1. HClO4 + CH3COOH → ClO4– + CH3COOH2+ 2. R3N + CH3COOH → R3N+H + CH3COO– 3. CH3COO– + CH3COOH2+ → 2 CH3COOH 4. R3N+H + ClO4– → [R3N+H]ClO4–](https://prezentacii.org/upload/cloud/18/08/70716/images/thumbs/screen19.jpg)