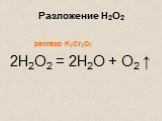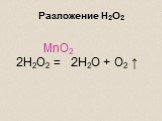Презентация "Скорость химических реакций" по химии – проект, доклад
Презентацию на тему "Скорость химических реакций" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 30 слайд(ов).
Слайды презентации
Список похожих презентаций
Скорость химических реакций
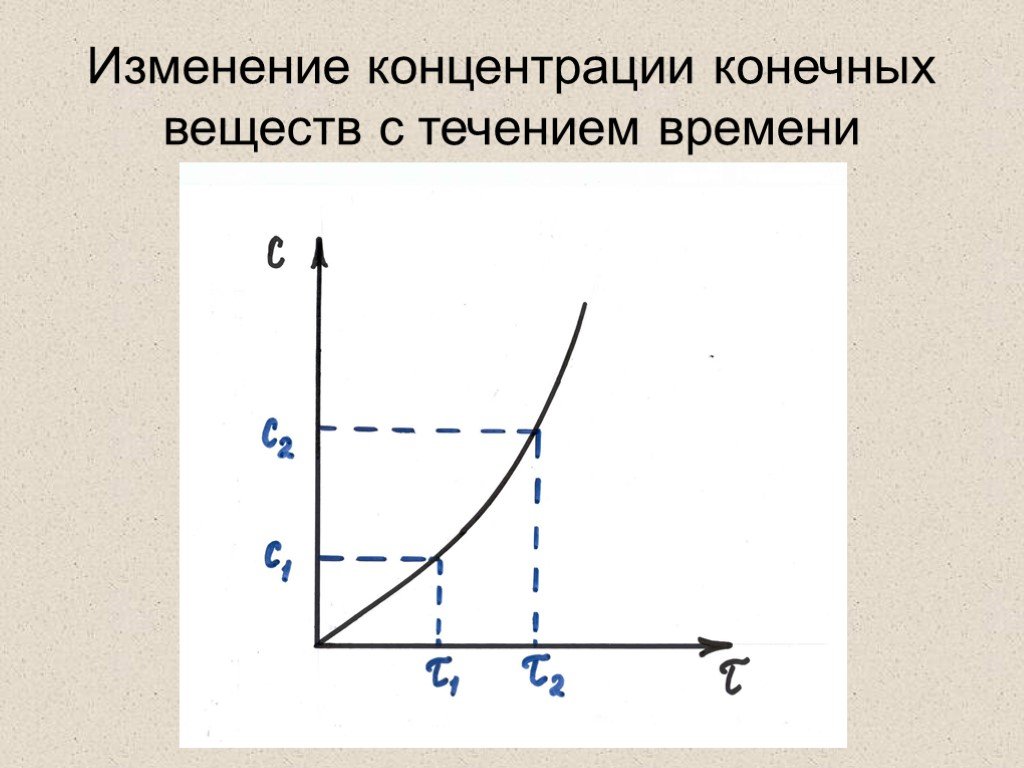
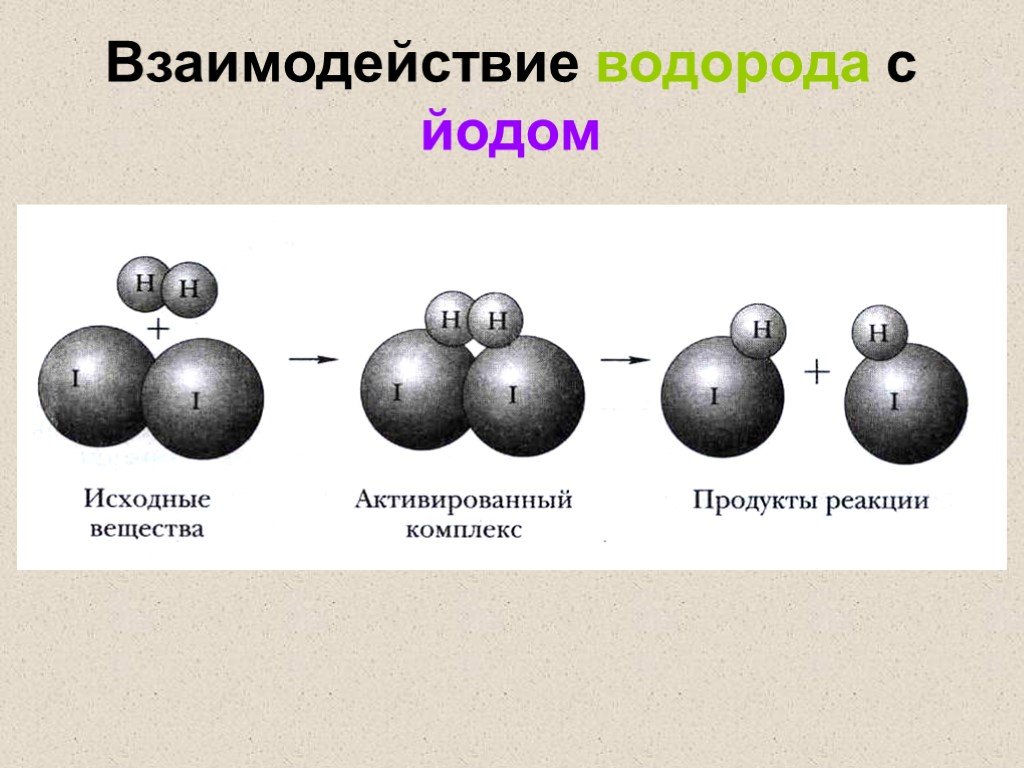
Для гомогенных реакций. Скорость химической реакции- это изменение концентрации одного из реагирующих веществ или одного из продуктов реакции в единицу ...Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Обсудим следующие вопросы:. Зачем нужны знания о скорости химических реакций? Какими примерами можно подтвердить то, что химические реакции протекают ...Скорость химических реакций
Определение:. Скорость химической реакции – это изменение количества реагирующего вещества в единицу времени в единице объёма. r – скорость химической ...Скорость химических реакций
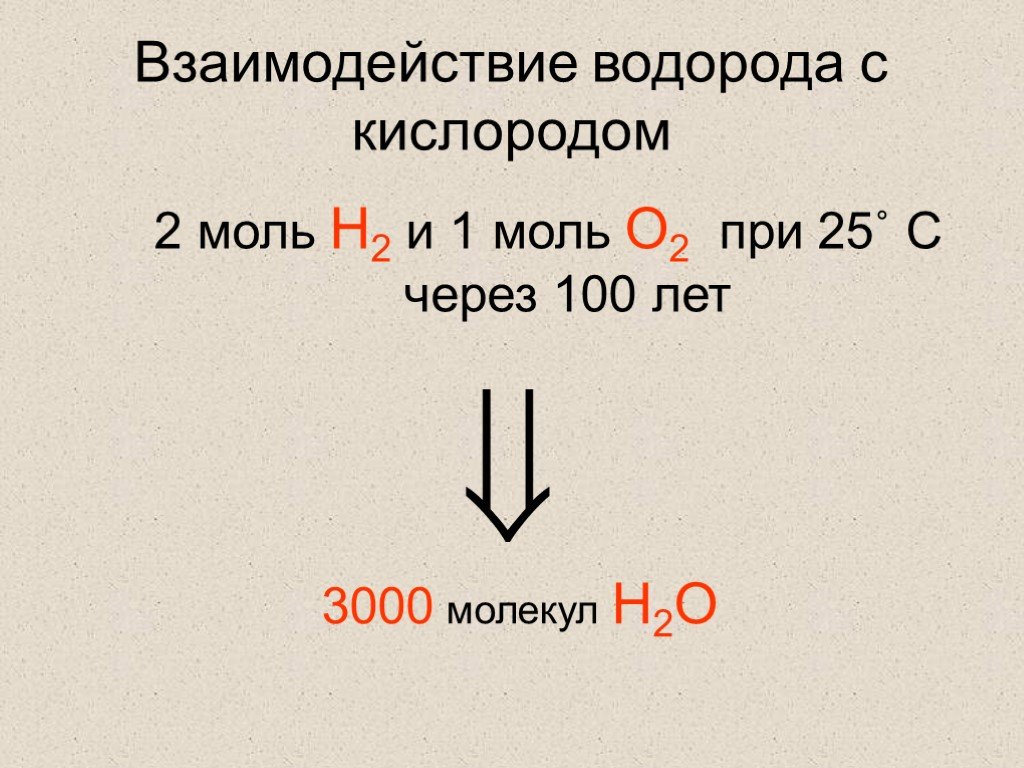
Химические реакции протекают с разными скоростями. Очень быстро проходят реакции в водных растворах, практически мгновенно. Скорость гомогенной реакции ...Скорость химической реакции. Факторы влияющие на скорость химических реакций
КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИИ ПО ПРИЗНАКУ ФАЗНОСТИ (АГРЕГАТНОЕ СОСТОЯНИЕ). ХИМИЧЕСКИЕ РЕАКЦИИ. ГОМОГЕННЫЕ ГЕТЕРОГЕННЫЕ. (реагирующие вещества и ...В мире химических реакций
Классификация химических реакций по числу и составу реагирующих веществ реакции. « …Мы отнюдь не властвуем над природой, все наше господство состоит ...Cкорость химических реакций
Определение:. Скорость химической реакции – это изменение количества реагирующего вещества в единицу времени в единице объёма. r – скорость химической ...«Систематизация и обобщение знаний по теме «Типы химических реакций»»
1) Что называют химической реакцией? 2) По каким признакам можно утверждать, что произошла или происходит химическая реакция? 3) Какие условия необходимы ..."Типы химических реакций
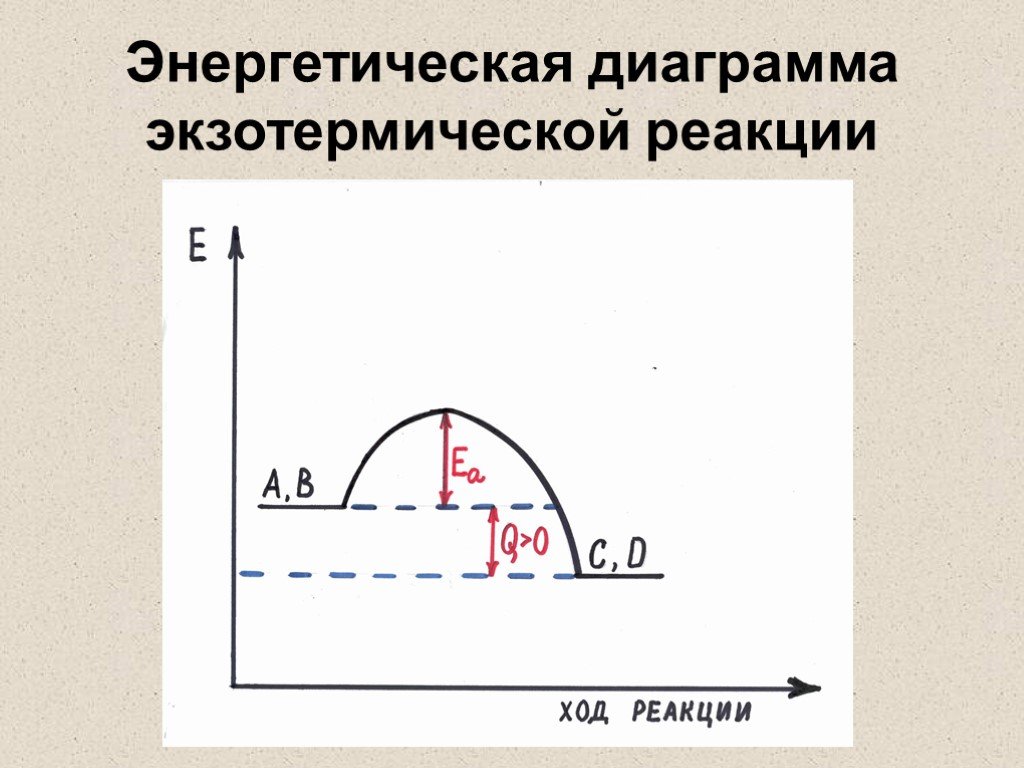
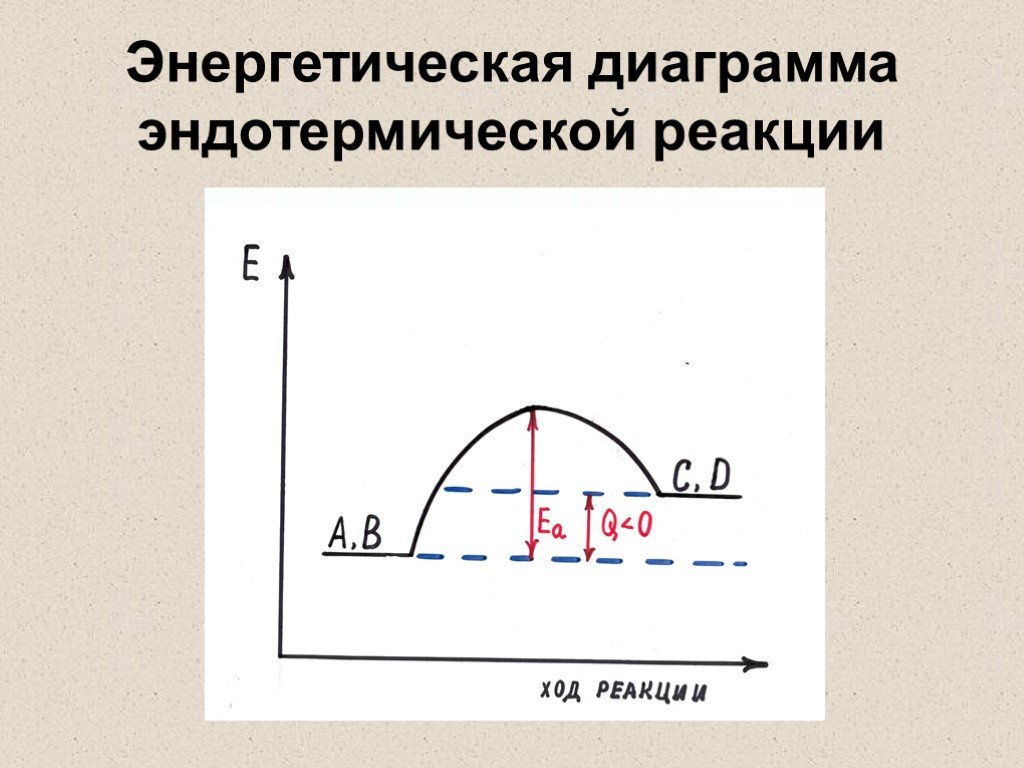
ЦЕЛЬ УРОКА:. ПОВТОРИТЬ И ОБОБЩИТЬ ЗНАНИЯ УЧАЩИХСЯ О ХИМИЧЕСКИХ ПРЕВРАЩЕНИЯХ, ПРИЗНАКАХ И ТИПАХ ХИМИЧЕСКИХ РЕАКЦИЙ. ЗАКРЕПИТЬ НАВЫКИ СОСТАВЛЕНИЯ ХИМИЧЕСКИХ ..."Тепловой эффект химических реакций
Явления природы Физические Химические. Химические явления – химические реакции. Химическая реакция – процесс превращения одних веществ в другие. 2Н2 ...Закон сохранения массы веществ. Уравнения химических реакций
Единственный путь, ведущий к знанию, - это деятельность. Цели урока: Обучающие - экспериментально доказать закон сохранения массы веществ. На основе ...Урок-путешествие в страну химических реакций
Химия – наука чудес и превращений. Девиз: « Знание только тогда знание, когда оно приобретено усилиями своей мысли, а не одной памятью.» Л.Н. Толстой. ...Химия. Классификация химических реакций
По числу и составу исходных и образовавшихся веществ:. Реакции разложения Реакции соединения Реакции замещения Реакции обмена. РЕАКЦИЯ РАЗЛОЖЕНИЯ. ...Уравнения химических реакций
Составьте схемы химических реакций Сульфат натрия + хлорид бария → хлорид натрия + сульфат бария Азот + кислород → оксид азота (V) Алюминий + … → ...Решение задач по уравнениям химических реакций
Основные физические величины. 8 класс. 1. Нахождение количества одного вещества по количеству другого вещества: ν1 → ν2. Дано: ν (O2) = 4 моль Найти: ...Уравнения химических реакций
Представители педагогической науки. А.В.Дистервег /29.10.1790 – 07.07.1866/. В.А.Сухомлинский /28.09.1918 – 02.09.1970/. К.Д.Ушинский /19.02.1824 ...Типы химических реакций на примере свойств воды
Вода Сложное вещество, состоящее из двух химических элементов. Является оксидом. Молекулярная формула воды Формула воды - Н2О В молекуле воды: 2 атома ...Классификация химических реакций
Пособие составила: учитель химии Людмила Александровна Гапиенко. (Электронное пособие для учителей и учащихся средней школы). Классификация химических ...Классификация химических реакций в органической и неорганической химии
Цели урока: обобщить представления о химической реакции как о процессе превращения одного или нескольких веществ в другие вещества; рассмотреть классификацию ...Классификация химических реакций
Химические реакции - это. процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и строению. Классификация. ...Конспекты
Скорость химических реакций. Химическое равновесие
Обобщение знаний по теме «Скорость химических реакций. Химическое равновесие». Цель:. Обобщение теоретических знаний учащихся о скорости химической ...Скорость химических реакций. Факторы, влияющие на скорость реакций
Скорость химических реакций. Факторы, влияющие на скорость реакций. 9 класс. Урок-исследование. Деятельностная цель:. освоение методов исследовательской ...Факторы, влияющие на скорость химических реакций
Озёрная средняя школа. Разработка урока по химии. Тема урока: «Факторы, влияющие на скорость химических реакций». 10 класс. Автор: Горбач ...Факторы, влияющие на скорость химических реакций
МОУ Судиславская средняя общеобразовательная школа Судиславского муниципального района Костромской области, учитель химии Кабанова Н.Н. . Урок химии ...Факторы, влияющие на скорость химических реакций
Калиничева Екатерина Антоновна –. учитель химии высшей квалификационной категории КГУ «Средняя школа №5» г. Петропавловск,. Северо-Казахстанская ...Признаки химических реакций
Признаки химических реакций. Николаева Валентина Геннадьевна, учитель химии 2 категории, СОШ№28, г. Нижнекамск РТ. Цель:. . познакомить учащихся ...Явления физические и химические. Признаки химических реакций
Итоговая работа. Явления физические и химические. Признаки химических реакций. . . Цель:. . 1. Сформировать представление учащихся о физических ...Решение задач по уравнениям химических реакций
Северо-Казахстанская область, Уалихановский район, Бидайыкская средняя школа. Учитель: Иманова Асель Нурмухамедовна. Предмет: химия. Класс: ...Скорость химических реакции
Сабақ жоспары №. 6. План учебного занятия. Күні Пән. химия. тобы. Дата Предмет группа. Оқытушының Т.Ә.А. Қайырбекова И. А. . Ф.И.О. преподавателя. ...Химические реакции. Признаки химических реакций
Тема: Химические реакции. Признаки химических реакций. Тип урока. : изучение нового материала и первичного закрепления знаний. Вид урока. : ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:24 июня 2018
Категория:Химия
Содержит:30 слайд(ов)
Поделись с друзьями:
Скачать презентацию




































![Механизм действия катализаторов. Для гомогенного катализа: K A + B = AB A + K = [AK] [AK] + B = AB + K Механизм действия катализаторов. Для гомогенного катализа: K A + B = AB A + K = [AK] [AK] + B = AB + K](https://prezentacii.org/upload/cloud/18/06/57892/images/thumbs/screen27.jpg)