"Урок химии в 10 классе" презентация, проект, доклад
Презентацию на тему "Урок химии в 10 классе" (10 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 9 слайд(ов).
Слайды презентации
Список похожих презентаций
План – конспект урока химии в 9-ом классе
Тема:. Общие химические свойства металлов. Цель:. Систематизировать сведения о химических свойствах металлов Осознать химическую функцию металлов ...Азот урок химии
ЦЕЛИ :. Сформировать представление о строении атома и молекулы азота. Рассмотреть физические и химические свойства азота в свете ОВР. Показать значение ...Активизация обучающихся на уроках химии как показатель развития их мыслительной деятельности.
Приёмы активизации мыслительной деятельности обучающихся:. Приём стимулирующих звеньев Приём реконструкции Приём прогнозирования. Приём стимулирующих ...10 класс Урок химии "Белки
Белки – биоорганические полимеры, образованные аминокислотами; имеют строго определенные элементарный состав и пространственную структуру. Белки - ...Метод проекта на уроках химии и биологии и внеурочное время
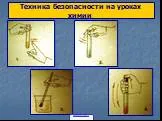
Вовлечённый в исследовательскую деятельность ребёнок находится на пути продвижения от незнания к знанию, от неумения к умению, то есть осознаёт смысл ...Техника безопасности на уроках химии
Enter. . Не трогайте вещества, посуду и не приступайте к работе без разрешения учителя! Вещества нельзя проверять на вкус! При выяснении запаха веществ ...Контроль знаний на уроках химии
Элементы и атомы, В менделеевский взятые круг Сделали химию самой богатой И самой творческой из наук. Г.Санников. Kонтроль результатов обучения учащихся ...Применение интерактивной доски на уроках химии
«Что вам интересно на уроках химии?». На протяжении года изучения химии с использованием возможностей интерактивной доски позволило в большей мере ...Проблемное обучение как средство реализации компетентностого подхода на уроках химии
Проблемное обучение - это комплекс технологий, способствующих развитию прямого (исследовательского) опыта получения новых знаний, и , как следствие, ...Применение современных приемов, форм ,методов обучения и оценки знаний на уроках химии
Урок-упражнение по теме: Основные классы неорганических веществ. Типы химических реакций. 8 класс. Приемы педагогической техники, разработанные Анатолием ...Использование разнообразных форм и средств контроля за качеством образования на уроках химии
В.Д.Шаталов утверждал, что для того, чтобы работа в школе была эффективной, должен сработать «эффект соленого огурца». Главное – создать рассол, тогда ...Безопасность на уроке химии
Пробовать вещества на вкус, есть и пить в химическом кабинете. Осторожно направляйте к себе газ рукой. ЗАПРЕЩАЕТСЯ. . . . . ЗАПРЕЩАЮЩИЕ ЗНАКИ. Запрещается ...Использование информационных технологий на уроках химии
Цель: становление профессиональной компетентности учителя химии в области применения ИКТ в процессе обучения химии в школе. Задачи: 1. Формирование ...Повышение эффективности уроков химии через активизацию познавательной деятельности учащихся
Теория развития познавательного интереса Г.И .Щукиной. Ценность познавательного интереса заключается в том, что: 1) от него зависит не только продуктивность ...Витамины. Урок химии
Витамины (в переводе с латинского «необходимые для жизни») – это органические вещества, которые являются незаменимыми компонентами нашего питания. ...Использование ИКТ на уроках химии
Современный урок должен быть. интересным, познавательным, обязан учитывать интересы учащихся, оставлять некоторую недосказанность и побуждать к творчеству, ...Организация самостоятельной работы учащихся на уроках химии
Кабинет химии. «Обучая других, мы учимся сами». Сенека. “ТО, ЧТО Я СЛЫШУ, Я ЗАБЫВАЮ, ТО, ЧТО Я ВИЖУ, Я ПОМНЮ, ТО, ЧТО Я ДЕЛАЮ, Я ПОНИМАЮ”. КОНФУЦИЙ. ...Организация и содержание профильного обучения на уроках химии
Исследовательская деятельность школьников в процессе обучения химии в профильных классах. Переход к профильному обучению в старших классах предъявляет ...Использование интерактивных обучающих заданий на уроках химии
электронные издания. Видеофрагмент «Разложение дихромата аммония». Вопросы к демонстрации. Что вы наблюдаете? Какое вещество вступает в реакцию? Какие ...Использование ИКТ на уроках химии
В своей педагогической деятельности использую технологию развивающего обучения, направленную на обеспечение личности гимназиста. При данной технологии ...Конспекты
АМИНОКИСЛОТЫ. Урок химии в 11 классе
АМИНОКИСЛОТЫ. Урок химии в 11 классе, 2010г. Учитель МОУ СОШ №26: Андреева Галина Анатольевна. Цель урока:. . . Дать понятие об аминокислотах ...Тренировка памяти на уроках химии
. Муниципальное бюджетное общеобразовательное учреждение. «Основная общеобразовательная школа №6». г.Топки Кемеровской области. Мастер-класс ...Игра как средство развития школьников на уроках химии
Игра как средство развития школьников на уроках химии. . Мы прекрасно знаем, что играть любят не только дети, но и взрослые. Главная задача моей ...методическая разработка урока по химии
Муниципальное бюджетное общеобразовательное учреждение. « Средняя общеобразовательная школа села Алексеевка ». Базарно – Карабулакского района Саратовской ...Развитие познавательной самостоятельности на уроках химии через составление химических задач
Развитие познавательной самостоятельности на уроках химии через составление химических задач. «Не мыслям надо учить, а мыслить…». . И.Кант. ...Развитие интеллекта и творческих способностей учащихся на уроках химии
Перед современной школой стоит задача воспитания грамотного, продуктивно мыслящего человека, адаптированного к условиям жизни в обществе. Проблема ...Использование опорных схем на уроках химии
Муниципальное образовательное автономное учреждение средняя общеобразовательная школа с углубленным изучением отдельных предметов №1 г. Белогорск, ...Развитие речи учащихся на уроках химии
Развитие речи учащихся на уроках химии. . «Изучая средства выражения,. . мы изучаем выражаемое.». Л.В.Щербы. Опыт работы в школе ...Урок чистой воды
Химия – 8,9 классы. 17.11.2010. Тема: «Урок чистой воды». Цели урока:. . 1. Обобщить и систематизировать знания учащихся о воде,. акцентируя ...Предмет органической химии
Муниципальное бюджетное общеобразовательное учреждение. Орловская средняя общеобразовательная школа №3. Открытый урок. по теме «Предмет ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:24 июня 2018
Категория:Химия
Классы:
Содержит:9 слайд(ов)
Поделись с друзьями:
Скачать презентацию