Презентация "Химия наука о веществах и их превращениях" – проект, доклад
Презентацию на тему "Химия наука о веществах и их превращениях" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 16 слайд(ов).
Слайды презентации
Список похожих презентаций
Биохимия как наука
Биохимия может быть определена как химия живых объектов (клеток и организмов). Структуры живых объектов обычно образуются из простых неорганических ...Виды химической связи в неорганических веществах
Знать. определение понятия химическая связь, виды химической связи, механизмы образования каждого вида связи. Уметь. определять вид связи по формуле ...Нефть, состав и свойства. Переработка нефти. Нефтепродукты, их применение.
Залежи нефти находятся в недрах Земли на разной глубине, где нефть заполняет свободное пространство между некоторыми породами. Сегодня нефть является ...Многоатомные Спирты и их строение
Глицерин (пропантриол-1,2,3) - простейший представитель трёхатомных спиртов. Представляет собой вязкую прозрачную жидкость, очень гигроскопична, смешивается ...Неметаллы и их характеристика
Разгадайте ребусы и назовите три химических элемента названия которых здесь зашифрованы:. уГ+лес,Т=Д , газ + , ,,,+. К какой группе относятся эти ...Кислородные соединения азота и их свойства
Цель урока:. Расширить, обобщить, закрепить, оценить знания по теме: «Кислородные соединения азота» Повторить свойства азотной кислоты Закрепить особенности ...Металлы в природе. Общие способы их получения
Распространенность металлов в природе. Содержание некоторых металлов в земной коре: Алюминий 8,2% Железо 5,0% Кальций 4,1% Натрий 2,3% Магний 2,3% ...Карбоновые кислоты и их производные
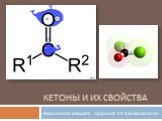
Функциональные производные карбоновых кислот. Образование сложных эфиров R'–COOR":. Реакция образования сложного эфира из кислоты и спирта называется ...Кетоны и их свойства
Строение кетонов. Кетоны - органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами. Общая формула ...Нитраты, их влияние на организм человека
Цель работы. Изучить литературу о нитратах и нитритах, овладеть методикой их определения, определить содержание нитратов и нитритов в разных сортах ...Закономерности измененияхимических свойств элементови их соединений по периодам и группам
1. Учебный тренажер содержит 20 заданий В-1 с кратким ответом. 2. Задание считается выполненным верно, если правильно указана последовательность цифр. ...Ароматические эфирные масла и их использование
Объект исследования:. Ароматические эфирные масла. Предмет исследования:. влияние ароматических масел на организм человека; эфирные масла – натуральные ...Биополимеры и их структурные компоненты
«жизнь – это особая форма существования биополимерных тел (систем), характеризующихся хиральной чистотой и способностью к самоорганизации и саморепликации ...Аминокислоты. История их открытия
История открытия. К началу XIX столетия появляются первые работы по химическому изучению белков. Уже в 1803 г. Дж. Дальтон дает первые формулы белков ...Альдегиды и их свойства
Содержание Строение молекул Изомерия и номенклатура Физические свойства Получение Химические свойства Применение Контрольные вопросы. Альдегиды – ...Алкины и их свойства
Непредельные углеводороды с тройной связью С=С в молекулах. Простейший представитель ряда – ацетилен С2Н2, общая формула СnH2n-2 (n>2). Атомы углерода ...Активизация обучающихся на уроках химии как показатель развития их мыслительной деятельности.
Приёмы активизации мыслительной деятельности обучающихся:. Приём стимулирующих звеньев Приём реконструкции Приём прогнозирования. Приём стимулирующих ...Азотные удобрения и их роль
Роль азота в жизни растений. Азот - важнейший питательный элемент для всех растений. Он входит в состав таких важных органических веществ как белки, ...«Циклоалканы, их строение. Свойства циклоалканов.»
Цель: Изучить строение, состав, физические свойства и тип гибридизации электронных облаков атома углерода в циклоалканах. Общая формула - СnH2n. Циклоалканы ...Вещества и их свойства
Физические тела – любые предметы, имеющие форму и объем. Например, физическими телами являются самые разнообразные предметы: алюминиевая ложка, гвоздь, ...Конспекты
Общие представления об органических веществах
IX. класс. . Тема: «ОБЩИЕ ПРЕДСТАВЛЕНИЯ. ОБ ОРГАНИЧЕСКИХ ВЕЩЕСТВАХ». (Урок изучения нового материала). Форма урока:. рассказ учителя и демонстрация ...Спирты, их строение, номенклатура, физические и химические свойства спиртов
Тема:. «Спирты, их строение, номенклатура, физические и химические свойства спиртов». . Цели. :. Знать строение, номенклатуру, физические и химические ...Соли в свете теории электролитической диссоциации, их свойства
Предмет – химия. Класс – 8. Тема урока: «Соли в свете теории электролитической диссоциации, их свойства». Тип урока: урок изучения нового ...Решение экспериментальных задач по теме «Металлы и их соединения
Дата_____________ Класс_______________. Тема:. Практическая работа №6 «Решение экспериментальных задач по теме «Металлы и их соединения»». . ...Природные источники углеводородов. Нефть и природный газ, их применение. Защита атмосферного воздуха от загрязненияПриродные источники углеводородов. Нефть и природный газ, их применение. Защита атмосферного воздуха от загрязнения
Дата_____________ Класс_______________. Тема:. Природные источники углеводородов. Нефть и природный газ, их применение. Защита атмосферного воздуха ...Предмет химии. Вещества и их свойства
Цели урока:. Обучающая:. сформировать представление о предмете химии. Дать первоначальные понятия о веществе, химическом элементе, о простых ...Положение неметаллов в периодической системе химических элементов Д.И. Менделеева, строение их атомов, физические свойства. Аллотропия
Тема:Положение неметаллов в периодической системе химических элементов Д.И. Менделеева, строение их атомов, физические свойства. Аллотропия. Цели ...Положение галогенов в периодической таблице Д.И. Менделеева и строение их атомов
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ. «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА №39. ИМЕНИ П. Н. САМУСЕНКО». Положение ...Вода в природе. Потребление воды в быту и на производстве. Жесткость воды и способы его устранения. Минеральные воды, их использование столовых и лечебных целях
Тема:. . Вода в природе. Потребление воды в быту и на производстве. Жесткость воды и способы его устранения. Минеральные воды, их использование ...Валентность. Определение валентности элементов по формулам их соединений
Урок химии в 8 –м классе по теме:. «Валентность. Определение валентности элементов по формулам их соединений». Цели урока. Дидактические:. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Неизвестен
Содержит:16 слайд(ов)
Поделись с друзьями:
Скачать презентацию