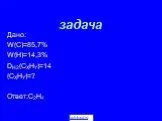
Презентация "Класс Алкины" по химии – проект, доклад
Презентацию на тему "Класс Алкины" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 23 слайд(ов).
Слайды презентации
Список похожих презентаций
Алкины и их свойства
Непредельные углеводороды с тройной связью С=С в молекулах. Простейший представитель ряда – ацетилен С2Н2, общая формула СnH2n-2 (n>2). Атомы углерода ...Класс Алкены
Тема урока: Непредельные углеводороды. Этилен Строение Получение Свойства Применение. Девиз урока: Все познается в сравнении. Цели и задачи урока. ...Алкины
алкин НС СН Н3С С СН. Общая формула алкинов. CnH2n-2. Номенклатура алкинов. Дайте названия углеводородам:. Н3С С С СН3 Этин Бутин - 2 Пропин. Строение ...Алкины
Алкины. Алкины — алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна тройная связь. СnН2n-2. Строение ...Алкины
План 1.Повторение пройденного: а)Рассказ о строении и свойствах алкенов по плану упр.2. б)Решение задачи: Рассчитать объем этилена, полученный дегидрированием ...Алкины
Сегодня на уроке вы узнаете:. Понятие о непредельных углеводородах. Характеристика тройной связи. Изомерия и номенклатура алкинов. Физические свойства. ...Алкины
АЛКИНЫ. Студент должен: знать стоение, номенклатуру, свойства, способы получения и применения алкинов умень составлять названия и химические уравнения ...Класс спиртов
Спирты́ (от лат. spiritus — дух; устар. алкого́ли) — органические соединения, содержащие одну или более гидроксильных групп (гидроксил, −OH), непосредственно ...Алкины
Ацетиленовые углеводороды. Ацетиленовыми углеводородами (алкинами) называются непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну ...Алканы, Алкены, Алкины
АЛКАНЫ. Получение, нахождение в природе и применение алканов. ВПЕРЕД НАЗАД. Газообразные алканы получают из природного и попутного нефтяных газов; ...Органическая химия А.А.Карцовой и А.Н.Лёвкина
. H3C-O-CH3 CH3-CH2-CH3 6 C УГЛЕРОД 12,011. Основные классы органических веществ. H2C=CH─CH2─CH3 HC≡C─CH2─CH3 H2C=CH─CH=CH2 CH3─CH2─OH CH3─CH2─NH2 ...Органические вещества химия
Органическая химия – это дремучий лес, в который и не отважишься войти. Фридрих Велер. С глубокой древности человечество использовало для удовлетворения ...Органическая химия
ФЕНОЛЫ. 2. Классификация и изомерия Как и спирты, фенолы бывают одноатомные (одна -OH) и многоатомными (несколько -OH). Для фенолов характерна изомерия ...Органическая химия
Цель: уяснить знания о предмете изучения и особенностях органической химии. Широко распростирает химия руки свои в дела человеческие … куда ни посмотрим, ...Токсикологическая химия
Токсикологическая химия. Токсикологическая химия – это наука о химических превращениях токсических веществ и их метаболитов в организме, методах их ...«Задачи» химия
- исследование задач по нанонауке; - ознакомление с наномиром: о достижениях нанохимии и нанотехнологии; - составление задач по нанонауке; - решение ...Коррозия металла химия
Цель презентации. В этой презентации мы рассмотрим процесс коррозии металлов как окислительно-восстановительную реакцию. Изучим : что такое коррозия; ...Сера химия
Сера принадлежит к числу веществ, известных человечеству испокон веков. Ещё древние греки и римляне нашли ей разнообразное практическое применение. ...Интересная химия
Введение:. Химия – удивительная наука. С одной стороны, она очень конкретная и имеет дело с бесчисленными полезными и вредными веществами вокруг нас ...Коллоидная химия
3 Пособия. Лекции, конспекты практических занятий. Фридрихсберг Д.А. Курс коллоидной химии. Л., «Химия». 1984. 368 с. Сумм Б.Д. Коллоидная химия. ...Конспекты
Непредельные углеводороды. Алкины
"Непредельные углеводороды. Алкины". (урок химии в 10 классе, учитель химии Артамонова О.А. МБОУ СОШ №12 г.Камышин, Волгоградской обл.). Цель ...Алкины
Муниципальное бюджетное общеобразовательное учреждение. Средняя общеобразовательная школа №6. Тема:. «Алкины». 10 класс. Ханты-Мансийский ...Генетическая связь между классами неорганических соединений 11 Класс
Генетическая связь между классами неорганических соединений. Урок в 11 классе. Девиз : «Величие человека в его способности мыслить»,. Цель :. ...Алкины
Открытый урок в 10 классе по теме «Алкины». Составил учитель химии 1 квалификационной категории Шуклина Оксана Валерьевна, МБОУ СОШ № 4, г. Можги ...Алкины
5. . . Разработка открытого урока. . по химии в 11 классе МОУ СОШ № 65. Красноармейского района Волгограда. Учитель: Недожогина Е.С. ...Алкины
5. . . Разработка открытого урока. . по химии в 10 классе. . Тема урока: «Алкины». Цели: образовательные:. в сказочно – игровой форме ...Алкины
Урок:. . Тема урока: Алкины. Цели урока:. 1. Расширить знания учащихся о непредельных углеводородах-. познакомить с ацетиленом и его гомологами. ...Алканы, Алкены, Алкины
Урок химии: обобщение знаний по темам «Алканы»,. . «Алкены, «Алкины». Викторова Екатерина Петровна. ГБОУ СОШ с. Новокуровка. Учитель химии ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:4 декабря 2018
Категория:Химия
Содержит:23 слайд(ов)
Поделись с друзьями:
Скачать презентацию