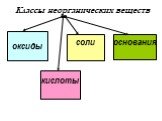
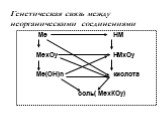
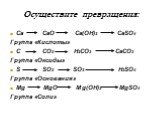
Презентация "Неорганические вещества" по химии – проект, доклад
Презентацию на тему "Неорганические вещества" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 48 слайд(ов).
Слайды презентации
Список похожих презентаций
Химическая организация клетки. Неорганические вещества
Вещества клетки Неорганические Органические Вода Минеральные соли белки жиры углеводы. Элементы клетки микроэлементы биоэлементы макроэлементы H, ...Простые вещества - неметаллы
Цели урока:. 1)Познакомить учащихся с простыми веществами – неметаллами; 2)изучить практическое значение неметаллов; 3)продолжить формирование знаний ...Простые вещества
Задачи урока: Развитие навыков решения задач с использованием понятия «количество вещества» Систематизация знаний по теме: «Простые вещества». Запишите ...Поверхностно-активные вещества
Пове́рхностно-акти́вные вещества. Пове́рхностно-акти́вные вещества́ (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела ...Органические вещества в клетке
Цели:. Изучить особенности строения и функций белков, нуклеиновых кислот – органических веществ, составляющих основу всего живого на Земле. 1. Все ...Чистые вещества и смеси
Цели урока:. Выяснить, какое вещество считают чистым. Что такое смесь? Какие бывают смеси? Выяснить различия между смесью и химическим соединением. ...Химические вещества и материалы
Химия и искусство имеют внутреннюю общность, которая коренится в их творческой природе. Марселе Бертппо. Цель работы. Изучить различные виды живописи. ...Твёрдое состояние вещества
Самостоятельная работа. ВАРИАНТ 1. Мальчик вычислил, что при нагревании воды от 15ºС до кипения внутренняя энергия её увеличилась на 178,5 кДж. Какова ...Вычисления массовой доли растворенного вещества
. Задачи ЕГЭ.1. Массовая доля серной кислоты в растворе, полученном при смешивании 120г 20 %-го и 40г 50 %-го растворов кислоты, равна ……...% (Запишите ...
Агрегатные состояния вещества
План урока. Определение целей урока Выполнение лабораторного исследования Определение основных следствий эксперимента Решение качественных задач Решение ...Агрегатные состояния вещества
1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества. 1.3.1. Основные понятия Жидкое агрегатное состояние является промежуточным между ...Агрегатное состояние вещества
Твердое тело. Состояние, характеризующееся способностью сохранять объём и форму. Атомы твёрдого тела совершают лишь небольшие колебания вокруг состояния ...Агрегатное состояние вещества
Существуют 3 основных агрегатных состояния вещества. Газообразное Твердое Жидкое. Чем же различаются данные вещества. Агрегатное состояние. Различия. ...Агрегатное состояние вещества
Общие понятия. Агрегатное состояние вещества- состояние вещества, характеризующееся определенными качественными свойствами. Строение твердых тел. ...Агрегатное состояние вещества
Три состояния вещества. Газ Жидкость Твердое тело. Твердое. Жидкое. Газообразное состояние. Процессы с поглощением и выделением тепла. Плавление Парообразование ...Простые и сложные вещества
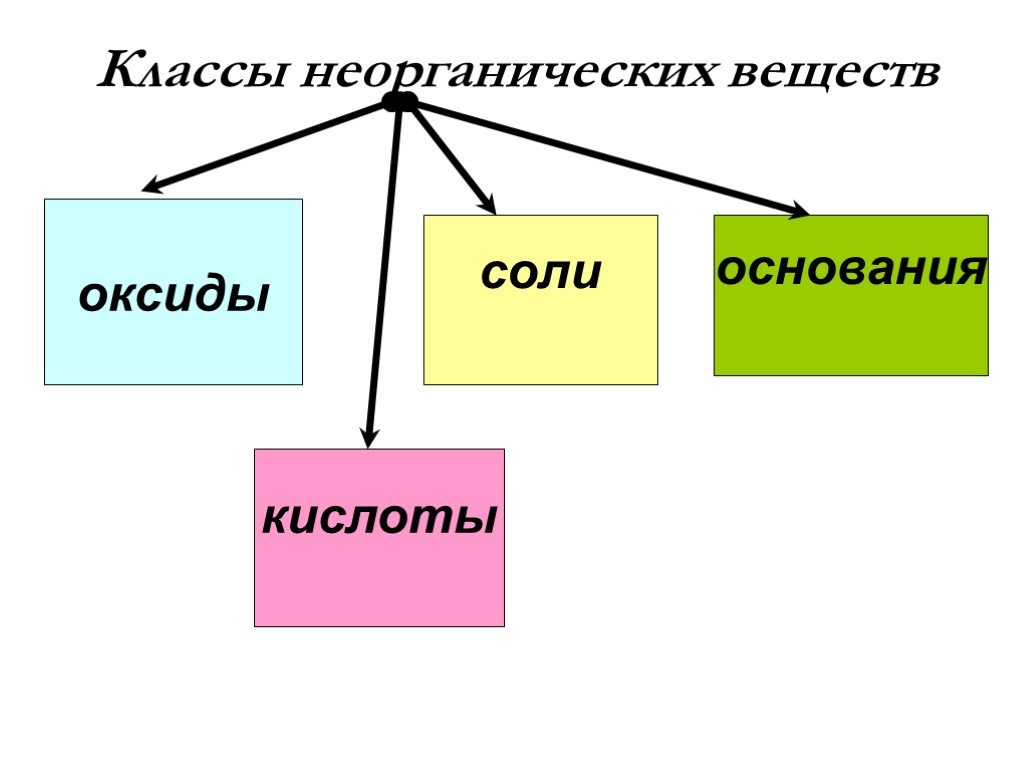
Содержание. Вещества Неорганические соединения Классификация неорганических соединений Простые вещества Металлы Неметаллы Аллотропия Агрегатное состояние ...Состояние вещества
Агрегатные состояния. Твердое Жидкое Газообразное. Плавление - переход вещества из твердого состояния в жидкое. Парообразование - переход вещества ...Газообразное состояние вещества
Цели урока:. Рассмотреть особенности газообразных веществ. Выделить важнейшие природные смеси газов. Обозначить основные экологические проблемы атмосферы. ...Характеристика азота как химического элемента и простого вещества
Вслед за Резерфордом такие же опыты провели Шееле, Пристли и Кавендиш, которые называли исследуемое вещество «удушливым воздухом», «дурным воздухом». ...Газообразные вещества
Рис.1. Агрегатные состояния воды: а – твёрдое; б – жидкое; в - газообразное. Большинство веществ в зависимости от условий могут находиться в одном ...Конспекты
Галогены. Общая характристика неметаллов. Элементы VII А группы. Неорганические вещества и охрана окружающей среды
План учебного занятия № 16. Дата Предмет. химия. группа. Ф.И.О. преподавателя:. Кайырбекова И.А. . І. Тема занятия:. Галогены. Общая характристика ...Химическая организация клетки. Неорганические вещества
Тема: «Химическая организация клетки. Неорганические вещества». Цели урока:. Образовательные. : сформировать знания о роли химических элементов, ...Химическая связь. Строение вещества
Тема: Систематизация и обобщение знаний по теме «Химическая связь. Строение вещества». (стр. флипчарта 1 скрыть / показать). Цель:. . обобщить и ...Строение вещества
Автор: Теплов Сергей Евгеньевич. Место работы: МБОУ ООШ №30, г. Сургут. Должность: учитель физики. 7 класс. Тема урока: «Строение вещества». ...Решение задач. Определение массовой доли растворенного вещества
Химия 9 класс. . . Тема. Решение задач. Определение массовой доли растворенного вещества. Цель. Научиться решать задачи с помощью алгоритмов; ...Растворы. Нахождение массовой доли растворенного вещества в растворе
Урок по химии в 8 классе. Тема урока: Растворы. Нахождение массовой доли растворенного вещества в растворе. Цель урока:. На основе сформированного ...Алюминий. Строение атома, физические и химические свойства простого вещества
ПЛАН-КОНСПЕКТ УРОКА. Тема: Алюминий. Строение атома, физические и химические свойства простого вещества. . . ФИО (полностью). . Иванова ...Чистые вещества и смеси. Способы разделения смесей
Урок химии в 8 классе. Тема: Чистые вещества и смеси. . Способы разделения смесей. Урок разработан на основе программы курса для 8 класса общеобразовательных ...Чистые вещества и смеси
8 класс. Тема урока:. Чистые вещества и смеси. Цели урока:. дать понятие о чистом веществе и смеси веществ; раскрыть значение смесей в природе ...Молекулы и вещества
ОМ – 5 класс. Тема "Молекулы и вещества". Тема урока. Молекулы как постройки из атомов. Цели урока:. а) дать первоначальные знания пятиклассникам ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:12 декабря 2018
Категория:Химия
Содержит:48 слайд(ов)
Поделись с друзьями:
Скачать презентацию