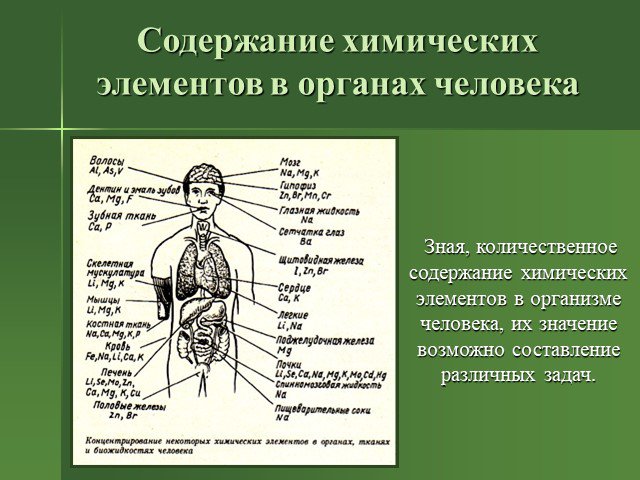
Презентация "Химия и здоровье человека" (10 класс) – проект, доклад
Презентацию на тему "Химия и здоровье человека" (10 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 31 слайд(ов).
Слайды презентации
Список похожих презентаций
Химические элементы металлы и здоровье человека
Ионы этого металла входят в состав вещества, употребляемого в пищу и называемого «белой смертью». Существенными источниками этого элемента являются ...Химия и здоровье
Цель: расширить знания учащихся о том, как сохранить и укрепить здоровье. Девиз урока: О, сколько нам открытий чудных Готовят просвещенья дух И опыт, ...рН среды и здоровье человека
Автор – Саутенко Александр Руководитель – Ширшина Н.В. Водородный показатель отражает активную реакцию среды и определяется содержанием катионов водорода ...Химия в жизни человека
«Широко распростирает химия руки свои в дела человеческие» М.В.Ломоносов. Химия. Моющие и чистящие средства. Пища. Средства для борьбы с насекомыми. ...Йод и здоровье человека
«…нос ее заострился, глаза вылезли из орбит, лицо и шея вздулись, мачеха стала трястись…». А может быть подобное превращение в жизни ? Более чем в ...Химия в быту человека
Элективный курс. Учитель: Сиротина С.Н. Химия в быту. Цель курса. Создание основы (мотивация и ориен- тация) для осознан- ного выбора естест- венно-научного ...Химия в повседневной жизни человека
Химия и повседневная жизнь человека. Химия, обладая огромными возможностями, создает не виданные материалы, умножает плодородие почвы, облегчает труд ...Влияние пищевых добавок на здоровье человека
Есть большая разница между тем, что любит есть человек и что любит организм. Что мы едим? У молодёжи широко распространены привычки неправильного ...Галогены и здоровье человека
Цель презентации. используя знания из области биологии, физиологии, медицины, исторические факты, показать важную роль галогенов для нормальной жизнедеятельности ...Химия и жизнь человека
Содержание. Химия и пища Химические средства гигиены и косметики Химические вещества в быту Химия и производство Химия и сельское хозяйство Химия ...Химия в искусстве
«Широко простирает химия руки свои в дела человеческие» М.В.Ломоносов. . . . Палитра. сажа мел охра. малахит лазурит киноварь. Пигмент - окрашенные ...Химия в жизни общества
Основополагающий вопрос:. Велики границы познания науки - химии в делах человеческих? Учебные предметы: химия, экология, биология. Направления работы: ...Влияние эфирного масла и конкрета из шалфея мускатного на организм человека
Введение. Эфирные масла - это пахучие вещества, которые вырабатываются эфиромасличными растениями и обусловливают их запах и практическую ценность. ...Вода в природе и жизни человека
Цель урока: обобщить, проанализировать и расширить знания о воде, ее роли в живой и неживой природе, в жизни человека, о необходимости бережного отношения ...Химия «Периодический закон»
Объектом исследования является Периодическая система и Периодический закон Д.И. Менделеева Цель исследования: проследить историю открытия Периодического ...Галогены в организме человека
Цель презентации. используя знания из области биологии, физиологии, медицины, исторические факты, показать важную роль галогенов для нормальной жизнедеятельности ...Химия в рисунках или эта удивительная химия
Цели: Воспитывать и развивать у учащихся стремление к самоопределению и самореализации. Задачи: Выявить творческих, инициативных учащихся; Активизировать ...Значение химии в жизни человека
Значение химии. Агропромышленность Машино – и ракетостроение Текстиль Архитектура Фармацевтика Предметы быта Пищевая промышленность Металлургия. Химия ...Значение химии в жизни человека
Значение химии в жизни человека трудно переоценить. Приведём фундаментальные области, в которых химия оказывает своё созидательное воздействие на ...Значение химии в жизни современного человека
Цель и задачи работы. Цель: Раскрыть степень влияния химии на повседневную жизнь современного человека. Задачи: Раскрыть тему; Изложить проблему; ...Конспекты
Химические элементы и здоровье человека
. Отдел образования администрации. . Тальменского района Алтайского края. Муниципальное общеобразовательное учреждение. Тальменская средняя ...Этиловый спирт и его влияние на здоровье человека
. . . . Интегрированный урок в 10 классе. (химия, биология). Учитель химии и биологии. МОУ ...Металлы в окружающей среде и здоровье человека
Тема урока:. «Металлы в окружающей среде и здоровье человека». (урок-конференция). 9 класс. Цели урока:. 1. Сформировать у учащихся представления ...Химия и повседневная жизнь человека
Тема урока в 9 классе. Химия и повседневная жизнь человека. Цель урока:. Определить роль химической науки в современной жизни и доказать, что ...Химия и повседневная жизнь человека
Брусова Татьяна Викторовна. МБОУ « СудогодскаяСОШ №2» г. Судогда. Учитель химии. Урок по химии в 11 классе. . . Тема «Химия и повседневная ...Химия и кулинария
Методическая разработка внеклассного мероприятия. на тему: «Химия и кулинария». (Аукцион). Автор: учитель химии. . Бижоева Лариса Аскеровна. ...Химия в руках художника
. Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». г.Нижнекамск Республика Татарстан. Конспект интегрированного ...Химия в моей жизни
МАОУ СОШ № 170 г. Екатеринбурга. Химия в моей жизни. . . Программа элективного курса. . . . . Дубровина Елена Николаевна,. . ...Действие этилового спирта на организм человека
План-конспект. открытого урока - презентации. в 10 классе по теме:. «Действие этилового спирта. на организм человека. .». Районной семинар - ...Химия на досуге
Внеклассное мероприятие «Химия на досуге». Цель мероприятия: Развивать интерес к предмету химия, смекалку, эрудицию, умение чётко и быстро формулировать ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:19 июня 2015
Категория:Химия
Классы:
Содержит:31 слайд(ов)
Поделись с друзьями:
Скачать презентацию