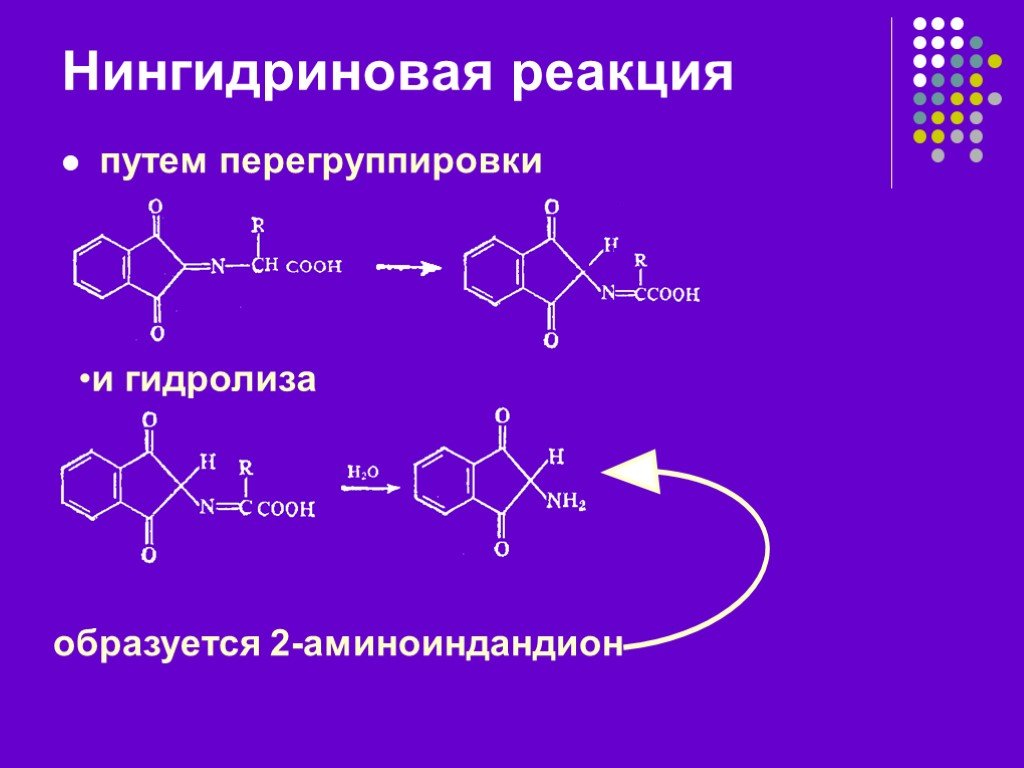
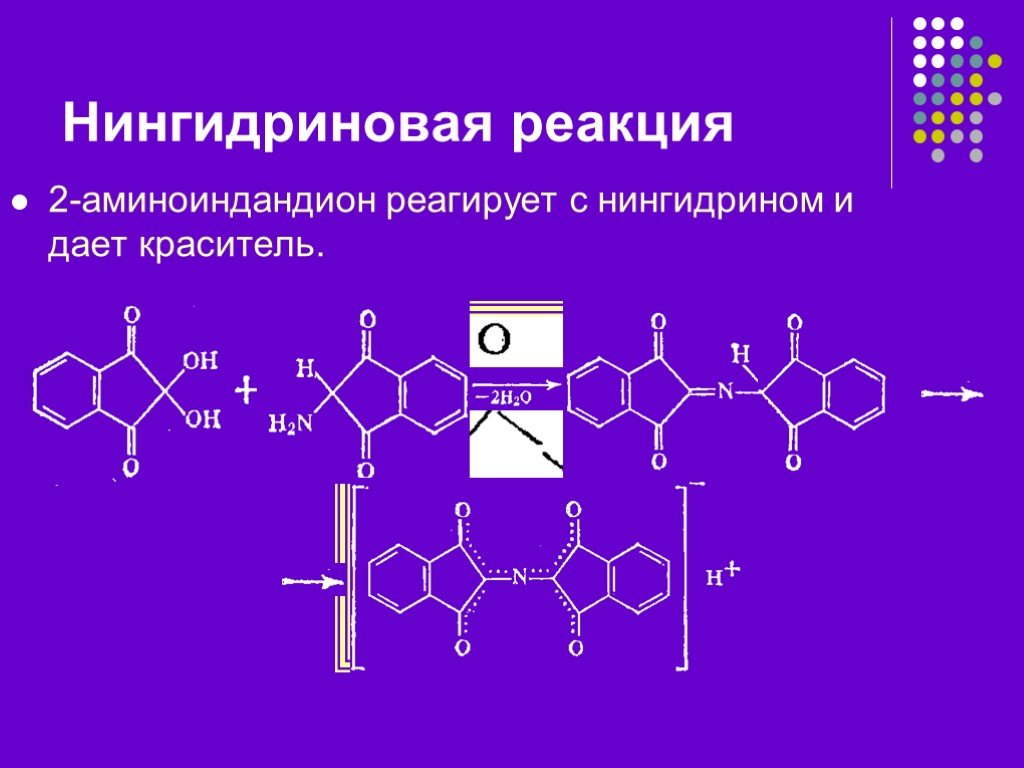
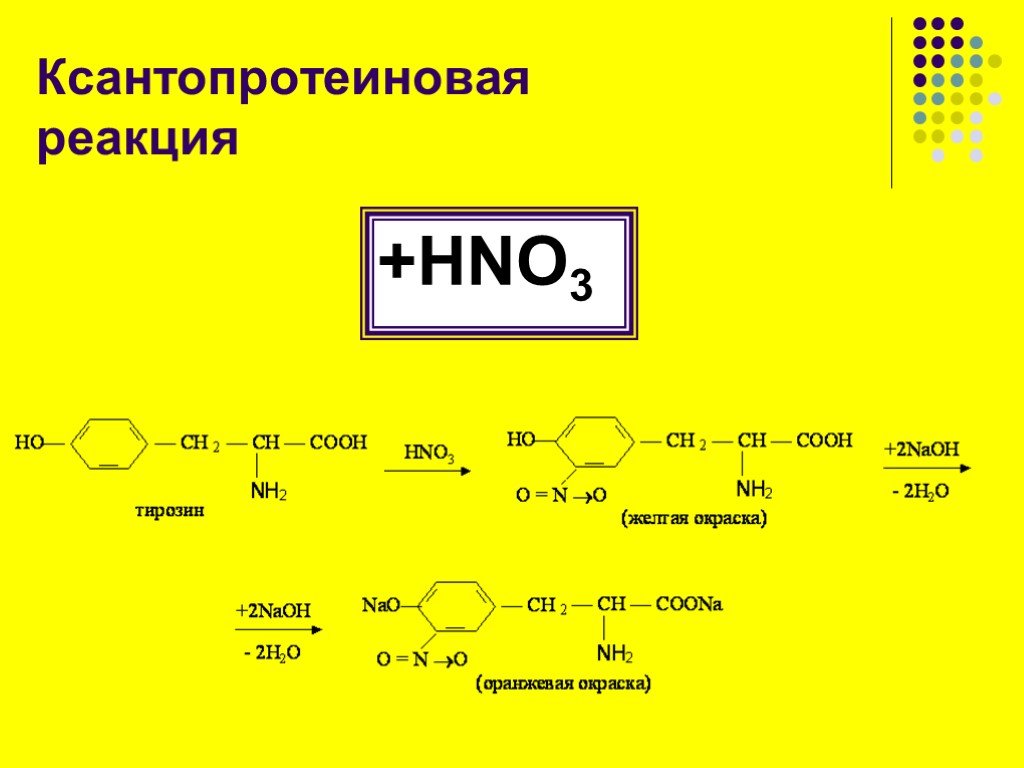
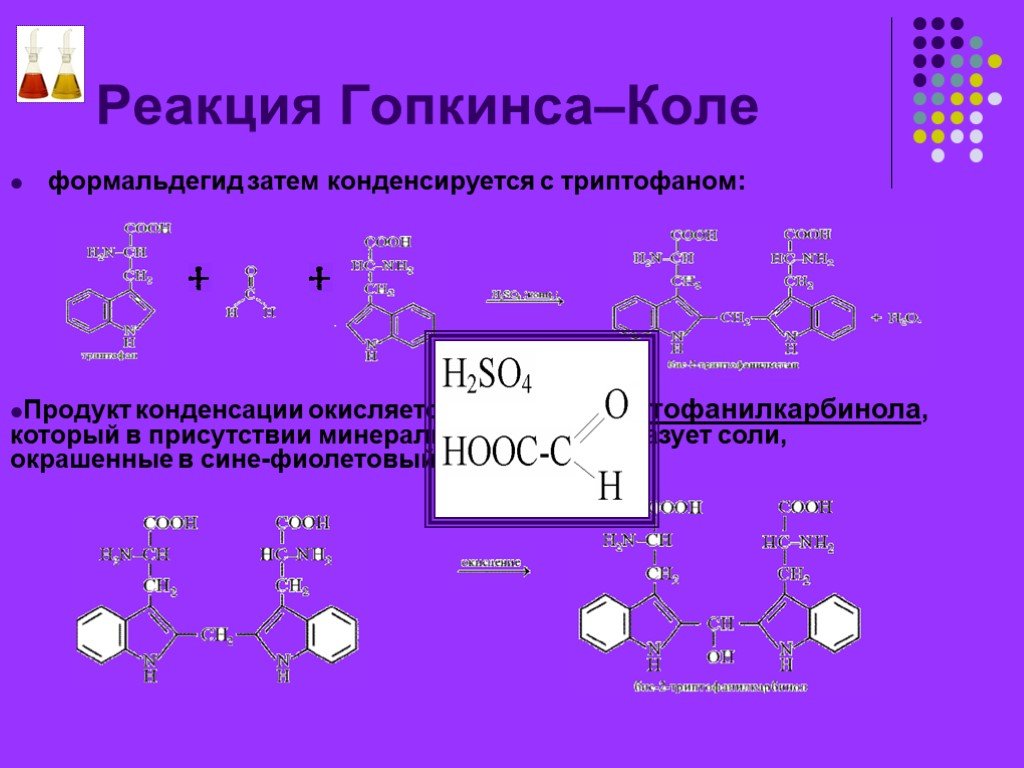
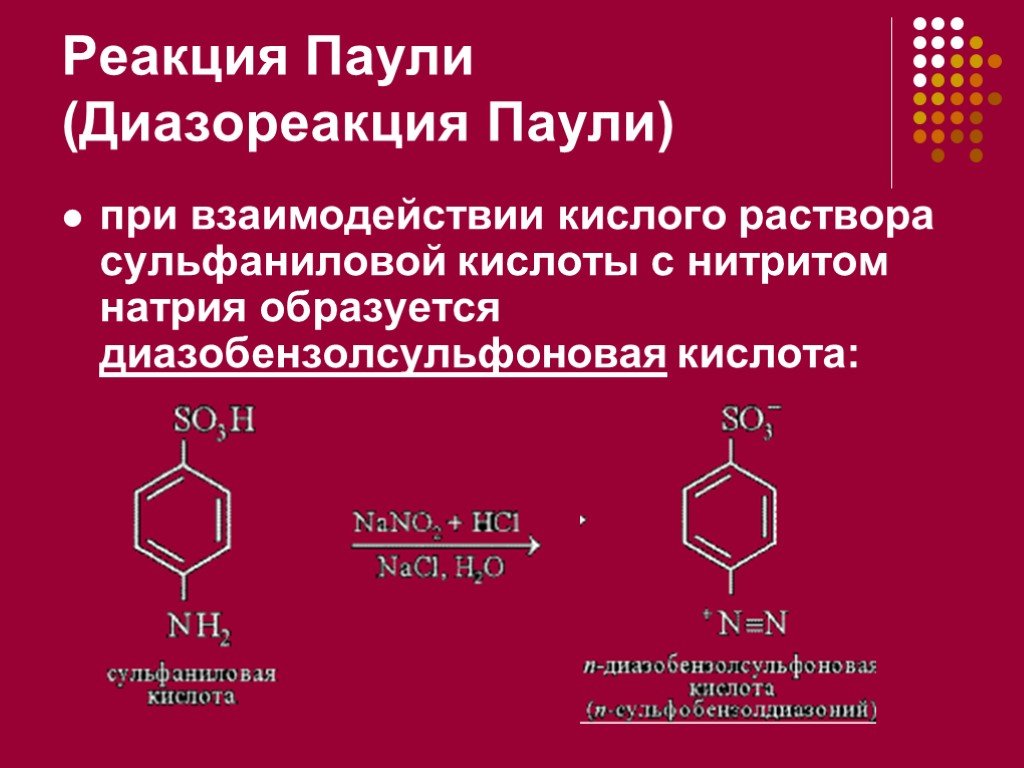
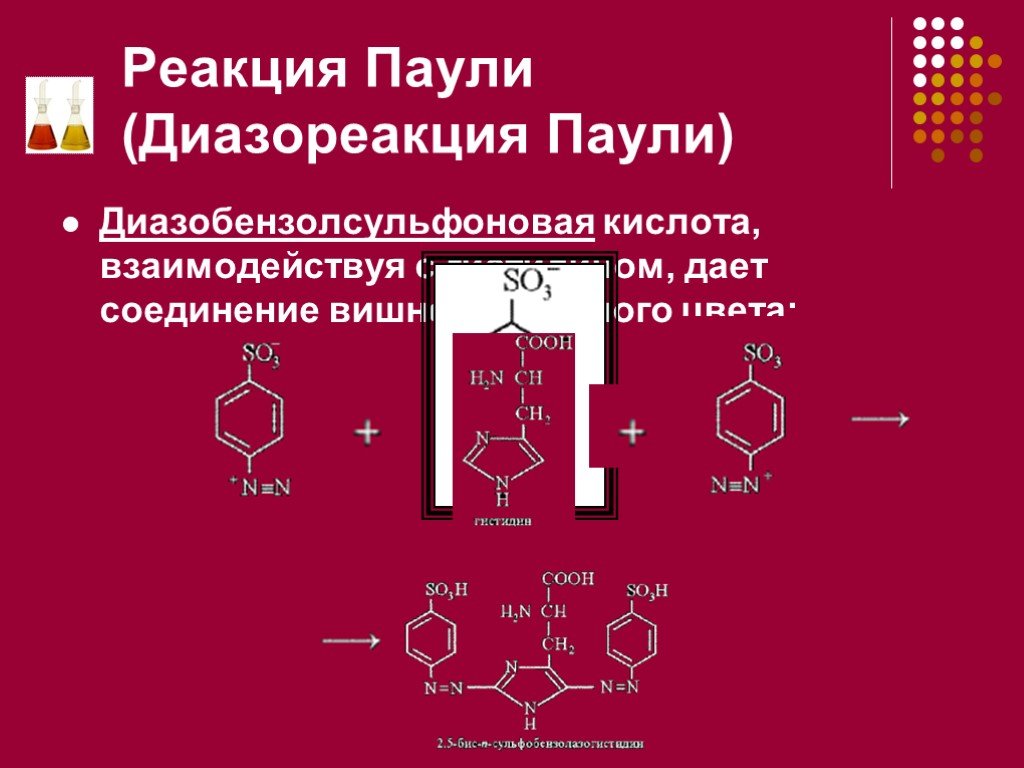
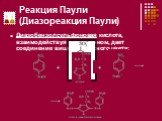
Презентация "Цветные реакции белков.Качественные реакции на остатки аминокислот." по химии – проект, доклад
Презентацию на тему "Цветные реакции белков.Качественные реакции на остатки аминокислот." можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 24 слайд(ов).
Слайды презентации
Список похожих презентаций
Влияние условий на скорость химической реакции
Заполните схему с вопросами о скорости реакции:. Задачи урока. Природа реагирующих веществ Концентрация реагирующих веществ Площадь реагирующих веществ ..."Факторы, влияющие на скорость химической реакции". 11-й класс
СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ –. отношение изменения концентрации вещества в единицу времени. . КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИИ ПО ПРИЗНАКУ ФАЗНОСТИ ...Анаэробные реакции
Ферменты анаэробных гликолиза и гликогенолиза. 1.Гексокиназа (глюкокиназа) (Mg2+) (2.7.1.1.) 2.Глюкозофосфатизомераза (5.3.1.9.) 3.Фосфофруктокиназа ...Изучение реакции среды в зависимости от типа гидролиза соли
Лабораторная работа Изучение реакции среды в зависимости от типа гидролиза соли. Цели: понять сущность гидролиза. научиться определять реакцию и тип ...Задачи на электролиз.
Задача 1. Водный раствор гидроксида натрия подвергли электролизу (сила тока 10 ампер, время электролиза 1 час). Определите количество веществ, выделившихся ...Задачи на определение массовой доли веществ в смесях
Цели:. Подготовка к ЕГЭ по математике и химии Отработать умение выделять часть в целом и объединять части в целое. «Истина не рождается в голове одного ...Задания на соответствие
Изотопы. Соотнесите:. Химический элемент:. Условные обозначения атомов:. 1. Углерод 2. Кальций 3. Неон а) б) в) г) д) е) ж) з) и). 1. Хлор 2. Калий ...Всё на свете химия!
А что же такое химия? Наука о веществах и превращениях друг в друга. Химия в быту. Химия в быту, сравнительно молодая наука, является нашим незаменимым ...Вплив радіонуклідів на живі організми
іонізує молекули; руйнує клітинні мембрани; уражає клітини кісткового мозку; призводить до генетичних ушкоджень; порушує імунну систему; викликає ...Вода – важнейшая составляющая жизни на Земле
Введение:. Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и ..."Химическая атака на нас"
Девиз урока: «Химики – это те, кто действительно понимает мир!». Страница 1 «Здоровье человека и средства бытовой химии». Рынок продажи средств бытовой ...Влияние железа на организм
Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности, оно – орудие войны и мирного ...Влияние внешних условий на рост кристаллов различных солей
Объект исследования:. насыщенные растворы медного купороса CuSO4∙5Н2О; алюмокалиевых квасцов KCl(SO4)2*12H2O. Задачи исследования:. приготовление ...Влияет - ли рН воды на рост бобовых
Актуальность выбора темы: Для роста растений необходимы определенные условия. Им нужен грунт, свет, вода и воздух. С помощью нашей работы мы хотели ...Благородные металлы на службе у человека
Цель урока:. Рассмотреть и сравнить с разных точек зрения Химии и экологии; Литературы и философии; Географии и истории Самые популярные металлы окружающие ...Безопасность на уроке химии
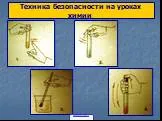
Пробовать вещества на вкус, есть и пить в химическом кабинете. Осторожно направляйте к себе газ рукой. ЗАПРЕЩАЕТСЯ. . . . . ЗАПРЕЩАЮЩИЕ ЗНАКИ. Запрещается ...Активизация обучающихся на уроках химии как показатель развития их мыслительной деятельности.
Приёмы активизации мыслительной деятельности обучающихся:. Приём стимулирующих звеньев Приём реконструкции Приём прогнозирования. Приём стимулирующих ...Изучение отдельных тем базового содержания курса химии в 8 классе, на основе технологии полного усвоения
Проблема. Усвоение всеми учащимися базового содержания образования через обучение в соответствии с индивидуальными особенностями восприятия и усвоения. ...«Радіоактивний розпад хімічних елементів. Вплив радіації на живі організми».
«Радіоактивний розпад хімічних елементів. Вплив радіації на живі організми». Тема уроку:. “Ворога необхідно знати в обличчя. Знати – значить перемогти!” ...Влияние культуры знаний на отношение к курению
Объект исследования:. Учащиеся 10-11 классов МОУСОШ № 5(112 учеников). Предмет исследования:. Условия и факторы, определяющие отношение учащихся к ...Конспекты
Обобщение знаний об основных типах химической реакции
. /8 класс/. Тема урока:. Обобщение знаний об основных типах химических реакций. Цель:. Обобщить и закрепить знания о типах ...Свойства ионов. Качественные реакции на катионы и анионы
Сидорина Г. Н. , учитель химии. . Г У. Средняя общеобразовательная школа. N. 0. 5, г. Актау. . . Тема урока: «Свойства ионов. Качественные ...Качественные реакции на катионы и анионы
Тема урока: «Качественные реакции на катионы и анионы». . Цель работы:. . проведение качественных реакций на ионы. . . Задачи работы:. ...Решение задач на определение выхода продукта реакции
Тема урока: Решение задач на определение выхода продукта реакции. Алгоритм решения задач. Составьте краткое условие задачи. . Составьте ...Вычисления по химическим уравнениям реакций массы, количества вещества или объема по известной массе, количеству вещества или объему одного из вступающих или получающихся в реакции веществ
Дата_____________ Класс_______________. Тема:. . Вычисления по химическим уравнениям реакций массы, количества вещества или объема по известной ...Переходные металлы и их качественные реакции
Методическая разработка урока по химии. Султанова Наталья Викторовна,. преподаватель ГБОУ СПО «Краевой политехнический колледж». г. Чернушка, ...Окислительно-восстановительные реакции
Анализ урока. Учитель. Гордова Марина Алексеевна. Класс. 9. . Предмет. химия. Тема урока. Окислительно-восстановительные реакции. Единица ...Окислительно-восстановительные реакции
Санкт-Петербургское государственное автономное. профессиональное образовательное учереждение. « морской технический колледж». Методические ...Окислительно - восстановительные реакции
Фалинская Наталья Васильевна. Учитель высшей категории химии и биологии. Кушокинксая СОШ Бухаржырауского района Карагандинской области. 8 ...Окислительно - восстановительные реакции
Рогова Е.В. Учитель химии и биологии. МКОУ Васильевская ООШ Воронежской области. Тема урока. - лекции: Окислительно - восстановительные ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:6 декабря 2018
Категория:Химия
Содержит:24 слайд(ов)
Поделись с друзьями:
Скачать презентацию