Слайд 1Соединения серы
Химия. 9 класс. Учитель химии МОУ СОШ №1 г. Алексеевки Харченко Е.П.
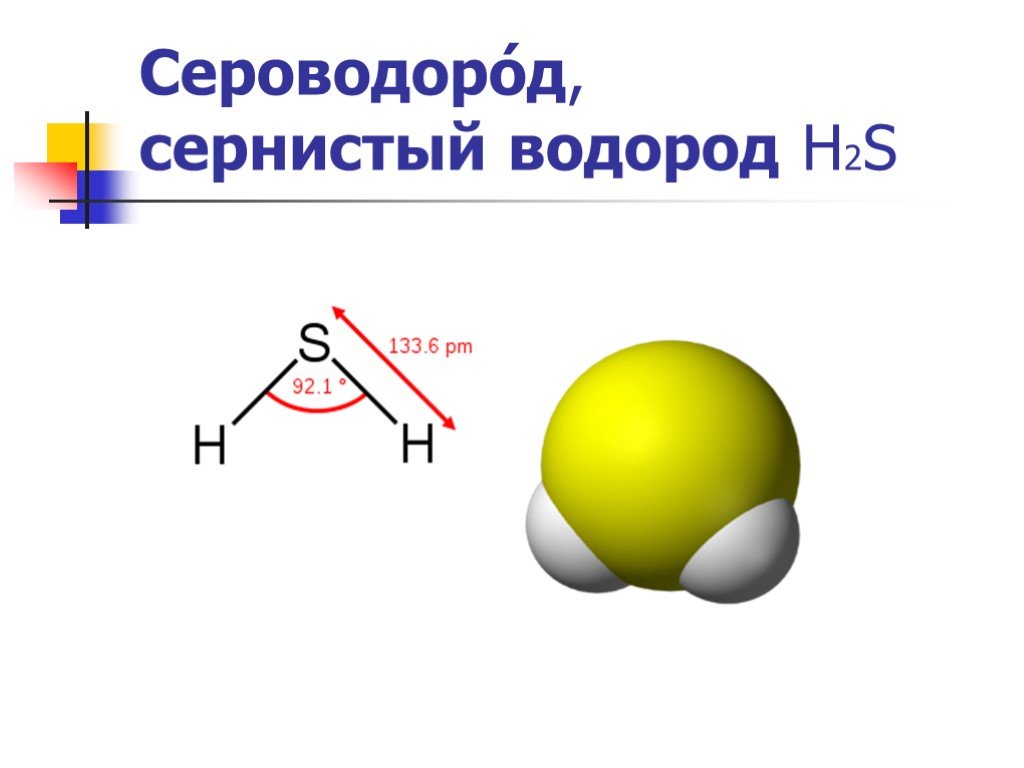
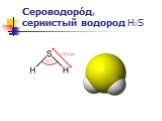
Слайд 2Сероводоро́д, сернистый водород Н2S
Слайд 3Общие Систематическое наименование сероводород / hydrogen sulphide Химическая формула H2S Отн. молек. Масса 34.082 а. е. м. Молярная масса34.082 г/моль Физические свойства Состояние (ст. усл.)бесцветный газ Плотность1.5392 г/л г/см³ Термические свойства Температура плавления-82.30 °C Температура кипения-60.28 °C Химические свойства pKa6.89, 19±2 Растворимость в воде0.25 (40 °C) г/100 мл КлассификацияРег. номер CAS7782-79-8
Слайд 4Бесцветный газ с неприятным запахом (тухлого яйца) и сладковатым вкусом. Плохо растворим в воде, хорошо — в этаноле. При больших концентрациях разъедает металл. Взрывчатая смесь с воздухом 4,5 - 45%. В природе встречается очень редко в виде смешанных веществ нефти и газа. Имеет очень неприятный запах, вреден для лёгких и всего организма. Сейчас сероводород используют в лечебных целях, например, в сероводородных ваннах

Слайд 5Сероводоро́д Н2S Физические свойства
Термически неустойчив (при температурах больше 400 °C разлагается на простые вещества — S и H2), ядовитый (вдыхание воздуха с его примесью вызывает головокружение, головную боль, тошноту, а со значительным содержанием приводит к коме, судорогам, отёку лёгких и даже к летальному исходу), газ, тяжелее воздуха с неприятным запахом тухлых яиц. Молекула сероводорода имеет угловую форму, поэтому она полярна (μ = 0,34·10-29 Кл·м). В отличие от молекул воды, молекулы сероводорода не образуют прочных водородных связей, поэтому H2S — газ. Насыщенный водный раствор (сероводородная вода) H2S является очень слабой сероводородной кислотой.

Слайд 6Сероводоро́д Н2S Химические свойства
В воде сероводород мало растворим, водный раствор H2S является очень слабой кислотой: H2S → HS− + H+ Ka = 6.9×10−7 моль/л; pKa = 6.89. С основаниями реагирует: H2S + 2NaOH = Na2S + 2H2O (обычная соль, при избытке NaOH) H2S + NaOH = NaHS + H2O (кислая соль, при отношении 1:1) Сероводород — сильный восстановитель. На воздухе он горит синим пламенем: 2H2S + ЗО2 = 2Н2О + 2SO2 при недостатке кислорода: 2H2S + O2 = 2S + 2H2O (на этой реакции основан промышленный способ получения серы). Сероводород реагирует также со многими другими окислителями, при его окислении в растворах образуется свободная сера или SO42-, например: 3H2S + 4HClO3 = 3H2SO4 + 4HCl 2H2S + SO2 = 2Н2О + 3S H2S + I2 = 2HI + S

Слайд 7Сульфиды Соли сероводородной кислоты называют сульфидами. В воде хорошо растворимы только сульфиды щелочных металлов, бария и аммония. Сульфиды остальных металлов практически не растворимы в воде, они выпадают в осадок при введении в растворы солей металлов раствора сульфида аммония (NH4)2S. Многие сульфиды ярко окрашены. Для щелочных и щелочноземельных металлов известны также гидросульфиды M+HS и M2+(HS)². Гидросульфиды Са²+ и Sr2+ очень нестойки. Являясь солями слабой кислоты, растворимые сульфиды подвергаются гидролизу. Гидролиз сульфидов, содержащих металлы в высоких степенях окисления (Al2S3, Cr2S3 и др.) часто проходит необратимо. Многие природные сульфиды в виде минералов являются ценными рудами (пирит, халькопирит, киноварь). Получение Взаимодействие разбавленных кислот на сульфиды: Взаимодействие сульфида алюминия с водой (эта реакция отличается чистотой полученного сероводорода):

Слайд 8Применеие сероводорода Н2S
Сероводород из-за своей токсичности находит ограниченное применение. В аналитической химии сероводород и сероводородная вода используются как реагенты для осаждения тяжёлых металлов, сульфиды которых очень слабо растворимы В медицине — в составе природных и искусственных сероводородных ванн, а также в составе некоторых минеральных вод Сероводород применяют для получения серной кислоты, элементной серы, сульфидов Используют в органическом синтезе для получения тиофена и меркаптанов В последние годы рассматривается возможность использования сероводорода, накопленного в глубинах Чёрного моря, в качестве энергетического (сероводородная энергетика) и химического сырья.
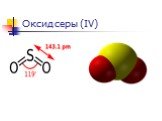
Слайд 10Общие свойства Систематическое наименование Оксид серы(IV) Химическая формула SO2 Относительная молекулярная масса 64.054 а. е. м. Молярная масса 64.054 г/моль Физические свойства Состояние (норм. условия )бесцветный газ, Плотность 2,927 г/л (г/см³) Термические свойства Температура плавления−75,5 °C Температура кипения−10,01 °C Химические свойства Растворимость в воде11,5 г/100 мл Классификация Рег. номер CAS[7446-09-5]
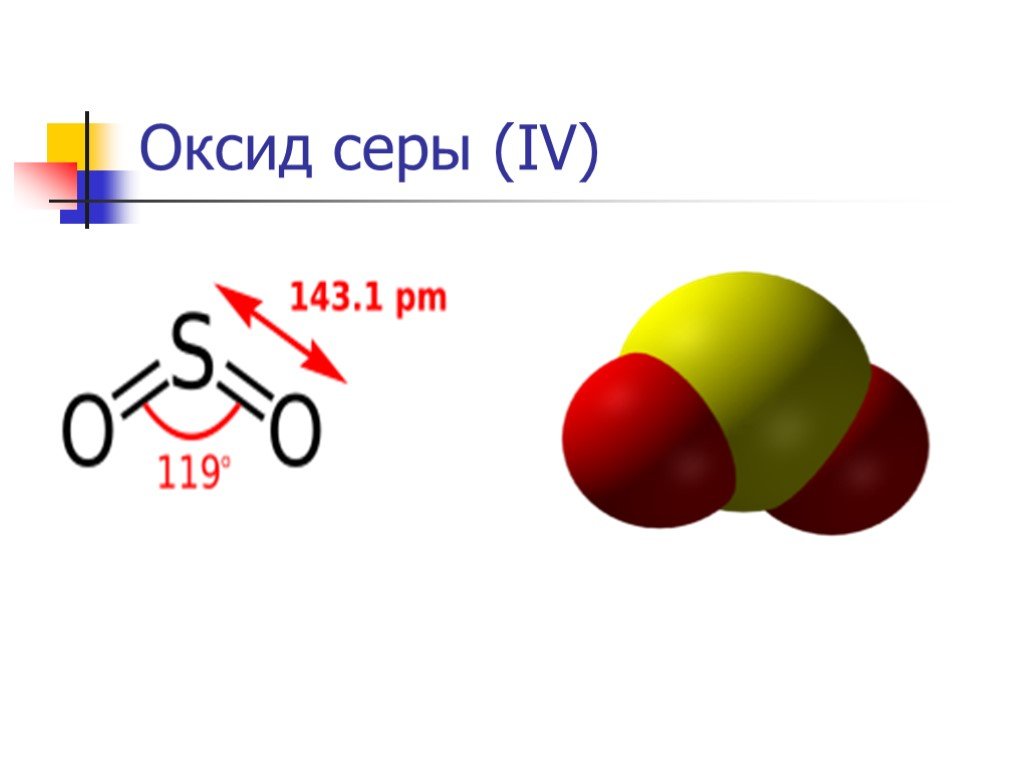
Слайд 11Химические свойства оксида серы (IV)
Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима): SO2 + H2O ↔ H2SO3. Со щелочами образует сульфиты: SO2 + 2NaOH → Na2SO3 + H2O. Химическая активность SO2 весьма велика. Наиболее ярко выражены восстановительные свойства SO2, степень окисления серы в таких реакциях повышается: SO2 + Br2 + 2H2O → H2SO4 + 2HBr, 2SO2 + O2 → 2SO3 (требуется катализатор V2O5 и температура 450°С),
Слайд 12Данная реакция является качественной реакцией на сульфит-ион SO32- и на SO2 (обесцвечивание фиолетового раствора). 5SO2 + 2KMnO4 + 2H2O → 2H2SO4 + 2MnSO4 + K2SO4. В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства. Например, для извлечения серы их отходящих газов металлургической промышленности используют восстановление SO2 оксидом углерода(II): SO2 + 2CO → 2CO2 + S↓. Или для получения фосфорноватистой кислоты: PH3 + SO2 → H(PH2O2) + S↓
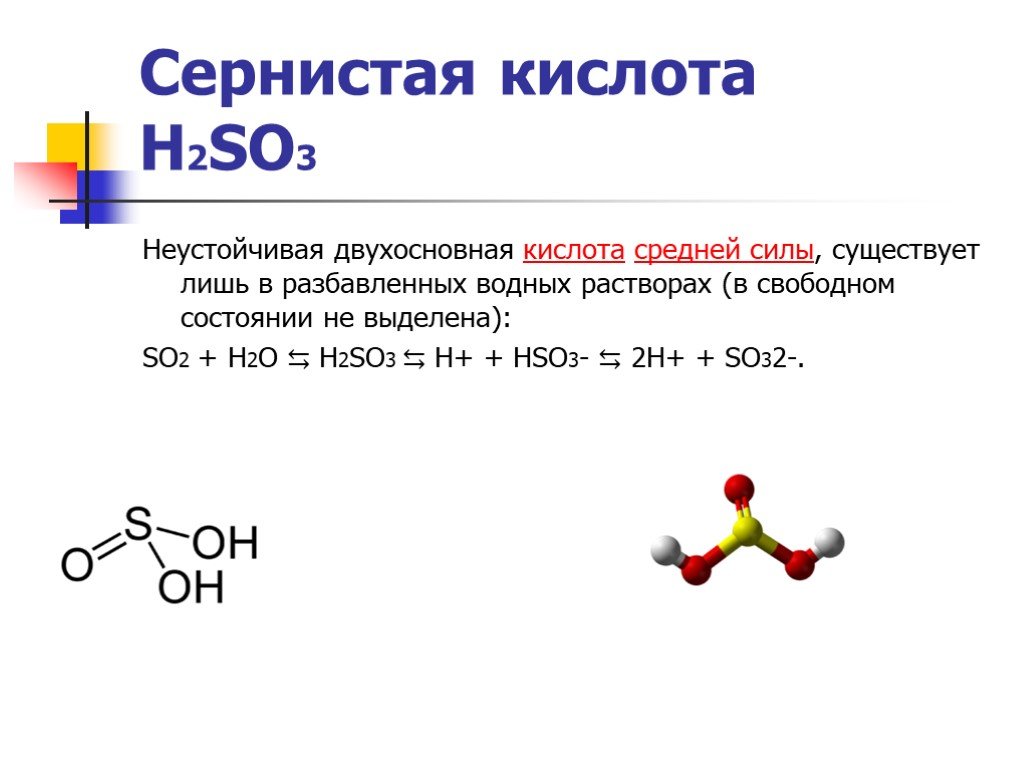
Слайд 13Сернистая кислота H2SO3
Неустойчивая двухосновная кислота средней силы, существует лишь в разбавленных водных растворах (в свободном состоянии не выделена): SO2 + H2O ⇆ H2SO3 ⇆ H+ + HSO3- ⇆ 2H+ + SO32-.
Слайд 14Химические свойства Сернистой кислоты H2SO3
Кислота средней силы: H2SO3 H+ + HSO3-, KI = 2·10-2 HSO3- H+ + SO32-, KII = 6·10-8 Растворы H2SO3 всегда имеют резкий специфический запах (похожий на запах зажигающейся спички), обусловленный наличием химически не связанного водой SO2. Двухосновная кислота, образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи): и средние — сульфиты (в избытке щёлочи): Как и сернистый газ, сернистая кислота и её соли являются сильными восстановителями: При взаимодействии с ещё более сильными восстановителями может играть роль окислителя: Качественная реакция на сульфит-ионы — обесцвечивание раствора перманганата калия:

Слайд 15Применение Сернистой кислоты H2SO3
Сернистая кислота и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальция Са(HSO3)2 (сульфитный щелок) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин — вещество, связывающее волокна целлюлозы, в результате чего волокна отделяются друг от друга; обработанную таким образом древесину используют для получения бумаги).
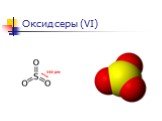
Слайд 17Общие свойства Систематическое наименование Оксид серы(VI) Химическая формула SO3 Отн. молек. Масса 80.06 а. е. м. Молярная масса 80.06 г/моль Физические свойства Состояние (ст. усл.) бесцветный газ Плотность1.92 г/см³ Термические свойства Температура плавления16,9 °C Температура кипения45 °C Энтальпия образования (ст. усл.)−397.77 кДж/моль Классификация Рег. номер CAS[7446-11-9]
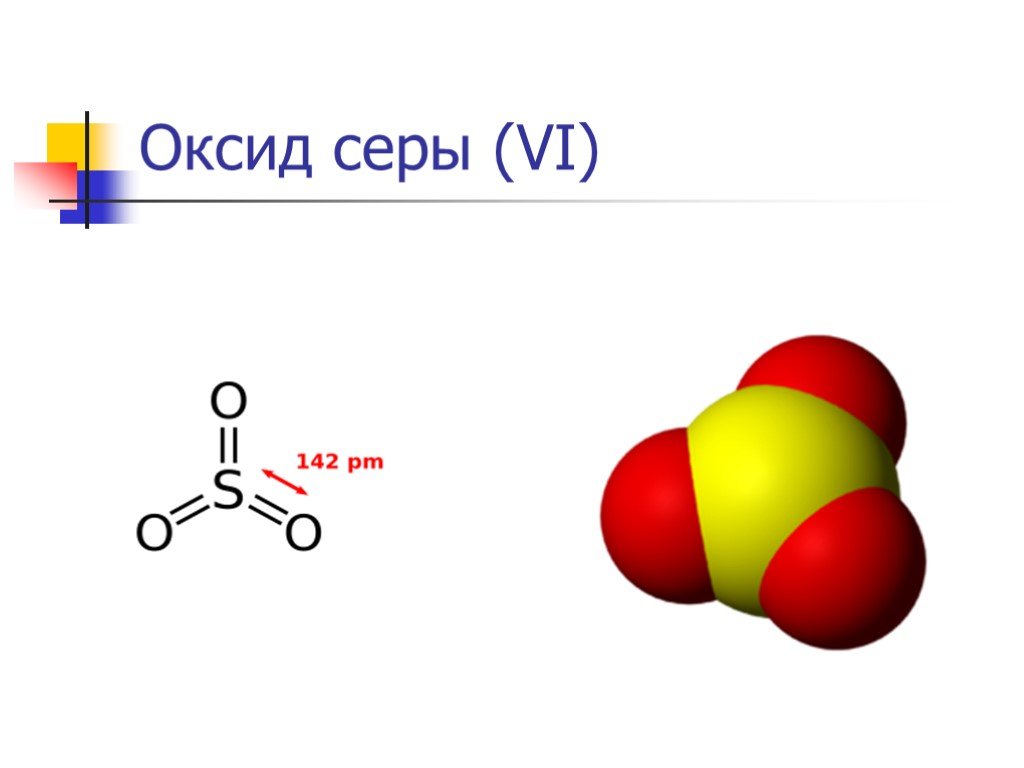
Слайд 18Оксид серы (VI) Физические свойства
Окси́д се́ры(VI) (се́рный ангидри́д, трео́кись се́ры, се́рный га́з) SO3 — высший оксид серы, тип химической связи: ковалентная полярная В обычных условиях легколетучая бесцветная жидкость с удушающим запахом. При температурах ниже 16,9 °C застывает с образованием смеси различных кристаллических модификаций твёрдого SO3.
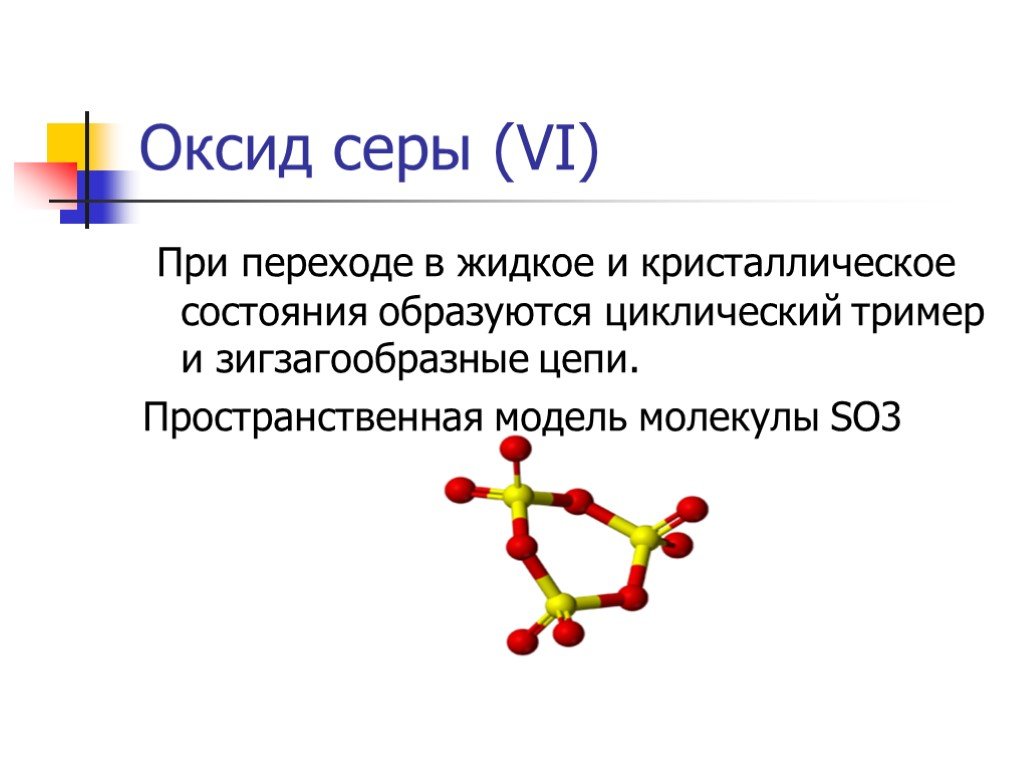
Слайд 19При переходе в жидкое и кристаллическое состояния образуются циклический тример и зигзагообразные цепи. Пространственная модель молекулы SO3
Слайд 20Получение оксида серы (VI)
Получают, окисляя оксид серы(IV) кислородом воздуха при нагревании, в присутствии катализатора (V2O5, Pt или Na2VO3): 2SO2 + O2 → 2SO3 + Q. Можно получить термическим разложением сульфатов: Fe2(SO4)3 → Fe2O3 + 3SO3, или взаимодействием SO2 с озоном: SO2 + O3 → SO3 + O2↑. Для окисления SO2 используют также NO2: SO2 + NO2 → SO3 + NO↑. Эта реакция лежит в основе исторически первого, нитрозного способа получения серной кислоты.
Слайд 21Оксид серы (VI) Химические свойства
1. Кислотно-основные: SO3 — типичный кислотный оксид, ангидрид серной кислоты. Его химическая активность достаточно велика. При взаимодействии с водой образует серную кислоту: SO3 + H2O → H2SO4. Взаимодействует с основаниями: 2KOH + SO3 → K2SO4 + H2O, основными оксидами: CaO + SO3 → CaSO4, c амфотерными оксидами: 3SO3 + Al2O3 → Al2(SO4)3. SO3 растворяется в 100%-й серной кислоте, образуя олеум: H2SO4 (100 %) + SO3 → H2S2O7.
Слайд 222. Окислительно-восстановительные: SO3 характеризуется сильными окислительными свойствами, восстанавливается, обычно, до сернистого ангидрида: 5SO3 + 2P→ P2O5 + 5SO2 3SO3 + H2S → 4SO2 + H2O 2SO3 + 2KI → SO2 + I2 + K2SO4. 3. При взаимодействии с хлороводородом образуется хлорсульфоновая кислота: SO3 + HCl → HSO3Cl Также присоединяет хлор, образуя тионилхлорид: SO3 + Cl2 + 2SCl2 → 3SOCl2
Слайд 23Серная кислота Н2 SO4
Слайд 24Общие свойства Систематическое наименование серная кислота Химическая формула H2SO4 Отн. молек. Масса 62.03 а. е. м. Молярная масса98.078 г/моль Физические свойства Состояние (ст. усл.)бесцветная маслянистая жидкость без запаха Плотность1,8356 г/см³ Термические свойства Температура плавления10,38 °C Температура кипения279,6 °C Химические свойства Растворимость в водесмешивается во всех соотношениях г/100 мл Классификация Рег. номер CAS7664-93-
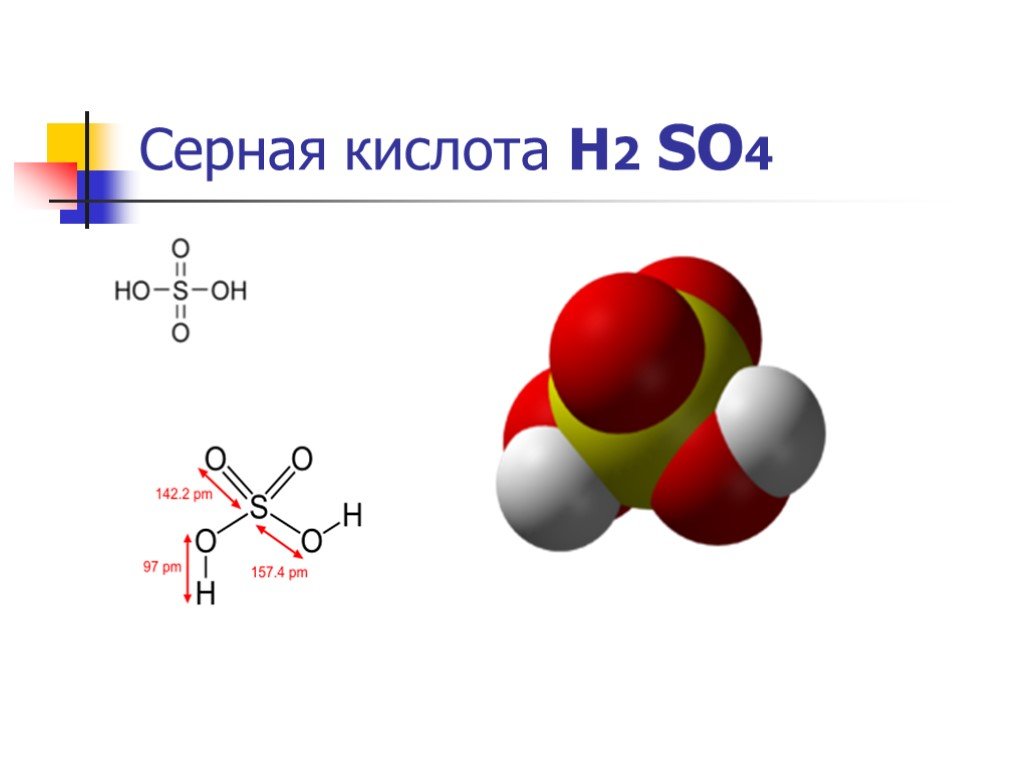
Слайд 25Физические свойства серной кислоты Н2 SO4
Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3:H2O 1, — раствор SO3 в серной кислоте (олеум).

Слайд 26Химические свойства серной кислоты Н2 SO4
Серная кислота - сильная двухосновная кислота, диссоциация ее протекает по двум ступеням: H2SO4 = H+ + HSO4- - первая ступень HSO4- =H+ + SO42- - вторая ступень В концентрированных растворах диссоциация серной кислоты по второй ступени незначительна. Серная кислота - сильнейшее дегидратирующее (водоотнимающее) вещество. Она поглощает влагу из воздуха (гигроскопична), отнимает воду 1. от кристаллогидратов: CuSO4*5H2O голубой ------------------------> CuSO4 белый + 5H2O 2. углеводов (обугливает дерево и бумагу): C12H22O11 --------------------------> 12C + 11H2O 3. спиртов: C2H5OH -----------------------------> CH2=CH2 + H2O В окислительно-восстановительных реакциях разбавленная серная кислота проявляет свойства обычной кислоты (неокислитель) - при этом восстанавливаются ионы Н+, например: Fe + H2SO4 разб.= FeSO4 + H2 Разбавленная H2SO4 не взаимодействует с металлами, стоящими в ряду напряжений правее водорода. Концентрированная серная кислота - кислота-окислитель, при этом восстанавливается сера (+6). Она окисляет металлы, стоящие в ряду напряжений правее водорода: Cu + 2H2SO4конц. = CuSO4 + SO2 + 2H2O

Слайд 27Серная кислота проявляет все свойства сильных кислот: а) взаимодействует с основными оксидами: CuO + H2SO4 = CuSO4 + H2O б) с основаниями: 2NaOH + H2SO4= Na2SO4 + 2H2O в) вытесняет другие кислоты из их солей, например те, которые слабее нее: CaCO3 + H2SO4 = CaSO4 + CO2 + H2O или более летучие (обладающие температурами кипения ниже, чем у серной кислоты): NaNO3твердый + H2SO4 конц.= NaHSO4 + HNO3- при нагревании и металлы,стоящие левее водорода, при этом сера восстанавливается до степени окисления +4, 0 и -2: Zn + 2H2SO4 = ZnSO4 + SO2 + 2H2O 3Zn + 4H2SO4 = 3ZnSO4 + S + 4H2O 4Zn + 5H2SO4 = 4ZnSO4 + H2S + 4H2O

Слайд 28Железо, алюминий, хром концентрированной серной кислотой пассивируются, однако при сильном нагревании реакция начинается, например: 2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2 + 6H2O Концентрированная серная кислота окисляет неметаллы, например: C + 2H2SO4 = CO2 + 2SO2 + 2H2O S +2H2SO4 = 3SO2 + 2H2O Концентрированная серная кислота окисляет также сложные вещества, например HI и HBr: 2HBr + H2SO4 = Br2 + SO2 + 2H2O 8HI + H2SO4 = 4I2 + H2S + 4H2O соли железа (2): 2FeSO4 + 2H2SO4 = Fe2(SO4)3 + 2H2O + SO2
Слайд 29Задания для самостоятельной работы:
Напишите уравнения взаимодействия разбавленной серной кислоты с металлами; основными оксидами; амфотерными оксидами; основаниями; амфотерными гидроксидами.

Слайд 30Соли серной кислоты
Серная кислота как двухосновная кислота образует два ряда солей - кислые - гидросульфаты и средние - сульфаты. В безводном состоянии выделены только гидросульфаты щелочных металлов. Средние сульфаты (безводные) - как правило, бесцветные кристаллические вещества, склонные к образованию кристаллогидратов (часто окрашеных), например: Na2SO4*10H2O - глауберова соль (мирабилит) - бесцветная MgSO4*7H2O - горькая (английская) соль - бесцветная CuSO4*5H2O - медный купорос - голубой FeSO4*7H2O - железный купорос - голубовато-зеленый CaSO4*2H2O - гипс - белый Сульфаты при нагревании разлагаются (кроме сульфатов щелочных металлов, которые термически устойчивы), например CaSO4 - при 1400oС: 2CaSO4 = 2CaO + 2SO2 + O2 Сульфаты переходных металлов разлагаются при более низких температурах, например Fe2(SO4)3 - при 700-800oС: Fe2(SO4)3 = Fe2O3 + 3SO3

Слайд 31Производство серной кислоты
Сырьём для получения серной кислоты служат сера, сульфиды металлов, сероводород, отходящие газы теплоэлектростанций, сульфаты железа, кальция и др. Основные этапы получения серной кислоты: Обжиг сырья с получением SO2 Окисление SO2 в SO3 Абсорбция SO3 В промышленности применяют два метода окисления SO2 в производстве серной кислоты: контактный — с использованием твердых катализаторов (контактов), и нитрозный — с оксидами азота.
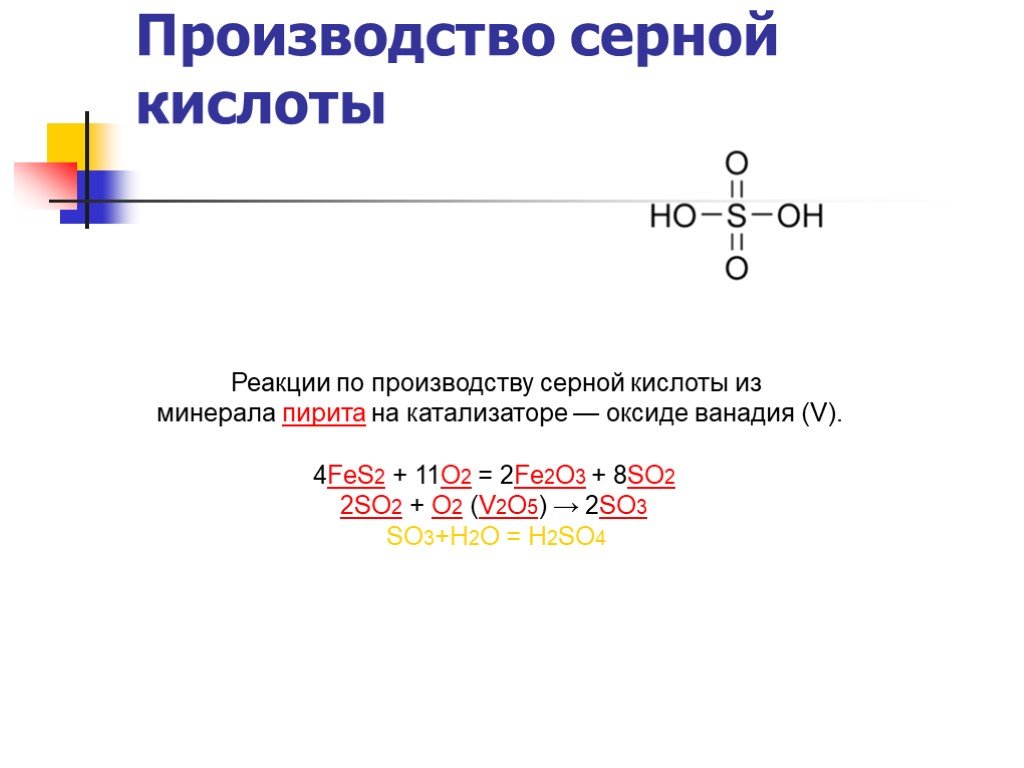
Слайд 32Реакции по производству серной кислоты из минерала пирита на катализаторе — оксиде ванадия (V). 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 2SO2 + O2 (V2O5) → 2SO3 SO3+Н2О = Н2SO4
Слайд 33Схема «Производство серной кислоты контактным способом»:
Слайд 34Применение серной кислоты
В производстве минеральных удобрений; как электролит в свинцовых аккумуляторах; для получения различных минеральных кислот и солей; в производстве химических волокон, красителей, дымообразующих веществ и взрывчатых веществ; в нефтяной, металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности; в пищевой промышленности — зарегистрирована в качестве пищевой добавки E513(эмульгатор); в промышленном органическом синтезе в реакциях: дегидратации (получение диэтилового эфира, сложных эфиров); гидратации (этанол из этилена); сульфирования (синтетические моющие средства и промежуточные продукты в производстве красителей); алкилирования (получение изооктана, полиэтиленгликоля, капролактама) и др. Самый крупный потребитель серной кислоты — производство минеральных удобрений.

Слайд 35Исторические сведения о серной кислоте
Серная кислота известна с древности. Первое упоминание о кислых газах, получаемых при прокаливании квасцов или железного купороса «зеленого камня», встречается в сочинениях, приписываемых арабскому алхимику Джабир ибн Хайяну. Позже, в IX веке персидский алхимик Ар-Рази, прокаливая смесь железного и медного купороса (FeSO4•7H2O и CuSO4•5H2O), также получил раствор серной кислоты. Этот способ усовершенствовал европейский алхимик Альберт Магнус, живший в XIII веке. В XV веке алхимики обнаружили, что серную кислоту можно получить, сжигая смесь серы и селитры, или из пирита — серного колчедана, более дешевого и распространенного сырья, чем сера. Таким способом получали серную кислоту на протяжении 300 лет, небольшими количествами в стеклянных ретортах. И только в середине 18 столетия, когда было установлено, что свинец не растворяется в серной кислоте, от стеклянной лабораторной посуды перешли к большим промышленным свинцовым камерам.

Слайд 36Дополнительные сведения о серной кислоте
Мельчайшие капельки серной кислоты могут образовываться в средних и верхних слоях атмосферы в результате реакции водяного пара и вулканического пепла, содержащего большие количества серы. Получившаяся взвесь, из-за высокого альбедо облаков серной кислоты, затрудняет доступ солнечных лучей к поверхности планеты. Поэтому (а также в результате большого количества мельчайших частиц вулканического пепла в верхних слоях атмосферы, также затрудняющих доступ солнечному свету к планете) после особо сильных вулканических извержений могут произойти значительные изменения климата. Например, в результате извержения вулкана Ксудач (п-ов Камчатка, 1907 г.) повышенная концентрация пыли в атмосфере держалась около 2 лет, а характерные серебристые облака серной кислоты наблюдались даже в Париже[1]. Взрыв вулкана Пинатубо в 1991 году, отправивший в атмосферу 3·107 тонн серы, привёл к тому, что 1992 и 1993 года были значительно холоднее, чем 1991 и 1994 [2].

Слайд 37В печь, где жар-огонь горит (поз. 1), Вносят раздробленный Серный колчедан, пирит (FeS2). Вот он, раскаленный, Серой струйкой пылевой Сверху вниз несется. Воздух мощною струей Снизу подается. Мощный стал противоток, Смерч тут настоящий, И, как огненный цветок, Слой частиц кипящий, В вихре раскаленных масс Кислород с пиритом Превратился в легкий газ В том процессе скрытом. Газ содержит пыль и грязь, От оксида серы (SO2)
Производство серной кислоты контактным способом
Их циклон отделит враз (поз. 2): В нем для них барьеры. Два цилиндра в нем, и вот, Сверху вниз обычно, По спирали газ идет. Пыль из газа упадет, Но не вся, частично. Смесь в электрофильтр подав (поз. 3), Где сплошные сетки И под током провода, Пыль, как птицу в клетку, Ловят каждый раз подряд, Ведь частички пыли Обретают здесь заряд, Подчиняясь силе Электрических полей. Минус-знак поймала Пыль, прилипнув массой всей К сетке из металла. В бункер или просто в ров Опадает сразу. Но очистить от паров Еще надо газы.

Слайд 38И в сушильной башне смесь (поз. 4) С легкостью безмерной Будет высушена здесь Кислотою серной, Сверху льется кислота, Поглощая воды, И огонь ей не чета, Он не той породы. После этих процедур У оксида серы Будет следующий тур: К нему из атмосферы Подают воздушный слой, И в узле контактном Он окислит сам собой Газ неоднократно: 2SO2 + O2 2SO3 + Q.
А контактный аппарат (поз. 6)? Что в нем происходит? Кислород окислить рад Газ, который входит. Но нагреть должны мы смесь,
И в теплообменник (поз. 5) Поступает газ наш весь, Как под стражу пленник. Но вот совсем холодный Идет продукт, и тут-то Последний пункт процесса Есть на пути продукта. Оксид направлен в башню (поз. 7), Где поглощаться будет, Но не водой обычной, А кислотой его остудят здесь. Недаром оксиды серы прочно Вступают с водным паром В контакт всегда досрочно: SO3 + H2O = H2SO4 + Q. И будет сернокислый Туман вреднейший виснуть. Другое дело, сразу Чтоб серной кислотой Продукты эти, газы, Внутри за слоем слой Поглощены бы были: В реакцию вступили С водой, которой много Есть в серной кислоте. Оксиды серы строго Идут в контакт за тем, Чтоб получился в чане Безводный олеум. На этом окончанье. Пусть отдохнет ваш ум.