Презентация "Азотная кислота и ее свойства" по химии – проект, доклад
Презентацию на тему "Азотная кислота и ее свойства" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 11 слайд(ов).
Слайды презентации
Список похожих презентаций
Азотная кислота и ее соли
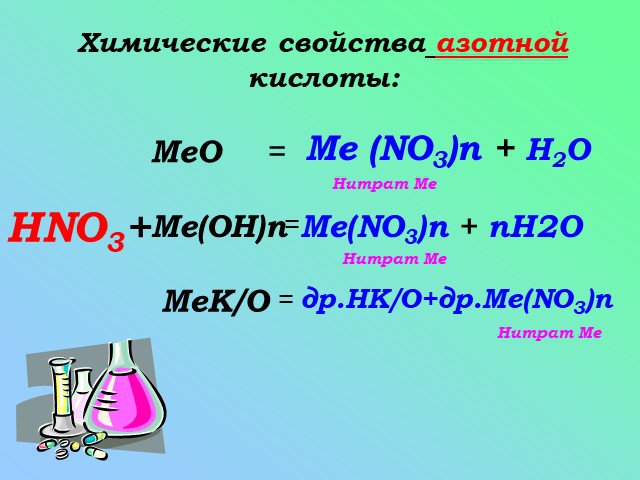
План изучения азотной кислоты. 1.Состав . 2.Строение. 3.Физические свойства. 4.Химические свойства. 5.Получение и применение. Состав и строение азотной ...Азотная кислота и ее соли
Это вещество было описано арабским химиком в VIII веке Джабиром ибн Хайяном (Гебер) в его труде «Ямщик мудрости», а с ХV века это вещество добывалось ...Азотная кислота и её свойства
Индивидуальная работа. Осуществите превращения 1 вариант: N2 → NO→NO2 2 вариант: N2→NH3→(NH4)SO4 3 вариант: NH3→N2→K3N. HNO. Содержание. Структурная ...Азотная кислота основные понятия
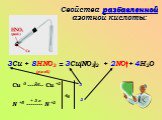
Физические и физико-химические свойства. Молекула имеет плоскую структуру (длины связей в нм): азот в азотной кислоте четырёхвалентен, степень окисления ...Азотная кислота и её соли
Познакомиться с азотной кислотами, её солями- нитратами, их физическими и химическими свойствами ; Экспериментально изучить свойства азотной кислоты ...Азотная кислота и её соли
Вспомните! Какие степени окисления проявляет азот в своих оксидах? Какие окислы азота вы знаете? Расскажите о N2O, NO, NO2? Какое из этих соединений ...Азотная кислота
НЕМНОГО ИСТОРИИ. Монах-алхимик Бонавентура в 1270 году в поисках универсального растворителя «алкагеста» решил нагреть смесь железного купороса с ...Азотная кислота
«Азотная кислота».Тема урока:. I. Строение молекулы.
Электронная формула :O : H :O: N : :O.
Структурная формула O // H ─ O ─ N \\ O.
Молекулярная ...
Азотная кислота
Разминка:. А1. Степень окисления азота в азотной кислоте 1) +4 2) +5 3) +2 4) +3. Подготовка к Е Г Э. А 2. По физическим свойствам азот и аммиак 1) ...Азотная кислота
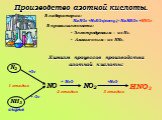
HNO3. Состав. Строение. Свойства. H O N —. степень окисления азота. валентность азота. +5 IV химическая связь. ковалентная полярная. Азотная кислота ...азотная кислота
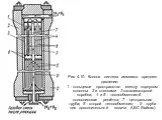
Рисунок 1.2 – Четырехполочная колонна синтеза аммиака мощностью 1360 т/сут 1 – люк для выгрузки катализатора; 2 – центральная труба; 3 – корпус катализа-торной ...Азотная кислота по химии
Тема: «Азотная кислота» Цель урока: Рассмотреть свойства азотной кислоты и области ее применения. План урока: 1. Проверка Д/З (письменная работа); ...Металлическая связь и ее свойства
Это связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке СХЕМА ...Вода и ее химические свойства
Молекулярное строение воды. Молекула воды состоит из 2 молекул водорода и 1 молекулы кислорода, которые находятся друг относительно друга под углом ...Положение металлов в таблице Д.И. Менделеева. Особенности строения атомов, свойства
Цель урока: 1. на основе положения металлов в ПСХЭ прийти к пониманию особенностей строения их атомов и кристаллов (металлической химической связи ...Происхождение нефти. Ее свойства
Нефть. - это природная горючая маслянистая жидкость, которая состоит из смеси углеводородов самого разнообразного строения. Их молекулы представляют ...Различные свойства воды и значение воды в живой и неживой природе
Вода! У тебя нет ни вкуса, ни цвета, ни запаха, тебя невозможно описать, тобою наслаждаются, не ведая, что ты такое. Нельзя сказать, что ты необходима ...Азот и его свойства
История открытия азота:. В 1772 г. Англичанин Д. Резерфорд установил, что воздух, оставшийся под колоколом, где жила несколько дней мышь, освобожденный ...Оцтова кислота
Найвідоміша карбонова кислота. Оцтова або етанова кислота— органічна речовина з формулою CH3COOH. Слабка, насичена одноосновна карбонова кислота. ...Альдегиды и их свойства
Содержание Строение молекул Изомерия и номенклатура Физические свойства Получение Химические свойства Применение Контрольные вопросы. Альдегиды – ...Конспекты
Азотная кислота и ее свойства, получение и применение. Соли азотной кислоты
Тема: «Азотная кислота и ее свойства, получение и применение. Соли азотной кислоты» (урок – исследование). Цели урока. Образовательная:. ...Азотная кислота и ее соли. Окислительные свойства азотной кислоты
Урок 21. Азотная кислота и ее соли. Окислительные свойства азотной кислоты. Цели урока:. 1. Охарактеризовать азотную кислоту по следующей схеме: ...Азотная кислота: состав молекулы, физические и хими- ческие свойства
Урок по химии разработан к учебнику И. И. Новошинского, Н. С. Новошинской. Технология критического мышления. Тема урока:. «Азотная кислота: состав ...Азотная кислота строение, свойстваи применение
Открытый урок по химии в 9 классе по теме:. . . « Азотная кислота строение, свойстваи применение». Учитель МКОУ СОШ с.п. Кара-Суу Жабоева Раиса ...Азотная кислота
Автор: Трегуб Алеся Васильевна, учитель химии МБОУ СОШ №2 г. Вилючинска. Цель урока:. продолжить формирование у учащихся понятия «кислота» на примере ...Углекислый газ, угольная кислота и ее соли
Дата_____________ Класс_______________. Тема:. . Углекислый газ, угольная кислота и ее соли. . Цели урока:. знать состав, строение, свойства ...Угольная кислота и ее соли
Открытый урок по химии в 9 классе по теме:. . . « Угольная кислота и ее соли». Учитель МКОУ СОШ с.п. Кара-Суу Жабоева Раиса Муратовна. ...Угольная кислота и ее соли
Муниципальное общеобразовательное учреждение. «Гимназия №32». г.Нижнекамск Республика Татарстан. Конспект урока по химии в 9 классе«. Угольная ...Угольная кислота и ее соли
Государственное казённое образовательное учреждение Ростовской области общеобразовательная школа-интернат основного общего образования. . п. Шолоховского ...Серная кислота и ее соли
Тема: Серная кислота и ее соли. Цель урока:. Продолжить изучать соединения серы на примере серной кислоты и ее солей. Изучить свойства серной кислоты. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:25 апреля 2015
Категория:Химия
Автор презентации:Неизвестен
Содержит:11 слайд(ов)
Поделись с друзьями:
Скачать презентацию