Презентация "Признаки реакций" по химии – проект, доклад
Презентацию на тему "Признаки реакций" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 14 слайд(ов).
Слайды презентации
Список похожих презентаций
Сущность химических реакций и признаки их протекания. Тепловой эффект реакции
Верные и неверные утверждения:. Горение ацетона – это физическое явление. Замерзание воды – это химическое явление. Диффузия паров духов – это физическое ...Составление уравнений окислительно-восстановительных реакций
Окислительно–восстановительные реакции – это реакции протекающие с изменением степеней окисления элементов. При составлении уравнений окислительно- ...Химические реакции. Составление уравнений химических реакций
Цели и ожидаемые результаты. Повторить понятия как простые и сложные вещества, составление химической формулы вещества, химические реакции. Научиться ...Скорость химических реакций
Цель урока:. Выяснить, что такое скорость химической реакции. Выяснить, какие факторы и как влияют на скорость химической реакции. Скорость химической ...Типы химических реакций
Содержание. Актуализация опорных знаний Изучение нового материала Первичное закрепление знаний и умений Подведение итогов урока. Рефлексия Домашнее ...Уравнения химических реакций
Составьте схемы химических реакций Сульфат натрия + хлорид бария → хлорид натрия + сульфат бария Азот + кислород → оксид азота (V) Алюминий + … → ...Классификация химических реакций
это процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и (или) строению. Химические реакции -. По числу ...Типы химических реакций
Цели урока. Обобщить представление о химической реакции как о процессе превращения одного или нескольких исходных веществ-реактивов в отличающиеся ...Ионные уравнения реакций
Протекающая реакция описывается следующим уравнением 2KOH + H2SO4 = K2SO4 + 2H2O. 2KOH + H2SO4 = K2SO4 + 2H2O. Отражает ли эта запись в истинном свете ...Классификация химических реакций
. . . . . . . . . . . . . . . ...Закон сохранения массы веществ. Уравнения химических реакций
Единственный путь, ведущий к знанию, - это деятельность. Цели урока: Обучающие - экспериментально доказать закон сохранения массы веществ. На основе ...В мире химических реакций
Классификация химических реакций по числу и составу реагирующих веществ реакции. « …Мы отнюдь не властвуем над природой, все наше господство состоит ...Cкорость химических реакций
Определение:. Скорость химической реакции – это изменение количества реагирующего вещества в единицу времени в единице объёма. r – скорость химической ...Тепловой эффект химических реакций
Введение. Тема реферата – ознакомление с тепловым эффектом и его применением в современной жизни. Цели и задачи:. Цель: разносторонне изучить явление ...Классификация химических реакций
Химические реакции – процессы в результате которого из одних веществ получаются другие, отличающиеся по составу и строению. І.По числу и составу реагирующих ...Типы химических реакций
Цель урока: повторить классификацию веществ, типы химических реакций и признак их классификации, научить учащихся применять полученные знания о типах ...Классификация химических реакций
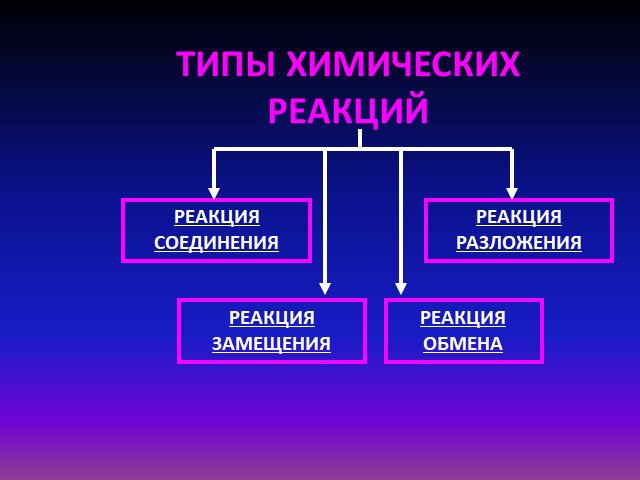
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ. РЕАКЦИИ СОЕДИНЕНИЯ. РЕАКЦИИ РАЗЛОЖЕНИЯ. РЕАКЦИИ ЗАМЕЩЕНИЯ. РЕАКЦИИ ОБМЕНА. 1) Водород + кислород вода. Н 2 + О2 Н2О 2. 2) ...Типы химических реакций
Эти явления знаете вы В природе и в нашем быту встречаются они, А отличают эти явления – взаимные превращения, Образуются всегда – новые вещества. ...Классификация химических реакций
«Химическое превращение, химическая реакция есть главный предмет химии». Н.Н.Семёнов. Какие явления относятся к (Ф) физическим, а какие к (Х) химическим. ...Типы химических реакций на примере свойств воды
Вода Сложное вещество, состоящее из двух химических элементов. Является оксидом. Молекулярная формула воды Формула воды - Н2О В молекуле воды: 2 атома ...Конспекты
Признаки химических реакций
Признаки химических реакций. Николаева Валентина Геннадьевна, учитель химии 2 категории, СОШ№28, г. Нижнекамск РТ. Цель:. . познакомить учащихся ...Физические и химические явления. Признаки химических реакций
Урок. : химия. Дата. :. Учитель. : Алимбаева А.К. . Класс. : 8. Тема урока. : Физические и химические явления. Признаки химических реакций. . ...Химические реакции. Признаки химических реакций
Тема: Химические реакции. Признаки химических реакций. Тип урока. : изучение нового материала и первичного закрепления знаний. Вид урока. : ...Явления физические и химические. Признаки химических реакций
Итоговая работа. Явления физические и химические. Признаки химических реакций. . . Цель:. . 1. Сформировать представление учащихся о физических ...Признаки химических реакций
Тема урока:. . Признаки химических реакций. Цель урока:. . Изучить на . практике признаки . химических реакций. Задачи урока:. 1. Сформировать ...Физические и химические явления. Признаки химических реакций
Разработка урока химии по теме «Физические и химические реакции. Признаки химических реакций», 8 класс, к учебнику О.С. Габриелян, Химия 8 класс- ...Типы химических реакций
Тема Урока : «Типы химических реакций» урок повторения в 8 классе. . А. . . П. . Т. ен,. ГУ. « Средняя школы имени М Габдуллина с дошкольным ...Типы химических реакций
. Тема:. . «Типы химических реакций». Класс:. . 8. Форма проведения урока:. . . индивидуально-групповая. . форма работы. ...Типы химических реакций
ГОУ НПО РПЛ. Урок по теме:. «Типы химических реакций». Преподаватель химии. Лебедева ...Классификация химических реакций
Открытый урок по химии в 11 классе по теме:. «Классификация химических реакций». Учитель МКОУ СОШ с.п. Кара-Суу Жабоева Раиса Муратовна. Задачи ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:15 января 2015
Категория:Химия
Содержит:14 слайд(ов)
Поделись с друзьями:
Скачать презентацию