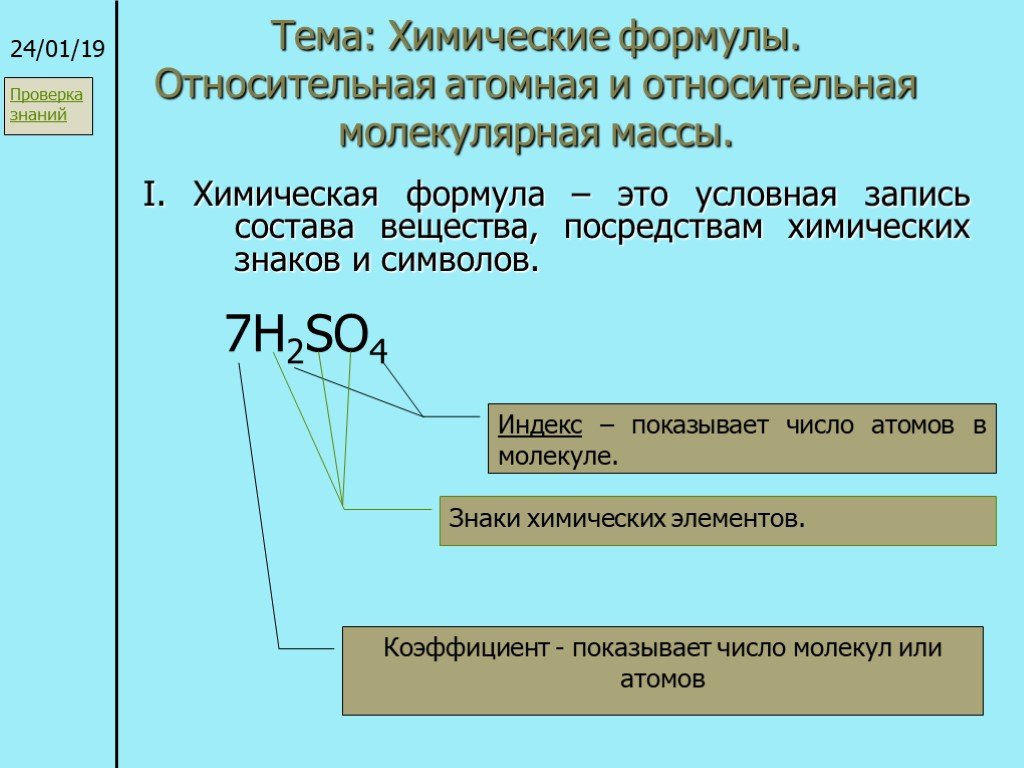
Презентация "Химические формулы. Относительная атомная и относительная молекулярная массы" по химии – проект, доклад
Презентацию на тему "Химические формулы. Относительная атомная и относительная молекулярная массы" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 9 слайд(ов).
Слайды презентации
Список похожих презентаций
Химические формулы. Относительная атомная и относительная молекулярная массы
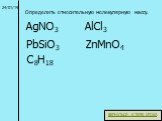
ХИМИЧЕСКОЕ ЛОТО. 16 – «5» 12 - 15 – «4» 9 – 11 – «3». Проверка:. ХИМИЧЕСКАЯ ФОРМУЛА. Н2О Порядок действий:. Прочитать химическую формулу. Дать характеристику ...Относительная атомная и молекулярная массы
тема урока. Относительная атомная и молекулярная массы. Химический диктант. Начертите таблицу по образцу, аккуратно перепишите в неё формулы. Задания. ...Химические знаки и химические формулы
Найдите лишнее:. 1. Железо, водород, никель 2. Сера, алюминий, кремний 3. Кислород, озон, азот. Знаки химических элементов. Физическое тело Вещество. ...Химические формулы
Химические формулы – это аналоги слов, которые записывают с помощью букв – знаков химических элементов. H2O O2 C12H22O11 вода кислород сахароза. Состав ...Химические формулы
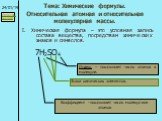
Молекула воды Н2О. 5 молекул воды Н2О коэффициент - показывает число молекул 10 молекул воды Н2О 12 молекул воды Н2О. Углекислый газ состоит из 1 ...Химические свойства металлов
По своим химическим свойствам все металлы являются восстановителями, все они сравнительно легко отдают валентные электроны, переходят в положительно ...Химические свойства кислот с позиции теории электролитической диссоциации
Кислоты. Тема урока: «Химические свойства кислот с позиции теории электролитической диссоциации». «От кислых яблок сразу скисну». В. Шекспир. Кислота, ...Химические свойства воды
Доказать уникальность воды, как химического вещества. Выяснить причины уникальности воды как химического соединения. Теоретический (анализ статей, ...Химические свойства алкенов
Цели урока. Знать: строение алкенов, характерные типы химических реакций (реакции присоединения, полимеризации, окисления), применение алкенов на ...Химические элементы и организм человека
Многие учёные считают, что в живом организме не только присутствуют все химические элементы, но каждый из них выполняет определённую биологическую ...Химические свойства солей
Определение солей. Мех(КО)у. КО - кислотный остаток. Na2SO4 2Na+ +SO42- CaCl2 Ca2+ + 2Cl-. Na2SO4 CaCl2 Сульфат натрия Хлорид кальция. Соли – ...Алкены. Строение. Изомерия. Химические свойства. Получение
Элементный анализ этилена показывает, что в его состав входят примерно 87,5% углерода и 14,3% водорода. Плотность этилена по отношению к водороду ...Понятие об углеводах. Моносахариды. Химические свойства глюкозы
Классификация углеводов. Углеводы Cn(H2O)m Моносахариды Дисахариды Полисахариды. Моносахариды – углеводы, не подвергающиеся гидролизу. триозы тетрозы ...Основания. Химические свойства оснований
Классификация оснований. Растворимые в воде (щелочи). Нерастворимые в воде. NaOH Ca(OH)2 Al(OH)3 Сu(OH)2. Название оснований. Гидроксид +. Название ...Основания. Химические свойства. Способы получения
Химические свойства. Гидроксид – ионы (ОН-), образующиеся при диссоциации оснований, обуславливают их химические свойства 1. Действие на индикаторы. ...Неорганические соединения - формулы и реакции
Цели урока. В игровой форме обобщить и закрепить знания о химических свойствах основных классов неорганических соединений и их взаимопревращениях. ...Металлы. Химические и физические свойства металлов
Физические свойства металлов. Очень важным свойством металлов является их сравнительно легкая механическая деформируемость. Металлы пластичны, они ...Интерактивная игра "Химия в ребусах: Химические элементы"
НИКЕЛЬ. ИОД. АЗОТ. БОР. МАГНИЙ Й. МАРГАНЕЦ. КРЕМНИЙ Л=й. МЫШЬЯК. УГЛЕРОД О. ЦИРКОНИЙ. АРГОН. МЕДЬ ДВЕ. КРИПТОН. ЗОЛОТО. СЕРА П=А. ВОДОРОД А=О Т=Д. ...Химические свойства неметаллов
Цель. На этом уроке мы поведем разговор о простых веществах – неметаллах, их химических свойствах. Вы должны усвоить общие химические свойства неметаллов ...Применение ацетилена. Химические реакции, лежащие в основе применения
Химические реакции, лежащие в основе применения ацетилена. Реакции получения и горения ацетилена CaC2 + 2H2O → Ca(OH)2 + C2H2 2C2H2 + 5O2 → 4CO2 +2H2O ...Конспекты
Химические формулы. Относительные атомная и молекулярная мас-сы. Массовая доля элемента в соединении
Автор: Учитель химии и биологии Карякина Екатерина Николаевна. МБОУ СОШ № 139 городского округа Самара. Конспект урока по химии для 8 класса. ...Химические формулы
Химические формулы. Цель урока. объяснить ученикам, что означают химические формулы. , а также понятия относительной атомной и молекулярной массы. ...Молярный объем газов. Относительная плотность газов
П. . Степной Курганинского района Краснодарского края МОУ СОШ № 17. Разработка урока химии. Тема:. «Молярный объем газов. Относительная плотность ...Кислоты. Химические свойства кислот в свете теории электролитической диссоциации
Урок химии в 8-м классе по теме: "Кислоты. Химические свойства кислот в свете теории электролитической диссоциации.". . Цели урока:. Образовательная. ...Химические свойства щелочных металлов
. МБОУ «Леплейская СОШ». Урок на тему:. «Химические свойства щелочных металлов». Класс:9. Продолжительность урока:45 ...Химические свойства соединений щелочных и щелочноземельных металлов. Жесткость воды
Муниципальное общеобразовательное учреждение. Бельская средняя общеобразовательная школа. г. Белый Тверской области. Конспект урока по химии ...Химические свойства предельных одноатомных спиртов
МОУ « Лицей № 47» г. Саратов. . Никитина Надежда Николаевна - учитель химии. ПОДГОТОВКА К ЕГЭ ( 10, 11 класс). Лекция по теме: Химические свойства ...Химические свойства оксидов
Чиркова Марина Юрьевна. МБОУ СОШ № 22. Г. Узловая Тульской обл. Тема урока: «Химические свойства оксидов». Тип урока:. Объяснение нового ...Химические свойства металлов и их соединений
Муниципальное общеобразовательное автономное учреждение. «Средняя общеобразовательная школа № 5 города Соль – Илецка». Оренбургской области. ...Химические свойства металлов
Химические свойства металлов (9 класс). Заведующий экспериментальной. . площадкой,. учитель химии,. . ГБОУ СОШ № 200. Чупина Н.А. Цель:. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:25 января 2019
Категория:Химия
Содержит:9 слайд(ов)
Поделись с друзьями:
Скачать презентацию