Слайд 1КГМУ им. С.И. Георгиевского Кафедра общей хирургии ОСНОВЫ ТРАНСПЛАНТАЦИИ ОРГАНОВ И ТКАНЕЙ Доцент Татарчук П.А.
Слайд 2В понятие «пластическая хирургия» (трансплантация) входят операции, направленные на восстановление целости и формы разрушенных или полуразрушенных органов человеческого тела, в том числе при пороках развития, с помощью перемещения тканей, взятых по соседству с дефектом, пересаженных из других мест на питающей ножке или взятых свободно и пересаженных на место дефекта. Сюда относятся также операции исправляющие форму и положение органа. Могут пересаживаться живые и мертвые ткани от другого человека.
Слайд 3История «пластической хирургии»
имеет свое начало еще в древности. Имеются сведения о пересадке кожи в древней Индии (пластическое восстановление носа), пластических операциях в древнем Египте и др. Со временем совершенствовались способы трансплантации, но пересадка целых органов и их комплексов, восстановление функции органов, разработка способов борьбы с тканевой несовместимостью стали возможны только в новейшее современное время.
Слайд 4Основные вехи этих открытий и исследований, в которые значительный вклад внесли и отечественные ученые
1852 г. Пирогов Н.И. разработал костно-пластическую операцию для создания опорной культи при ампутации стопы. 1869 г Reverden J.L. впервые перенес на гранулирующую поверхность несколько кусочков кожи. 1865 г. Шимановский Р.К. издал руководство по кожной пластике в Киеве.
Слайд 51872 г. Янович-Чайнский С.М. предложил пересадку кожных островков в толщу грануляций. Филатов В.П. предложил метод мигрирующей пересадки кожи на ножке. Склифосовский Н.В. разработал способ «мостовидной» пересадки кожи Лимберг А.А. теоретически обосновал и внедрил метод пластики встречными треугольниками.
Слайд 61943 г. Kolff – предложил гемодиализ при острой почечной недостаточности (ОПН). 1946-1960 г. Демихов В.Д.– впервые произвел пересадку сердечно-легочного комплекса и пересадку второго сердца в грудную полость.
Слайд 71949 г. – Burnet and Fenner описали иммунную толерантность. 1958 г. – Dausset открыл антигены тканевой несовместимости и начало тканевого типирования. 1959 г. – Выявлено иммуннодепрессивное действие 6-меркаптопурина и положено начало фармакологической иммунодепрессии.
Слайд 81960 г. – Положено начало успешной аллогенной трансплантации почек. Применена иммунодепрессия азатиоприном и кортикостероидами. 1967 г. – K.Bernard произвел первую успешную пересадку сердца человеку. 1966-1968 гг. – открыт антилимфоцитарный глобулин (АЛГ). 1968 г. Road основал Европейскую организацию тканевого типирования.

Слайд 9Классификация
По виду трансплантации и используемому материалу для пересадки существует: Аутотрансплантация – пересаживают собственные ткани и органы, т.е. трансплантат взятый у этого же индивидума (аутотрансплантат). Например, больному с ожогом пересаживают на пораженную поверхность собственную кожу, взятую из непораженных ожогом участков. Изотрансплантация - пересаживают почку от одного однояйцевого близнеца другому. Они имеют генетически одинаковые тканевые антигены, что способствует хорошему приживлению у реципиента (изотрансплантант). Сингенная трансплантация - трансплантат (сингенный трансплантат) берут у родственников первой степени (отец, мать, братья, сестры, но не однояйцевые), который хотя и отличается содержанием антигенов, но не значительно. Это способствует преодолению тканевой несовместимости и приживлению.

Слайд 10Аллотрансплантация - производится пересадка тканей и органов генетически разнородных индивидов, но от одного и того же вида. Можно пересадить кожу от другого человека (донора) реципиенту, или, например, в эксперименте, почку от одной собаки другой. Трансплантат в этом случае называется – аллотрансплантат. По старой терминологии такая пересадка называлась – гомотранспл антацией. При этом виде пересадки может быть пересажена ткань или орган от живого индивидуума (донора) – а л л о в и т а л ь т а н а я трансплантация (алловитальный трансплантат) и от трупа (консервированный или лиофилизированный аллостатический трансплантат) – а л л о с т а т и ч е с к а я трансплантация. В этом случае трансплантат служит как бы каркасом для регенерации собственных тканей реципиента.

Слайд 11Ксенотрансплантация - пересадка тканей и органов, полученных от организма другого биологического вида. Трансплантат называется ксенотрансплантат. Примером может служить пересадка человеку консервированной кости, взятой у теленка, сердце пересаженное от обезьяны человеку (в США) или пересадка ткани от кролика собаке и др. По старой терминологии такая пересадка называлась гетеротрансплантацией. Эксплантация (протезирование) - производят пересадку трансплантатов (эксплантат, протез) из искусственного материала (пластмассы, искусственных нитей и др.). Например, пересаживают искусственные сердечные клапаны, сосуды из дакрона, искусственный хрусталик и др. По старой терминологии этот вид трансплантации носит название алотрансплантация.

Слайд 12По месту пересадки различают: О р т о т о п и ч е с к у ю трансплантацию. В этом случае трансплантат, состоящий из ткани или органа помещают на его собственное место. Например, пересадка сердца, печени на то место, где они были удалены. Г е т е р о т о п и ч е с к а я трансплантация. Органы или ткани помещаются на новое место. Например, почку размещают в подвздошной области, хрящ пересаживают в кость и др. Р е п л а н т а ц и я - орган или ткань после удаления (травматическая ампутация пальцев, конечности, ушной раковины, хирургического удаления и др.) пришивают на то же место. И м п л а н т а ц и я - в орган или ткань внедряют, подсаживают клетки и участки ткани. Например, при сахарном диабете в сосуды, питающие печень, вводят В-клетки поджелудочной железы, продуцирующие инсулин; при тотальном удалении щитовидной железы в мышцы имплантируют участки неизмененной ткани железы и др.

Слайд 13Основным условием приживления трансплантата является его биологическая совместимость, которая зависит от степени генетической близости между донором и реципиентом. Трансплантация будет всегда успешной, при соблюдении всех других требований к пересадке, если это будет аутотрансплантацией.

Слайд 14В пределах одного вида пересадка будет успешной, если оба индивида имеют одинаковый генотип, т.е. если они являются однояйцевыми близнецами или происходят от одной чистой линии животных. Органы и ткани приживают, так как выполняется изогенная трансплантация. В остальных случаях пересадки в пределах одного биологического вида имеется разный генотип. Поэтому при аллотрансплантации нельзя считать, что трансплантат приживет. Вероятность успешной пересадки несколько больше, если донорами являются родители, братья и сестры реципиента, так как они имеют все же более близкий генотип, чем другие люди (сингенная трансплантация). Неуспешной является трансплантация, если донор и реципиент являются особями разного биологического вида (ксенотрансплантация). Например, пересадка кожи от собаки обезьяне и наоборот.

Слайд 15основной причиной отторжения является иммунитет это предположение подтверждено в 1943 году при многократных пересадках кожи. Обращено внимание на то, что при повторных пересадках кожи одному и тому же реципиенту от одного и того же донора, время отторжения трансплантата укорачивается. Иммунологическая природа отторжения была доказана путем введения клеток лимфатических узлов донора, который уже имел одно или более отторжений трансплантата, реципиенту с пересаженным первым трансплантатом. Наступало ускорение отторжения первого трансплантата. Исследования показали, что трансплантация чужой ткани (антигенов) вызывает в организме реципиента типичный процесс иммунизации, приводящий к приживлению или отторжению трансплантата. Этот иммунитет был назван «трансплантационным». За глубокое изучение толерантности к отторжению аллотрансплантата Medawar et Barnet получили Нобелевскую премию.

Слайд 16Проблема отторжения аллотрансплантата может быть рассмотрена с двух точек зрения: хирургической и более сложной – иммунно-биологической. Последняя хорошо прослеживается на примере пересадки кожи. Сразу после трансплантации кожи, существующие в дерме сосуды не участвуют в питании кожного лоскута. Питательные вещества поступают с плазмы путем диффузии. В течение 5 дней врастают капилляры в дерму кожного лоскута из соединительной ткани реципиента и создаются анастомозы между трансплантатом и реципиентом. На второй неделе развивается реакция трансплантата. Появляется нарушение кровообращения, гиперемия, стаз, тромбоз, васкулиты, кровоизлияния, что приводит к воспалению и появлению экссудата.

Слайд 17Вследствие этого позднее возникают некрозы, отслойка эпидермиса от дермы лоскута и между ними скапливаются гематомы, экссудат. Это приводит к отделению трансплантата от его ложа и разрастанию грануляционной ткани под ним. Сроки этих изменений от 2 недель до года. Если развивается иммунобиологическая толерантность у очень истощенных больных, то может наступить полное приживление аллотрансплантата (В.Рейнгард, 1955 и др.). Морфологические изменения характеризуются ранним накоплением лимфоцитов, лимфоидных мононуклеарных клеток, макрофагов, плазмоцитов, гистоцитов вокруг трансплантата или в стенках его кровеносных сосудов. После инфильтрации наступает разрушение его клеток, закупорка сосудов и полное «удушье» вследствие наступающей ишемии. Особую роль в разрушении принимают лимфоциты.

Слайд 18Ф а к т о р ы, от которых зависит у с п е ш н о с т ь пластических операций:
1. От строгого учета показаний и противопоказаний для проведения соответствующей операции. 2. От оперативной техники: анатомичности операции (правильности разрезов, точного выкраивания лоскутов), тщательности остановки кровотечения, безукоризненности шва, асептичности и других мелких деталей техники. 3. От качества консервированного трансплантата, который может консервироваться различными методами: а) консервация при низкой температуре в незамороженном виде, в растворах; б) путем лиофилизации (обезвоживание в замороженном состоянии под вакуумом); в) консервация методом замораживания при температуре от –183 до 2730 С; г) путем химической обработки; д) консервация путем включения в пластмассы (парафин). 4. От иммунной реакции реципиента как гуморальной, так и клеточной, которая приводит к отторжению трансплантата.

Слайд 19Способы воздействия на трансплантационный иммунитет для успешной пересадки органов и тканей
Подбор доноров с минимальным числом различий основных трансплантационных антигенов Совместимость реципиента и донора по АВО осуществляется наподобие правила Оттенберга при гемотрансфузии: а/ реципиенту с группой крови О(I) возможна пересадка от донора с группой О(I); б/ реципиенту с группой крови А(II) возможна пересадка только от донора с группой крови А(II), а с группой крови О(I) – нежелательно; в/ при группе крови у реципиента В(III) возможна пересадка от доноров с группой крови О(I) и В(III); г/ при группе крови у реципиента АВ(IV) могут быть использованы доноры с группами крови А(II), В(III) и АВ(IV). По Rh – фактору совпадение не обязательно.

Слайд 20HLA (антигены лейкоцитов, так называемые антигены гистосовместимости).
Совместимость по антигенам HLA является определяющей. Основные антигены гистосовместимости располагаются в VI хромосоме, их полиморфизм очень широкий. Основное значение имеют: локус А, в котором уже идентифицированы 24 аллеля; локус В, с идентифицированными 52 аллелями и локус DR c идентифицированными 20 аллелями. Комбинация генов крайне разнообразна и совпадение одного во всех трех локусах практически невозможно. Поэтому при трансплантации проводят типирование реципиента и донора по основным антигенам. Для этого типирования существует панель из 200 антител. Производится также перекрестное типирование, при котором в присутствии комплемента тестируют несколько проб сыворотки реципиента взятых в разное время с лимфоцитами донора. Если не проявляется цитотоксичность сыворотки реципиента к лимфоцитам донора, то считается положительным результат. Но в случае гибели лимфоцитов донора, хотя бы в одном случае, трансплантацию не делают.

Слайд 21В Европе действует несколько банков (Евротрансплантат) содержащих карты реципиентов с результатами типирования. После появления донора, у которого предполагается изъятие органов, производится типирование и подбирают реципиента с которым он наиболее совместим. Реципиент вызывается в центр трансплантации и ему выполняется операция.
Слайд 22Применяют способы снижения силы иммунной реакции, что достигается иммуннодепрессивными средствами. При отсутствии осложнений применяют небольшие дозы препаратов по специальным схемам. Если появляются признаки отторжения, то дозы иммуннодепрессантов значительно возрастают и изменяется их комбинация. Нужно помнить, что эти препараты увеличивают риск возникновения инфекционных осложнений. В связи с этим в отделениях трансплантации должны соблюдаться особые меры асептики.

Слайд 23Используют следующие препараты для иммуннодепрессии: Ц и к л о с п о р и н (циклоспорин –А, сандиммун) считается основным иммуннодепрессантом в трансплантологии. Представляет из себя циклический полипептидный антибиотик грибкового происхождения. Подавляет транскрипцию гена интерлейкина-2, который необходим для пролиферации Т-лимфоцитов и блокирует Т-интерферон. Отрицательным свойством его является нефротоксичность. А з а т и о п р и н в печени превращается в 6-меркаптопурин, который подавляет синтез нуклеиновых кислот и деление клеток. Применяется в сочетании с другими препаратами при кризах отторжения. Может вызывать лейкопению и тромбоцитопению. П р е д н и з о л о н - стероидный гормон оказывает сильное неспецифическое депрессивное действие на гуморальный и клеточный иммунитет. Применяется в различных схемах иммуннодепрессии. При кризах отторжения используют высокие дозы. О р т о к л о н содержит антитела к CD3+ - лимфоцитам. Используется во время кризов отторжения в сочетании с другими препаратами. А н т и л и м ф о ц и т а р н ы й г л о б у л и н и а н т и л и м ф о ц и т а р н ы е с ы в о р т к и. За счет угнетения Т-лимфоцитов происходит иммуннодепрессивное их действие.

Слайд 24Однако, несмотря на предпринимаемые меры, не всегда удается достичь приживления и может наступить реакция отторжения. Выделяют: сверхострое (на операционном столе), раннее острое (в течение одной недели), острое (в течении 3 месяцев) хроническое (отсроченное по времени) отторжение, которое проявляется ухудшением функции трансплантированного органа и морфологическими изменениями, полученными при биопсии. Быстрое ухудшение состояния реципиента, связанное с активизацией иммунной системы в отношении пересаженного органа называется «кризисом отторжения». При его возникновении проводится иммунодепрессивная терапия.
Слайд 25КОЖНАЯ ПЛАСТИКА
При пересадке кожи чаще используется аутопластика (собственная кожа), так как не имея генетических, антигенных различий хорошо приживает и не возникает несовместимости. Все виды кожной пластики можно осуществить путем пересадки на питающей ножке (несвободная пластика), методом свободной трансплантации и при комбинации этих способов.
Слайд 26Пластика кожи на питающей ножке
Этот вид пластики предполагает, что трансплантируемый участок кожи сохраняет связь с тканями больного и кровоснабжение. Формируется из кожи и подкожной клетчатки. Ширина питающей ножки должна быть достаточной для обеспечения хорошего кровоснабжения. Она не должна быть перекрученной вокруг оси при трансплантации и не сдавлена повязкой.
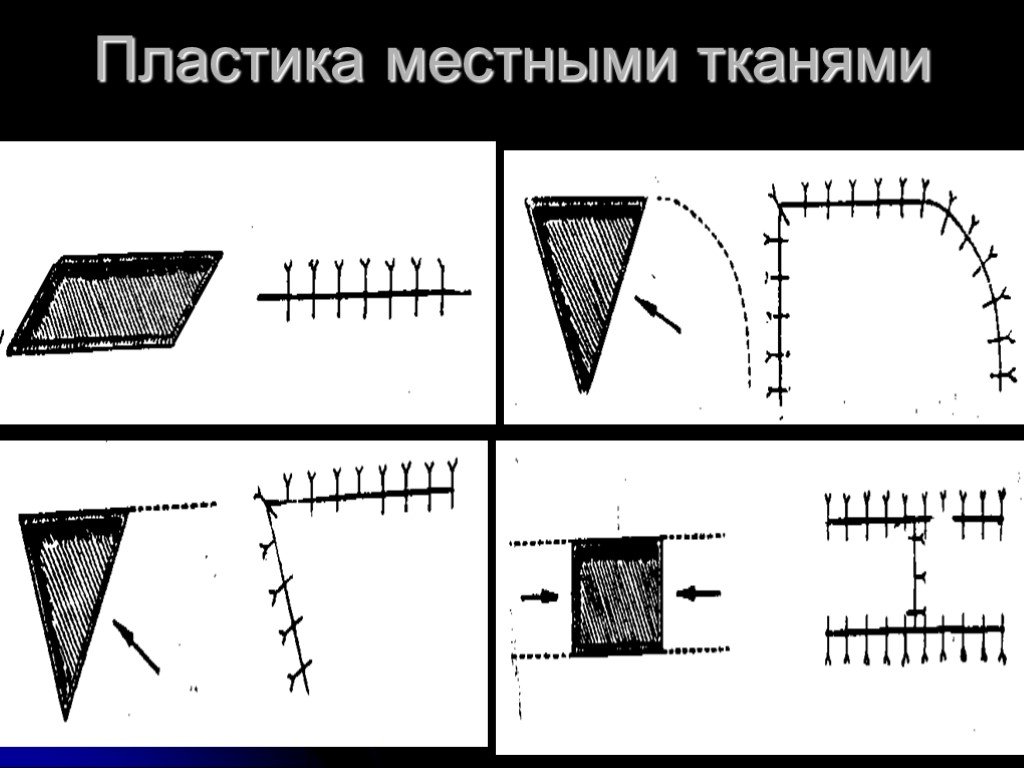
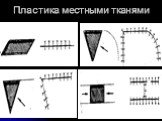
Слайд 27Пластика местными тканями
Слайд 28Использование послабляющих разрезов
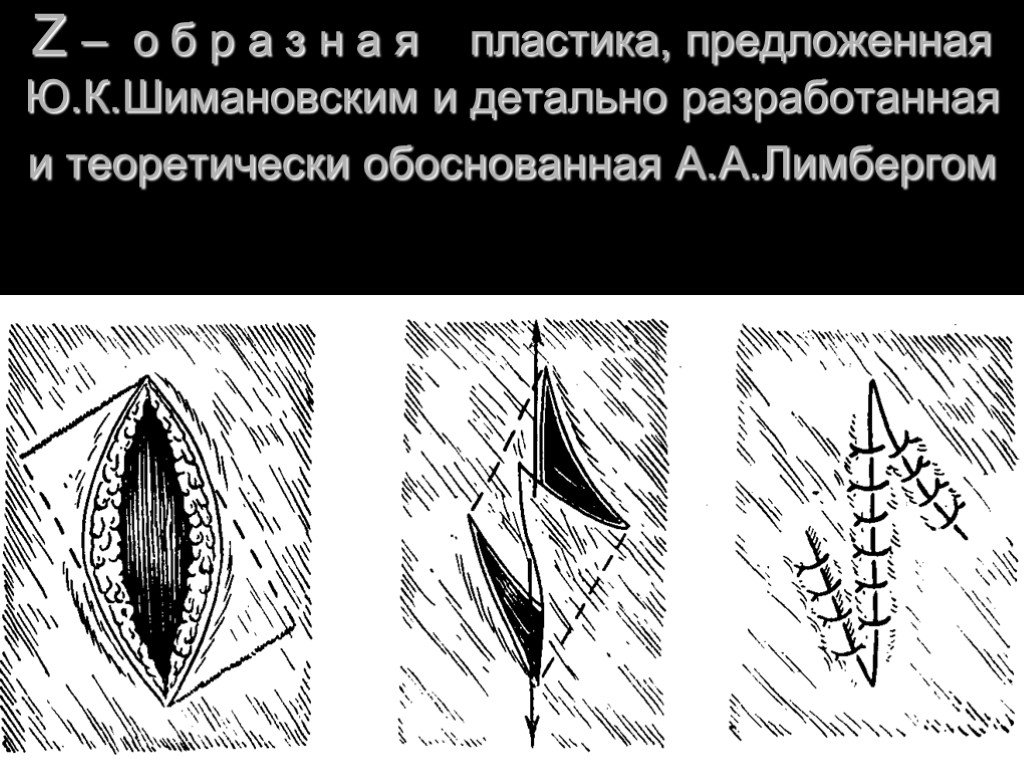
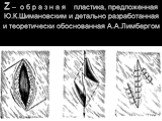
Слайд 29Z – о б р а з н а я пластика, предложенная Ю.К.Шимановским и детально разработанная и теоретически обоснованная А.А.Лимбергом
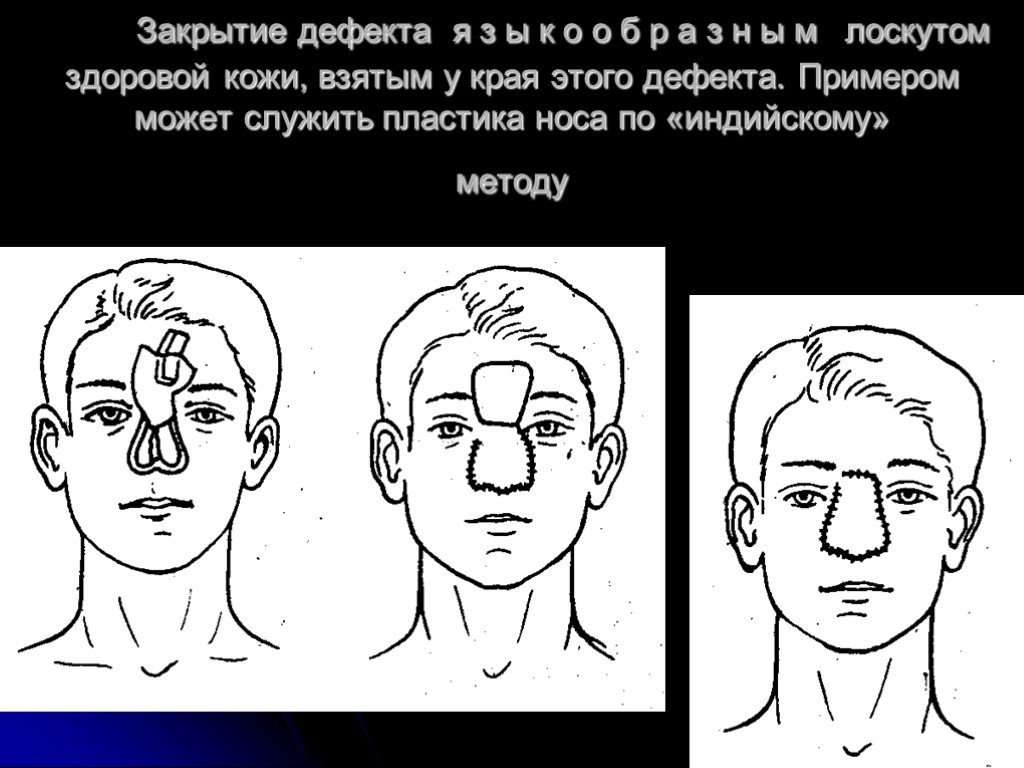
Слайд 30Закрытие дефекта я з ы к о о б р а з н ы м лоскутом здоровой кожи, взятым у края этого дефекта. Примером может служить пластика носа по «индийскому» методу
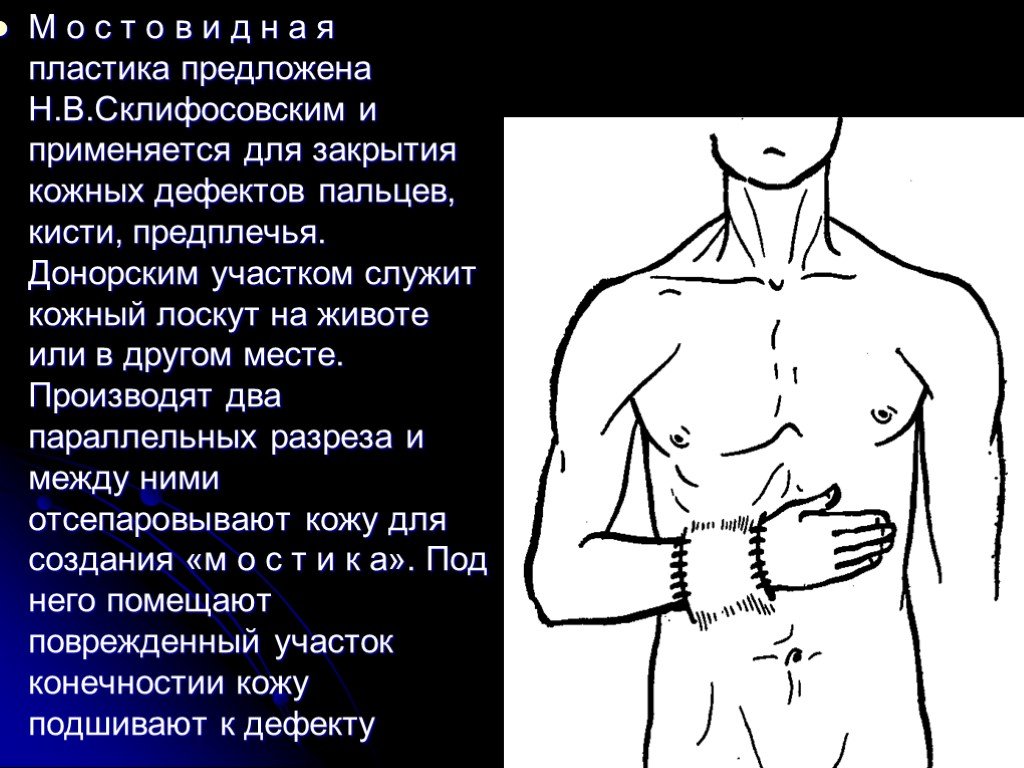
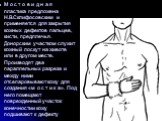
Слайд 31М о с т о в и д н а я пластика предложена Н.В.Склифосовским и применяется для закрытия кожных дефектов пальцев, кисти, предплечья. Донорским участком служит кожный лоскут на животе или в другом месте. Производят два параллельных разреза и между ними отсепаровывают кожу для создания «м о с т и к а». Под него помещают поврежденный участок конечностии кожу подшивают к дефекту
Слайд 32П р я м у ю кожную пластику на отдаленных участках лоскутом на питающей ножке можно выполнить, если донорский участок и место дефекта возможно близко сопоставить. Производится одномоментное закрытие дефекта. Для этого используется «итальянский» метод пластики. При замещении дефекта носа языкообразный лоскут на ножке выкраивается в области плеча. Донорский участок ушивается, а трансплантат подшивается к краям дефекта носа.
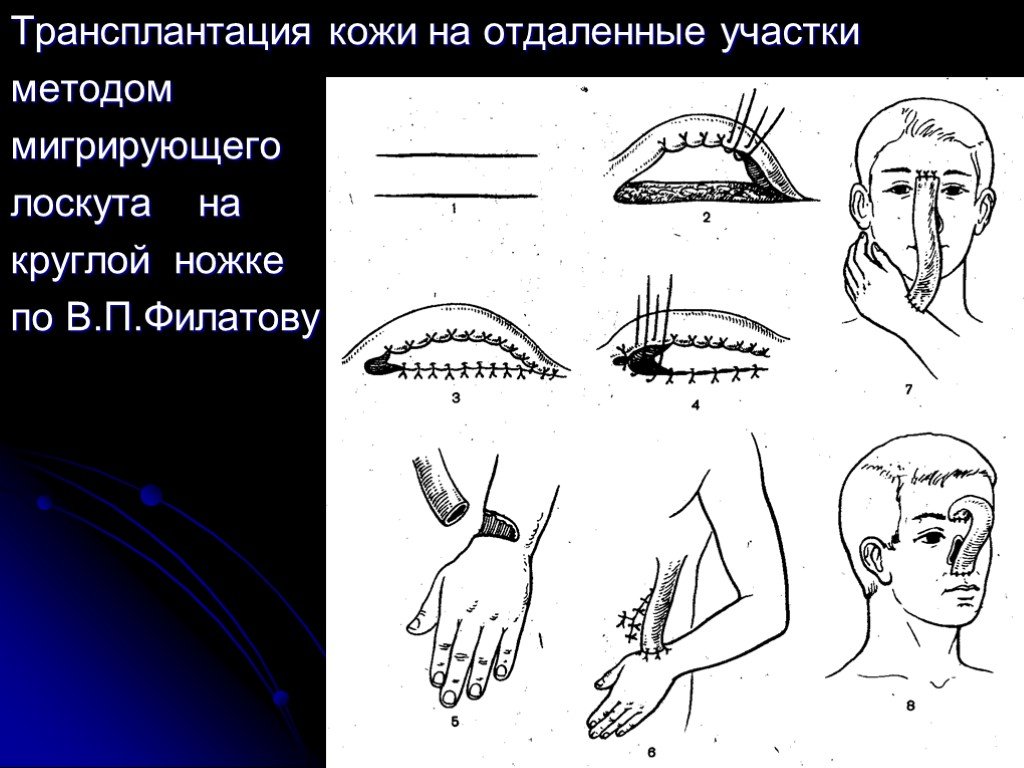
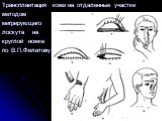
Слайд 33Трансплантация кожи на отдаленные участки методом мигрирующего лоскута на круглой ножке по В.П.Филатову

Слайд 34Свободная пересадка кожи
может быть выполнена двумя путями: пересадкой тонких кусочков эпидермиса; лоскутов всей толщи кожи (всего эпидермиса) или «расщепленных лоскутов». Впервые пересадку кожи тонкими, толщиной 0,3 см, кусочками эпидермиса, на гранулирующую поверхность осуществил Реверден, в 1869 году. В дальнейшем этот способ был усовершенствован. По Я ц е н к о – Р е в е р д е н у под местной анестезией бритвой брали кусочки кожи размерами 0,3-0,5 см на наружной поверхности бедер, плеча или живота и черепицеобразно покрывали дефект. Я ц е н к о и Т и р ш предложили также брать кусочки кожи значительно больших размеров: длиной до 15 см, шириной до 3 см. По Я н о в и ч у – Ч а й н с к о м у – Д е в и с у под местной анестезией берутся участки эпидермиса с поверхностными слоями дермы. Забор производится с помощью иглы, которой приподнимают эпидермис в виде конуса и срезают у его основания в шахматном порядке. Полученный округлый кусочек кожи диаметром до 0,3-0,5 см, имеющий наиболее толстый слой в центре и тонкий - по его краю,.с помощью иглы переносят на дефект, оставляя между трансплантируемыми лоскутами пространство до 0,5 см. Такой лоскут более жизнеспособный, он обеспечивает быструю регенерацию эпителия, так как толстые слои создают как бы депо для эпителия.

Слайд 35Способ Л о у с о н а – К р а у з е использовался с 1870 года. Особенностью его является то, что на донорском участке производят забор большого по размерам лоскута, во всю толщину кожи. А на пораженном участке, куда его пересаживают, края лоскута фиксируют швами к краям дефекта. Однако под таким лоскутом может скапливаться раневое отделяемое и препятствовать заживлению, так как приводит к отслаиванию трансплантата. Чтобы увеличить площадь взятого лоскута и обеспечить лучший отток из под него, что способствует лучшему приживлению эпидермиса Ленц (1908), Девис (1919), Дуглас (1930) рекомендовали перфорировать лоскут, взятый во всю толщу кожи. Его стали назвать «лоскутом-ситом», «дырчатым» и «перфорированным». С этой цель Д у г л а с на донорском участке острым пробойником высекал кружочки на расстоянии 1,5 см один от другого. Затем лоскут отсепаровывал с оставлением кружочков на донорском участке, переносил его на дефект и фиксировал по краям дефекта швами. На месте донорского участка рана быстро заживала за счет нарастания эпителия с краев раны и из оставшихся кружков. По способу Д р а г с т е д т а – У и л с о н а берут лоскут кожи без клетчатки длиной на 1/3 больше дефекта, но на половину уже его. Затем наносят на лоскуте разрезы в шахматном порядке, растягивают и подшивают к краям дефекта. Раневое отделяемое из под лоскута без препятствий выходит наружу, что не нарушает приживления пересаженной кожи.
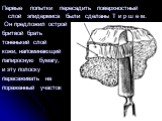
Слайд 36Первые попытки пересадить поверхностный слой эпидермиса были сделаны Т и р ш е м. Он предложил острой бритвой брать тоненький слой кожи, напоминающий папиросную бумагу, и эту полоску пересаживать на пораженный участок

Слайд 37Однако обосновали применение «р а с щ е п л е н н о г о» лоскута Блэр и Браун (V.P.Blair and J.Brown,1929). Они считают, что лучшей толщиной кожного лоскута является толщина трансплантата равной 1/3 или 2/3 толщины кожи. С этой целью они с помощью шаблона на донорском участке делали разрез, соответствующий величине и форме дефекта до дермы. Острым скальпелем пилящими движениями вырезали лоскут неполной толщины. Делали мелкие насечки и после удаления грануляций с раневой поверхности, на которую переносят кожный лоскут, тщательно подшивая его к краям дефекта. На лоскут накладывают повязку с антибиотиками, а на донорское место – мазевая повязка. Раневая поверхность на месте взятия трансплантата быстро эпителизируется и через 4-5 недель на этом месте можно повторно взять слой кожи для пересадки
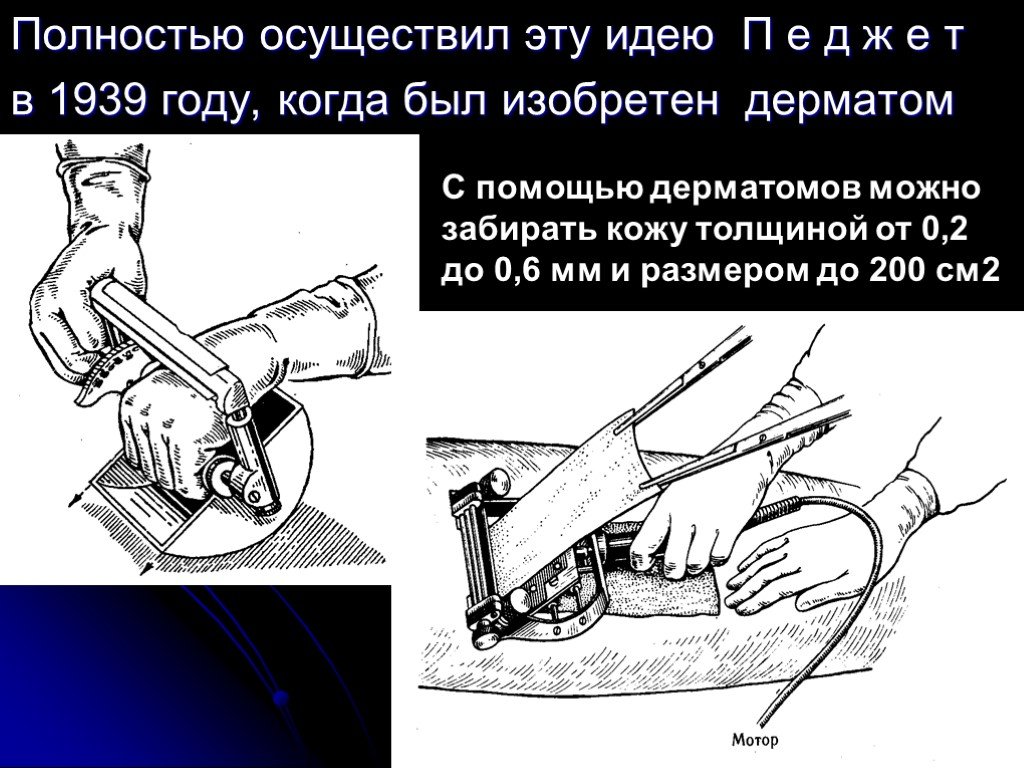
Слайд 38Полностью осуществил эту идею П е д ж е т в 1939 году, когда был изобретен дерматом
С помощью дерматомов можно забирать кожу толщиной от 0,2 до 0,6 мм и размером до 200 см2