Презентация "Алкены" по химии – проект, доклад
Презентацию на тему "Алкены" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 13 слайд(ов).
Слайды презентации
Список похожих презентаций
Непредельные углеводороды. Алкены
Непредельные – углеводороды, содержащие между атомами углерода одну или несколько π- связей. Непредельные углеводороды. Алкены С=С Алкины С≡ С Алкадиены ...Класс Алкены
Тема урока: Непредельные углеводороды. Этилен Строение Получение Свойства Применение. Девиз урока: Все познается в сравнении. Цели и задачи урока. ...Непредельные углеводороды. Алкены
Содержание. 1.Определение 2.Номенклатура алкенов 3.Изомерия алкенов 4.Строение алкенов 5.Получение алкенов 6.Физические свойства 7.Химические свойства ...Алкены
Содержание. Алкены Номенклатура Изомерия Физические свойства Строение алкенов Химические свойства (реакции присоединения: галогенирование, гидрирование, ...Алкены
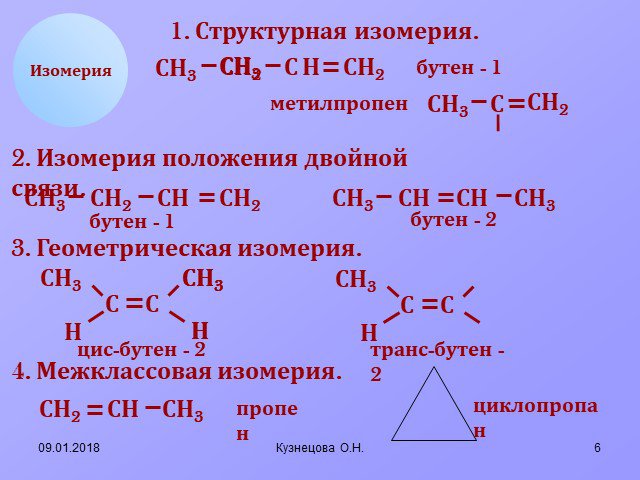
Строение молекулы этилена, как одного из представителей алкенов. Изомерия и гомологический ряд алкенов. Изомерия углеродного скелета: CH2=CH-CH2-CH3 ...Алкены
Алкены. Студент должен: знать стоение, номенклатуру, свойства, способы получения и применения алкенов умень составлять названия и химические уравнения ...Алкены
Часть 1. А 1. К непредельным углеводородам относят органические соединения в которых А) одна кратная связь Б) несколько кратных связей В) тройная ...Алканы, Алкены, Алкины
АЛКАНЫ. Получение, нахождение в природе и применение алканов. ВПЕРЕД НАЗАД. Газообразные алканы получают из природного и попутного нефтяных газов; ...Конспекты
Непредельные углеводороды. Алкены
Базовый лист контроля на примере темы : «Непредельные углеводороды. Алкены». На первом же уроке новой темы учитель вывешивает «Базовый лист контроля». ...Непредельные углеводороды. Алкены, их строение, номенклатура и изомерия
Дата:. . . Предмет: химия. . . . . Название, тема:. . Непредельные углеводороды. Алкены, их строение, номенклатура и изомерия. . . ...Непредельные углеводороды. Алкены
Преподаватель химии. Катаркольского Сельскохозяйственного. . Колледжа Бурабайского района. Иманкулова Алмагуль Толегеновна. (1 категория, ...Алкены :состав, строение ,номенклатура , изомерия ,физические свойства
Алкены :состав, строение ,номенклатура ,. изомерия ,физические свойства. Девиз: Величие человека в его способности мыслить. Цель урока :. познакомить ...Алкены
Муниципальное общеобразовательное учреждение. лицей № 9. имени заслуженного учителя школы Российской Федерации А.Н.Неверова Дзержинского района ...Алкены
Краевое государственное бюджетное образовательное учреждение начального профессионального образования «Профессиональное училище №86». Методическая ...Алканы, Алкены, Алкины
Урок химии: обобщение знаний по темам «Алканы»,. . «Алкены, «Алкины». Викторова Екатерина Петровна. ГБОУ СОШ с. Новокуровка. Учитель химии ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Кузнецова О.Н.
Содержит:13 слайд(ов)
Поделись с друзьями:
Скачать презентацию






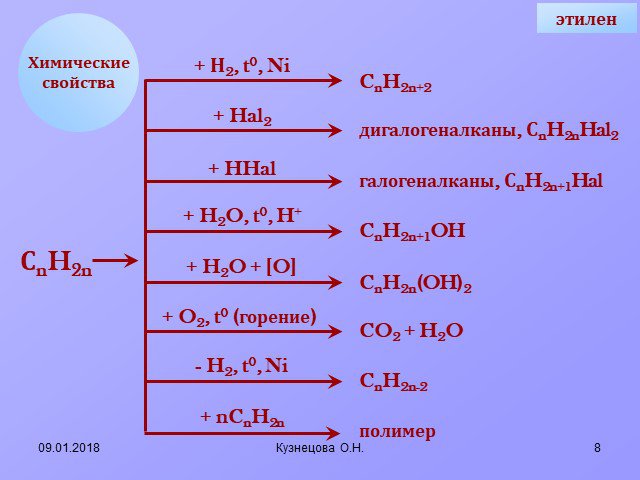












![+ Н2, t0, Ni + Hal2 + HHal + H2O, t0, H+ + H2O + [O] + O2, t0 (горение) - H2, t0, Ni + nCnH2n CnH2n+2. дигалогеналканы, СnH2nHal2. галогеналканы, СnH2n+1Hal. CnH2n+1OH CnH2n(OH)2 CO2 + H2O CnH2n-2 полимер СnH2n этилен + Н2, t0, Ni + Hal2 + HHal + H2O, t0, H+ + H2O + [O] + O2, t0 (горение) - H2, t0, Ni + nCnH2n CnH2n+2. дигалогеналканы, СnH2nHal2. галогеналканы, СnH2n+1Hal. CnH2n+1OH CnH2n(OH)2 CO2 + H2O CnH2n-2 полимер СnH2n этилен](https://prezentacii.org/upload/cloud/14/09/4586/images/thumbs/screen8.jpg)
![ОН 4. Гидратация: Pt, t. Химические свойства этилена. 1. Гидрирование: + Н2. 2. Галогенирование: + Br2 СН2Вr. 3. Гидрогалогенирование: + НСl CН3 СН2Сl + Н2О t, Н3РО4 СН2ОН. 5. Мягкое окисление: + [О] +Н2О 6. Горение: + 3О2 2СО2 2Н2О 7. Дегидрирование: t, Ni 8. Полимеризация: nСН2 cat ( … …)n главная ОН 4. Гидратация: Pt, t. Химические свойства этилена. 1. Гидрирование: + Н2. 2. Галогенирование: + Br2 СН2Вr. 3. Гидрогалогенирование: + НСl CН3 СН2Сl + Н2О t, Н3РО4 СН2ОН. 5. Мягкое окисление: + [О] +Н2О 6. Горение: + 3О2 2СО2 2Н2О 7. Дегидрирование: t, Ni 8. Полимеризация: nСН2 cat ( … …)n главная](https://prezentacii.org/upload/cloud/14/09/4586/images/thumbs/screen9.jpg)