Презентация "Растворение. Растворы" (8 класс) по химии – проект, доклад
Презентацию на тему "Растворение. Растворы" (8 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 16 слайд(ов).
Слайды презентации
Список похожих презентаций
Решение задач на смеси, сплавы, растворы
1%−это сотая часть рассматриваемой величины (52% от х кг − это 0,52х кг); Если в смеси растворов объемом V (массой m) нас интересует компонент объемом ...Решение расчетных задач на сплавы, смеси и растворы различными методами.
Актуальность темы:. В курсе химии в результате сокращения часов, на решение задач отводится недостаточное количество времени, происходит неполноценное ...Истинные растворы
Оглавление. Введение 3 слайд Основная часть 4-9 слайд Вывод 10 слайд Список используемой литературы 11 слайд. Введение. Цель: Исследовать и изучить ...Решение задач на смеси, растворы и сплавы
Задача № 1. Задача № 2. Имеются сплавы золота и серебра. В одном эти металлы находятся в отношении 2: 3, а в другом в отношении 3: 7. Сколько нужно ...Дисперсные системы и растворы
Агрегатное состояние — состояние вещества, характеризующееся определёнными качественными свойствами: способностью или неспособностью сохранять объём ...Дисперсные системы и растворы
Дисперсные системы. Дисперсия = раздробление, измельчение. Дисперсные системы состоят как минимум из двух компонентов:. 1. дисперсионной среды, которая ...Буферные растворы
Концентрация – масса, объём или количество вещества в определённой массе или объёме раствора. В связи с этим концентрация может быть массовой, объёмной ...Растворы и их свойства
Растворы (дисперсные системы). Растворы – это физико-химические дисперсные системы состоящие из двух или более компонентов. Дисперсная система, фаза, ...Растворы
Растворы – это гомогенные (однородные) системы, состоящие из двух и более компонентов и продуктов их взаимодействия. Точное определение раствора ( ...Растворы
Растворы – это гомогенные (однородные) системы, состоящие из двух и более компонентов и продуктов их взаимодействия. Точное определение раствора ( ...Растворы
Раствор – гомогенная система, переменного химического состава, состоящая из двух и более компонентов: растворитель и растворенное вещество (вещества). ...Вода - растворитель. Растворы
Я и туча, и туман, И ручей, и океан, И летаю, и бегу, И стеклянной быть могу! Мы говорим: она течёт; Мы говорим: она играет; Она бежит всегда вперёд, ..."Растворимость веществ в воде. Растворы
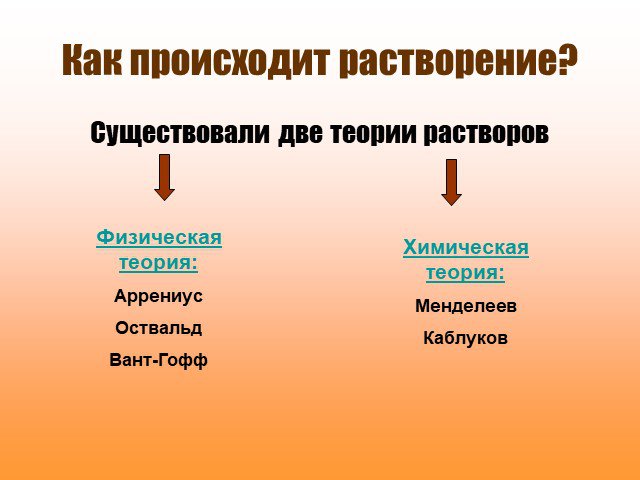
Как образуется раствор? Что такое раствор? Растворы – это однородные системы, состоящие из молекул растворителя и частиц растворенного вещества, между ...Конспекты
Вода. Растворы
Общеобразовательная школа. I. -III ступеней обучения №8. . Симферопольского городского совета. Республики Крым. Конспект итогового урока ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:6 мая 2015
Категория:Химия
Классы:
Содержит:16 слайд(ов)
Поделись с друзьями:
Скачать презентацию