Презентация "Предельные углеводороды" по химии – проект, доклад
Презентацию на тему "Предельные углеводороды" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 15 слайд(ов).
Слайды презентации
Список похожих презентаций
Предельные углеводороды химия
Органическая химия – это раздел химической науки, в котором изучаются соединения углерода и их превращения. В наши дни к органическим веществам относятся ...Химия Предельные углеводороды
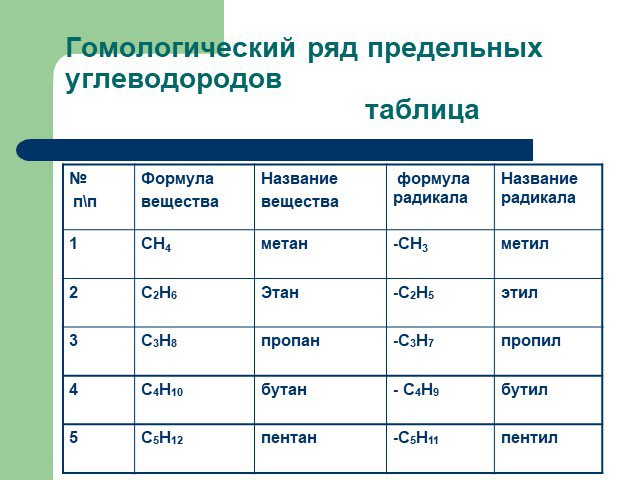
1.Строение предельных углеводородов. 2.Гомологический ряд метана. 3.Таблица 1 гомологический ряд алканов. 4.Изомерия и номенклатура. 5.Получение. ...Предельные углеводороды
План урока. Понятие о углеводородах. 2.Предельные углеводороды. 3.Природные источники углеводородов. 4. Вопросы. Д/З § 33, В.3, 4. 1. Понятие о углеводородах. ...Предельные углеводороды
Цели урока: Научить учащихся выводить формулу вещества по его относительной плотности и массовым долям элементов, выводить формулу вещества по его ...Предельные углеводороды
Классификация органических веществ. УГЛЕВОДОРОДЫ – это вещества, состоящие только из углерода и водорода. Определение предельных углеводородов (ПУВ). ...Предельные углеводороды (алканы, или парафины)
Алканы – название предельных углеводородов по международной номенклатуре Междунаро́дный сою́з теорети́ческой и прикладно́й хи́мии (ИЮПАК, International ...Непредельные углеводороды
Почему этилен – газ, а полиэтилен – твёрдое вещество? Гипотеза: Свойства веществ определяются их строением. Проблема. Для того, чтобы выяснить, возможно ...Непредельные углеводороды
Непредельные УГЛЕВОДОРОДЫ. Алкены Алкадиены Алкины. Цель викторины:. Повторить, закрепить и проверить материал по теме: «Непредельные углеводороды», ...Обобщение: предельные и непредельные углеводороды
Цели урока:. повторить, обобщить и закрепить полученные знания и умения по темам «Предельные и непредельные углеводороды» изучить генетическую связь ...Предельные одноосновные карбоновые кислоты
Тема урока: «Предельные одноосновные карбоновые кислоты». Цель урока: •Знать строение одноосновных карбоновых кислот, их определение, изомеры, гомологи, ...Предельные одноосновные карбоновые кислоты
Назовите вещества. СН3-СН2-ОН. Соотнесите формулу вещества и его название. Формула 1) СН3-СН2-ОН 2) С3Н8 3) СН3-ОН 4). Название а) пропан б) метанол ...Предельные одноатомные спирты
Определение спиртов Классификация спиртов Номенклатура Изомерия Физические свойства Аномалии у спиртов Химические свойства Физиологическое действие ...Ароматические углеводороды – арены. Бензол как представитель ароматических углеводородов
Бензол как представитель ароматических углеводородов. Задачи урока:. на примере бензола познакомиться с углеводородами, которые имеют замкнутые цепи ...Спирты. Предельные одноатомные спирты
Общая характеристика. Общая формула гомологического ряда предельных одноатомных спиртов — CnH2n+1OH. В зависимости от того, при каком углеродном атоме ...Насыщенные углеводороды
Определение. Алканы- это углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле CnH2n+2. Строение. ...Диеновые углеводороды
« Мало знать, надо и применять. Мало хотеть, надо и делать.» И.В.Гёте. «3» Лимон 1. Какие углеводороды называют диеновыми? 2. Перечислите качественные ...Диеновые углеводороды
I. Номенклатура и изомерия. Классификация. Непредельные соединения, содержащие в молекуле две двойные связи, называют диеновыми углеводородами. Их ...Ароматические углеводороды, арены, бензол
Общая характеристика класса:. Ароматическими углеводородами называются соединения, молекулы которых содержат устойчивые циклические структуры- бензольные ...Ароматические углеводороды
Арены. Ароматическими углеводородами (аренами) называются вещества, в молекулах которых содержится одно или несколько бензольных колец — циклических ...Ароматические углеводороды
Познакомиться с классом ароматических углеводородов. Изучить представителей этого класса. Знать их отличительные свойства. Знать области их применения. ...Конспекты
Предельные углеводороды
. Конспект урока химии в 10 классе. . по теме «. Предельные углеводороды». с мультимедийным сопровождением. . . . Урок изучения нового ...Предельные углеводороды. Метан – представитель насыщенных углеводородов
Разработка урока по органической химии в 9 классе с рефлективным отчетом. Составитель: учитель химии Рысмухамбетова М.Д. г.Костанай. ГУ «Основная ...Предельные углеводороды
Кроссворд «Предельные углеводороды». . На каждую парту выдается по кроссворду, время решения которого 5 мин. После этого проверяют ответы. Ребята, ...Предельные углеводороды. Метан, этан. Физические и химические свойства. Применение
Дата_____________ Класс_______________. Тема:. Предельные углеводороды. Метан, этан. Физические и химические свойства. Применение. . Цели урока:. ...Непредельные углеводороды
тема : Непредельные углеводороды. Цель. :. организация деятельности учащихся, направленной на прочное усвоение знаний по непредельным углеводородам. ...Алкены.Непредельные углеводороды
Тема урока: Алкены.Непредельные углеводороды. Цели урока:. А) образовательная. Познакомить с классом алкенов,их строении,получении,свойствах,применении. ...Ароматические углеводороды
Ароматические углеводороды (5часов). Планирование уроков:. 1. Строение, изомерия, физические и химические свойства, получение и применение аренов. ...Спирты. Предельные одноатомные спирты
Муниципальное бюджетное образовательное учреждение. «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА № 3». . . . Конспект урока по химии. в 10 классе. ...Ароматические углеводороды – арены. Бензол как представитель ароматических углеводородов
ФОРМА УРОКА:. презентация с музыкальным сопровождением. ТИП УРОКА:. изучение нового материала. ТЕМА УРОКА. «Ароматические углеводороды – арены. ...Ароматические углеводороды
ПРЕДМЕТ-ХИМИЯ. . 10 класс. Учитель - Барышникова Ирина Владимировна. ГОУ СОШ № 129 Красногвардейского района, г. Санкт-Петербурга. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:15 января 2015
Категория:Химия
Содержит:15 слайд(ов)
Поделись с друзьями:
Скачать презентацию

























![Реакции окисления. Полное окисление – горение СН4 + 2О 2→СО 2 +2Н2О +Q 2. Неполное окисление СН4 + [О] →метиловый спирт, м метаналь (формальдегид), метановая (муравьиная)кислота Реакции окисления. Полное окисление – горение СН4 + 2О 2→СО 2 +2Н2О +Q 2. Неполное окисление СН4 + [О] →метиловый спирт, м метаналь (формальдегид), метановая (муравьиная)кислота](https://prezentacii.org/upload/cloud/15/01/11402/images/thumbs/screen12.jpg)