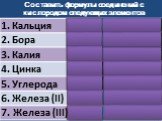
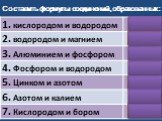
Презентация "Валентность. Составление формул" по химии – проект, доклад
Презентацию на тему "Валентность. Составление формул" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 21 слайд(ов).
Слайды презентации
Список похожих презентаций
Составление химических формул бинарных соединений по степени окисления атомов
Цель урока. Обучить учащихся составлению химических формул бинарных соединений по степеням окисления. 1. Что называется степенью окисления. 2. Чем ...Составление химических формул бинарных соединений по степеням окисления
«Свои способности человек может узнать, только попытавшись приложить их» Сенека младший. Определите степени окисления элементов. Al2O3 Ca3N2 K2Se ...Валентность и степень окисления
Из атомов мир создавала Природа. Два атома лёгких взяла водорода. Прибавила атом один кислорода. И получилась частица …. Н2О Почему такой состав имеет ...Химические реакции. Составление уравнений химических реакций
Цели и ожидаемые результаты. Повторить понятия как простые и сложные вещества, составление химической формулы вещества, химические реакции. Научиться ...Составление уравнений химических реакций
Научится составлять уравнения химических реакций. Пример. Пример: Составить уравнение реакции взаимодействия фосфора и кислорода. =. 1. В левой части ...Составление уравнений окислительно-восстановительных реакций
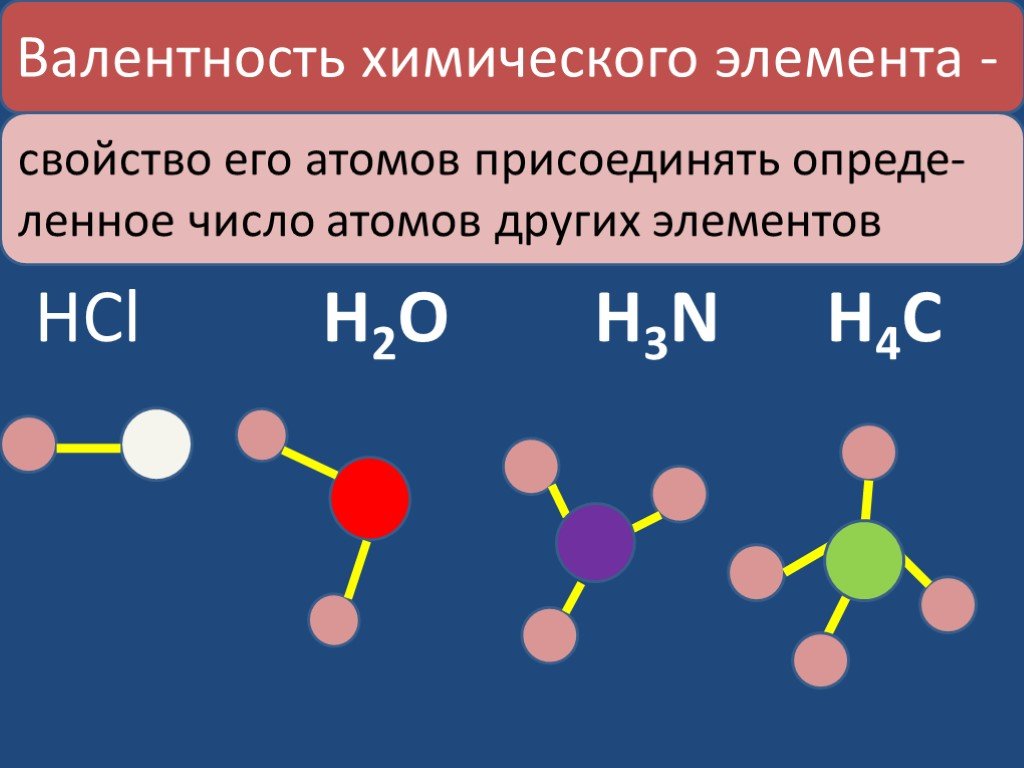
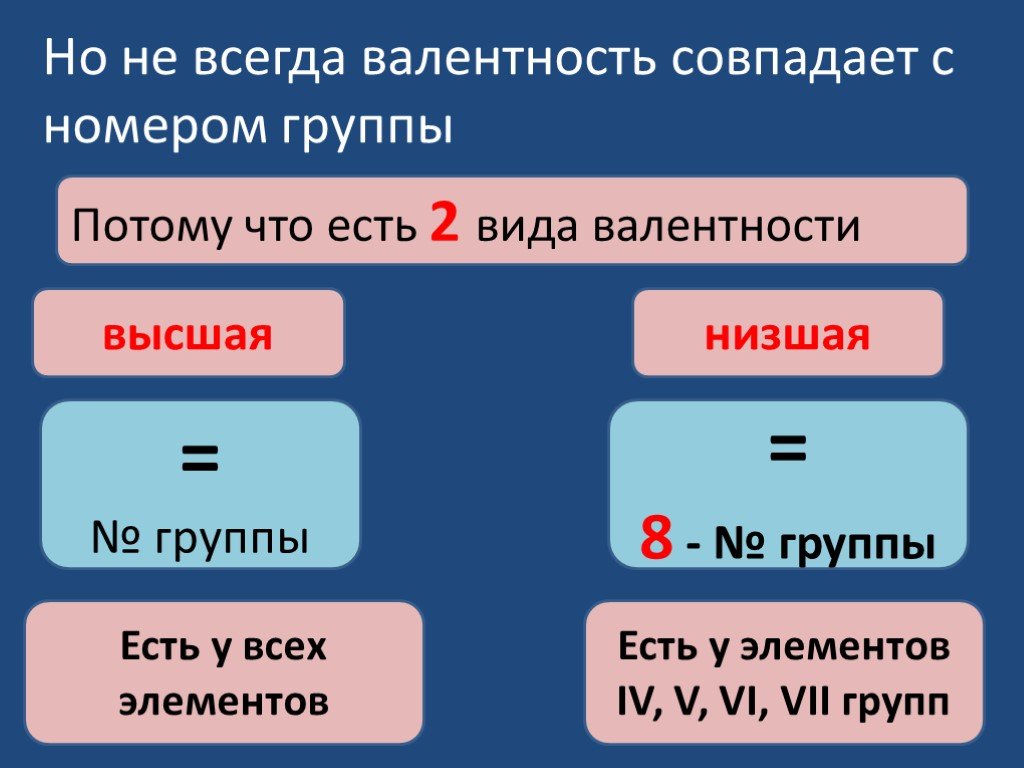
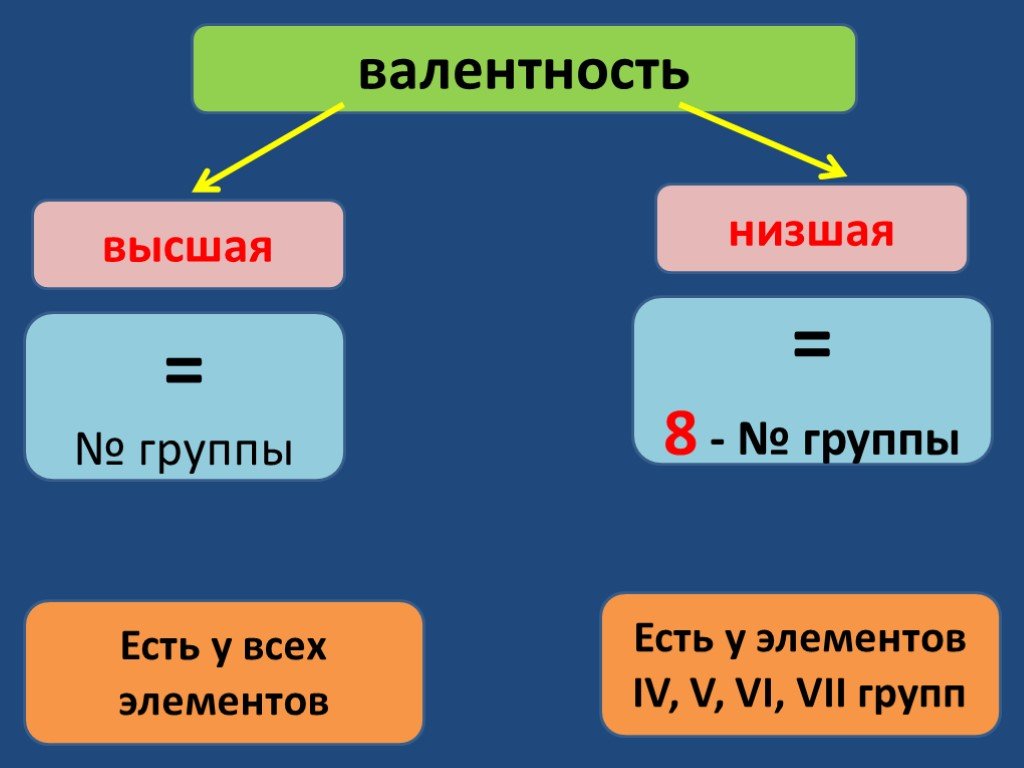
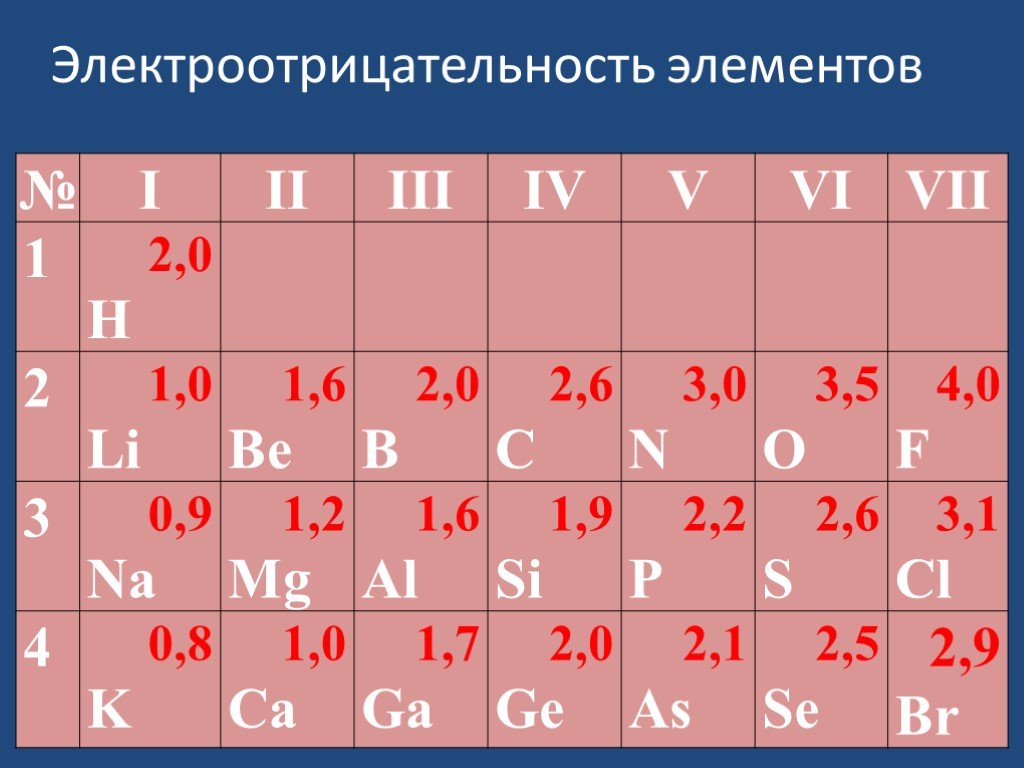
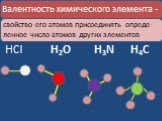
Окислительно–восстановительные реакции – это реакции протекающие с изменением степеней окисления элементов. При составлении уравнений окислительно- ...Валентность химических элементов
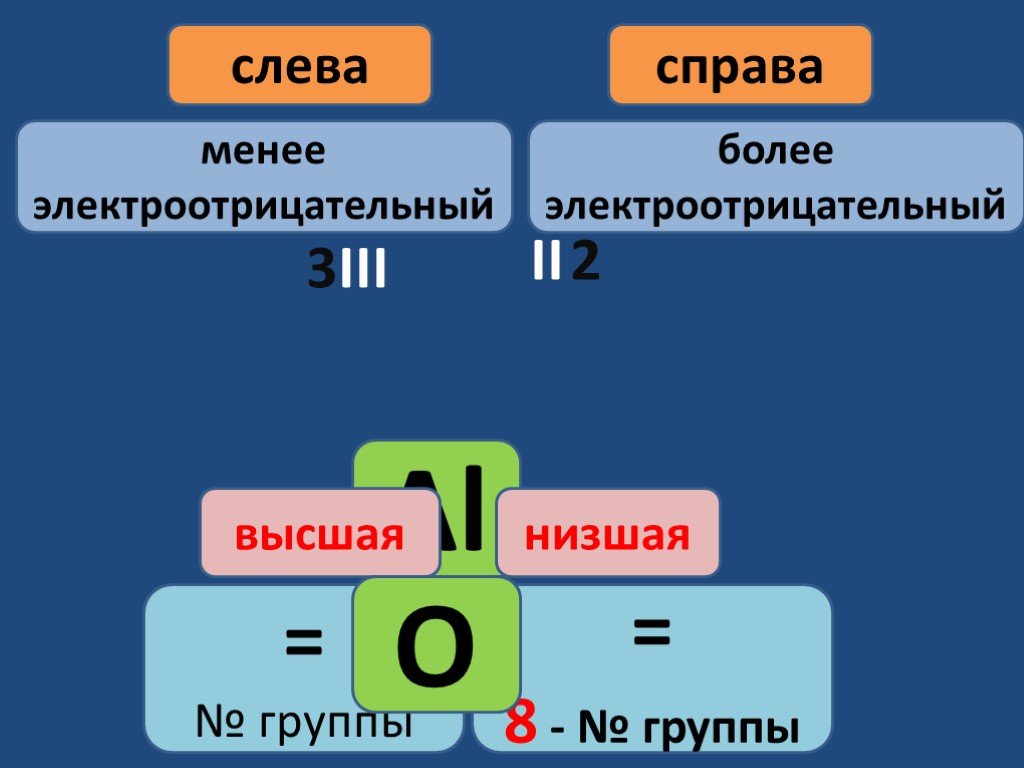
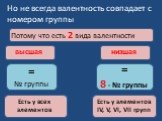
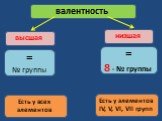
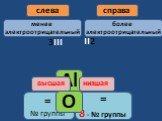
Валентность некоторых химических элементов в химических соединениях. С постоянной валентностью. C переменной валентностью. Определение валентности ...Валентность
Здравствуйте, сегодня я расскажу вам о таких понятиях в химии, как валентность и степень окисления, а также о том чем они друг от друга отличаются. ...Строение вещества химия
СТРОЕНИЕ ВЕЩЕСТВА. Основополагающий вопрос КАК УСТРОЕН МИР? Проблемные вопросы Из чего сделано все на Земле? Почему все устроено так, а не иначе? ...Своя игра. Физика и химия
Интегрированный урок ФИЗИКА+ХИМИЯ. Авторы: Орлова И.В., Шувалова Л.В. Муниципальное образовательное учреждение Фоминская средняя общеобразовательная ...Откуда ты, химия ?
Химические элементы. Роберт Бойль – впервые дал определение химического элемента. Джон Дальтон – впервые ввёл понятие атомного веса. А.М.Бутлеров ...Органическая химия "Жиры"
Рацион питания Белки Жиры Углеводы 2а, 2б 1 4б, 5. Роль жиров в здоровом питании спортсменов.Жиры хорошо усваиваются организмом, имеют высокую калорийность, ...
Органическая химия
история развития органической химии предмет органической химии особенности органических веществ Бутлеров теория строения органических соединений Бутлерова ...М.В. Ломоносов и химия
- М.В. Ломоносов был создателем многих химических производств (неорганических пигментов, глазурей, стекла, фарфора). - Он разработал технологию и ...«Жиры» химия
жиры. Оглавление. Определение и общая формула Физические свойства Химические свойства Классификация жиров Животные жиры Растительные жиры Роль жиров ...Коллоидная химия
Признаки объектов коллоидной химии. Поперечный размер частицы (а) – диаметр для сферических частиц (d) и длина ребра для кубических частиц (l). Дисперсность ...Кто ты и откуда химия?
Откуда пошло слов химия? Хи́мия (от араб. کيمياء, предположительно от египетского «chemi» — чёрный, откуда также греческое название Египта, чернозёма ...«Задачи» химия
- исследование задач по нанонауке; - ознакомление с наномиром: о достижениях нанохимии и нанотехнологии; - составление задач по нанонауке; - решение ...Незнайка в стране химия
Я – известный химик Незнайка. Я знаю все и все могу. Сейчас я взмахну волшебной палочкой и начнется извержение вулкана. Смотри! А теперь все за мной ...«Нуклеиновые кислоты» химия
Цель урока: сформировать у студентов понимание взаимосвязанности и взаимозависимости веществ в клетке. Задачи урока: повторить строение и основные ...Конспекты
Валентность. Составление формул по валентности
Разработка урока Валентность. Составление формул по валентности. . Тема урока: Валентность. Составление формул по валентности. Цель урока:. ...Составление химических формул по валентности
Муниципальное казённое общеобразовательное учреждение «Тальменская средняя общеобразовательная школа №1». Тальменского района Алтайского края. ...Химические уравнения. Составление химических уравнений
ПЛАН-КОНСПЕКТ УРОКА «Химические уравнения. Составление химических уравнений». (Тема урока). . ФИО (полностью). . Кротова Светлана Викторовна. ...Составление ионных уравнений
Конспект урока на тему: Составление ионных уравнений. Тип урока: . урок комплексного применения знаний, умений и навыков. . . Вид урока: практическая ...Вывод молекулярных формул органических веществ по продуктам сгорания
Львова Елена Михайловна. . Учитель-методист Почетный работник образования. КГУ гимназия город Балхаш Казахстан. Вывод молекулярных формул ...Валентность химических элементов
Тема:. Валентность химических элементов. Цель:. Ознакомление с понятием «валентность». Определение валентности элементов по формулам их соединений. ...Валентность химических элементов
Муниципальное бюджетное образовательное учреждение. . средняя общеобразовательная школа № 144. . ул. Красных партизан, 8а г. Нижний Новгород, ...Валентность химических элементов
10. . . Урок по теме: «Валентность химических элементов». Тип урока. : комбинированный, изучение нового материала. Цель урока:. сформировать ...Валентность и степень окисления атомов. Периодичность в изменении свойств соединений элементов
План учебного занятия №4. . Дата Предмет. химия. группа. Ф.И.О. преподавателя:. Кайырбекова И.А. . І. Тема занятия:. . Валентность и степень ...Валентность и степень окисления атомов
Тема урока: «Валентность и степень окисления атомов». Цель урока:. Определить понятие валентности и степени окисления атомов. . Задачи:. . обучающие:. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:6 декабря 2018
Категория:Химия
Содержит:21 слайд(ов)
Поделись с друзьями:
Скачать презентацию