Слайд 1Стронций
Презентацию подготовила Жаркова Ольга, 11 «А»
Слайд 2Стронций.
Стро́нций — элемент главной подгруппы второй группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 38. Обозначается символом Sr (лат. Strontium). Простое вещество стронций — мягкий, ковкий и пластичный щёлочноземельный металл серебристо-белого цвета. Sr - (стронций) , имеет порядковый номер 38. Схема электрон. строения: +38 ) ) ) ) ) 2 8 18 8 2 Электрон. фор-ла: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s2 Графическая электрон. ф-ла: 5s2 | | 4p6 | | | | | | 4s2 | | 3d10 | | | | | | | | | | 3p6 | | | | | | 3s2 | | 2p6 | | | | | | 2s2 | | 1s2 | |

Слайд 3Свое название стронций получил от минерала стронцианита, найденного в 1787 в свинцовом руднике около Стронциана (Шотландия) в 1790 английским химиком Адером Кроуфордом было показано, что стронцианит содержит новую, еще неизвестную «землю». Эту особенность стронцианита установил также и немецкий химик Мартин Генрих Клапрот Английский химик Т.Хоп в 1791 доказал, что в стронцианите содержится новый элемент. Он четко разграничил соединения бария, стронция и кальция, используя, помимо других методов, характерную окраску пламени: желто-зеленую для бария, ярко-красную для стронция и оранжево-красную для кальция. Независимо от западных ученых, петербургский академик Тобиаш (Товий Егорович) Ловиц (1757–1804) в 1792, исследуя минерал барит, пришел к заключению, что в нем, помимо оксида бария, в качестве примеси находится и «стронцианова земля». Он сумел извлечь из тяжелого шпата более 100 г новой «земли» и исследовал ее свойства. В свободном виде стронций первым выделил английский химик и физик Гемфри Дэви в 1808. Металлический стронций был получен при электролизе его увлажненного гидроксида. Выделявшийся на катоде стронций соединялся с ртутью, образуя амальгаму. Разложив амальгаму нагреванием, Дэви выделил чистый металл.
Мартин Генрих Клапрот
История открытия
ЛОВИЦ Товий Егорович

Слайд 4Нахождение в природе
Содержание в земной коре 0,034% по массе. В свободном виде не встречается. Он входит в состав около 40 минералов. Из них наиболее важный — целестин SrSO4 (51,2% Sr). Добывают также стронцианит SrCO3 (64,4% Sr). Эти два минерала имеют промышленное значение. Чаще всего стронций присутствует как примесь в различных кальциевых минералах. Среди прочих минералов стронция: SrAl3(AsO4)SO4(OH)6 — кеммлицит; Sr2Al(CO3)F5 — стенонит; SrAl2(CO3)2(OH)4•Н2О — стронциодрессерит; SrAl3(PO4)2(OH)5•Н2О — гойясит; Sr2Al(PO4)2OH — гудкенит; SrAl3(PO4)SO4(OH)6 — сванбергит; Sr(AlSiO4)2 — слосонит; Sr(AlSi3O8)2•5Н2О — брюстерит; Sr5(AsO4)3F — ферморит; Sr2(B14O23)•8Н2О — стронциоджинорит; Sr2(B5O9)Cl•Н2О — стронциохильгардит; SrFe3(PO4)2(OH)5•Н2О — люсуньит; SrMn2(VO4)2•4Н2О — сантафеит; Sr5(PO4)3OH — беловит; SrV(Si2O7) — харадаит.

Слайд 5Физические свойства
Стронций — мягкий серебристо-белый металл, обладает ковкостью и пластичностью, легко режется ножом. Полиморфен — известны три его модификации. До 215оС устойчива кубическая гранецентрированная модификация (α-Sr), между 215 и 605оС — гексагональная (β-Sr), выше 605оС — кубическая объемно-центрированная модификация (γ-Sr). Температура плавления — 768оС, Температура кипения — 1390оС.

Слайд 6Химические свойства
Стронций в своих соединениях всегда проявляет валентность +2. По свойствам стронций близок к кальцию и барию, занимая промежуточное положение между ними. В электрохимическом ряду напряжений стронций находится среди наиболее активных металлов (его нормальный электродный потенциал равен −2,89 В. Энергично реагирует с водой, образуя гидроксид: Sr + 2H2O = Sr(OH)2 + H2↑ Взаимодействует с кислотами, вытесняет тяжёлые металлы из их солей. С концентрированными кислотами (H2SO4, HNO3) реагирует слабо. Металлический стронций быстро окисляется на воздухе, образуя желтоватую плёнку, в которой помимо оксида SrO всегда присутствуют пероксид SrO2 и нитрид Sr3N2. При нагревании на воздухе загорается, порошкообразный стронций на воздухе склонен к самовоспламенению. Энергично реагирует с неметаллами — серой, фосфором, галогенами. Взаимодействует с водородом (выше 200оС), азотом (выше 400оС). Практически не реагирует с щелочами. При высоких температурах реагирует с CO2, образуя карбид: 5Sr + 2CO2 = SrC2 + 4SrO Легкорастворимы соли стронция с анионами Cl−, I−, NO3−. Соли с анионами F−, SO42−, CO32−, PO43− малорастворимы.

Слайд 7Биологическая роль стронция
Стронций – составная часть микроорганизмов, растений и животных. У морских радиолярий скелет состоит из сульфата стронция – целестина.
Морские водоросли содержат 26–140 мг стронция на 100 г сухого вещества, на-земные растения – около 2,6, морские животные – 2–50, наземные животные – около 1,4, бактерии – 0,27–30. Накопление стронция различными организмами зависит не только от их вида, особенностей, но и от соотношения содержания стронция и других элементов, главным образом кальция и фосфора, в окружающей среде.
Соли и соединения стронция относятся к малотоксичным веществам, однако при избытке стронция поражаются костная ткань, печень и мозг. Будучи близок к кальцию по химическим свойствам, стронций резко отличается от него по своему биологическому действию. Избыточное содержание этого элемента в почвах, водах и продуктах питания вызывает «уровскую болезнь» у человека и животных– поражение и деформацию суставов, задержку роста и другие нарушения.
В результате ядерных испытаний и аварий на АЭС в окружающую среду поступило большое количество радиоактивного стронция-90, период полураспада которого составляет 29,12 года. До тех пор, пока не были запрещены испытания атомного и водородного оружия в трех средах, число пострадавших от радиоактивного стронция росло из года в год.

Слайд 8Применение
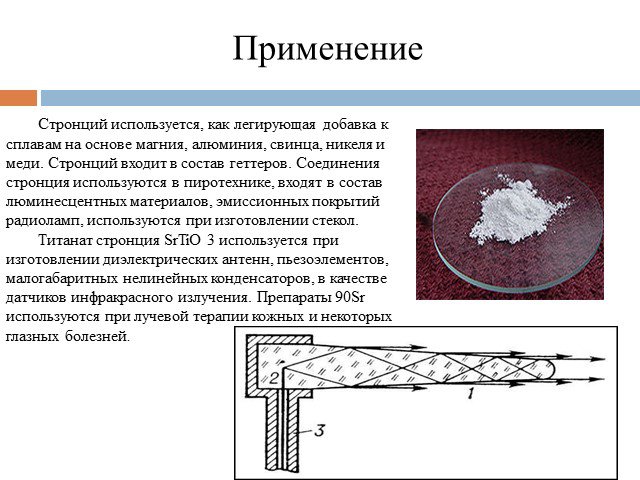
Стронций используется, как легирующая добавка к сплавам на основе магния, алюминия, свинца, никеля и меди. Cтронций входит в состав геттеров. Соединения стронция используются в пиротехнике, входят в состав люминесцентных материалов, эмиссионных покрытий радиоламп, используются при изготовлении стекол. Титанат стронция SrTiO 3 используется при изготовлении диэлектрических антенн, пьезоэлементов, малогабаритных нелинейных конденсаторов, в качестве датчиков инфракрасного излучения. Препараты 90Sr используются при лучевой терапии кожных и некоторых глазных болезней.

Слайд 9Стронций-90
Радиоизотоп стронция применяется в производстве атомных электрических батарей. Принцип действия таких батарей основан на способности стронция-90 излучать электроны, обладающие большой энергией, преобразуемой затем в электрическую. Элементы из радиоактивного стронция, соединенные в миниатюрную батарейку (размером со спичечную коробку), способны безотказно служить без перезарядки 15–25 лет, такие батареи незаменимы для космических ракет и искусственных спутников Земли. А швейцарские часовщики с успехом используют крохотные стронциевые батарейки для питания электрочасов.
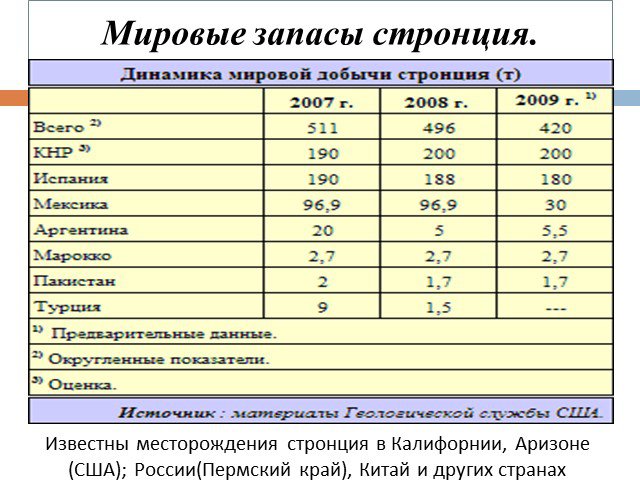
Слайд 10Мировые запасы стронция.
Известны месторождения стронция в Калифорнии, Аризоне (США); России(Пермский край), Китай и других странах