"Задачи по химии для 10 класса" презентация, проект, доклад
Презентацию на тему "Задачи по химии для 10 класса" (10 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 16 слайд(ов).
Слайды презентации
Список похожих презентаций
Занимательные задачи по химии
Физические и химические явления. Задача №1. Прочитайте отрывок из стихотворения С. Я. Маршака «Вчера и сегодня». Лампа плакала в углу, За дровами ...Задачи по химии
Муниципальное бюджетное образовательное учреждение «Средняя общеобразовательная школа № 7». Составитель: Маклакова Т.С. Вид: Электронный задачник ...Задания С 3 для подготовки к ГИА -9 по химии
№ 1. При нагревании красного порошка некоторого металла на воздухе порошок стал чёрным. Когда этот порошок растворили в серной кислоте, раствор приобрёл ...«Средства для мытья полов»
Моющие средства. Моющее средство, детергент — вещество или смесь, помогающее отмывать что-либо от грязи. Наиболее распространены три вида смесей-детергентов: ...«Своя игра» по химии
Необходим в составе костей скелета. Меню. Лечебные элементы 20. Дезинфектор ран. Лечебные элементы 40. Избыток ионов этого элемента может вызвать ...«Деятельностно-компетентностный подход к преподаванию химии в средней школе через современные образовательные технологии»
КЛЮЧЕВЫЕ КОМПЕТЕНТНОСТИ. Общепредметные компетенции:. Предметные компетенции:. понятие о химии, как неотъемлемой составляющей естественно-научной ...Методические рекомендации по подготовке к ЕГЭ по химии
Кодификатор. Программа элективного курса «окислительно-восстановительные реакции». H2O2 H2SO4. «окислительно-восстановительные реакции в органической ..."Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Химическая среда. Сама вода является очень слабым электролитом. При её электролитической диссоциации образуются катионы водорода и гидроксид-ионы ..."Гидролиз солей". Готовимся к ОГЭ и ЕГЭ по химии.
Содержание химии очень обширно и часто предстает копилкой огромного числа формул, уравнений, фактов и законов, запомнить которые не просто трудно, ...Методика преподавания химии
ПРИМЕРНАЯ СХЕМА НАКОПЛЕНИЯ БАЛЛОВ. Самостоятельная домашняя работа. 7 – 9 неделя. Составление алгоритма выполнения заданий. Составление тематического ...Алгоритм решения задач по химии
Алгоритм решения задач по химии:. Записать краткое условие задачи; *В случае необходимости произвести предварительный расчет; Перевести величины, ...Активизация обучающихся на уроках химии как показатель развития их мыслительной деятельности.
Приёмы активизации мыслительной деятельности обучающихся:. Приём стимулирующих звеньев Приём реконструкции Приём прогнозирования. Приём стимулирующих ...Методы познания химии
09.09.2018. Метод (от греческого слова «методос» — путь к чему-либо) означает совокупность приемов и операций практического и теоретического освоения ...Личностно – ориентированный подход в обучении химии
Когда людей станут учить не тому, что они должны думать, а тому как они должны думать, то тогда исчезнут всякие недоразумения. Г. Лихтенберг. Как ...Анализ результатов ЕГЭ по химии 2010 (окружной семинар учителей химии)
Результаты ЕГЭ 2010. Граница минимального балла -33 тестовых балла (12 первичных баллов). Уровни оценивания: неудовлетворительный – 0–32 / 0–11; удовлетворительный ...Консультация экспертов ЕГЭ по химии 2012 год
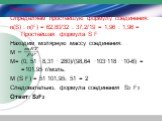
С1. Cr2(SO4)3 + Br2 + NaOH = = Na2CrO4 + NaBr + Na2SO4+ H2O. 2 Cr+3 – 3e- → Cr+6 ок-е 3 Br2 + 2e- → 2Br -1 в-е. 3 6 16 8. C2-2012. Демо-2012. Соль, ...Методика преподавания химии в школе. УМК по химии
Учебник. Дидактические материалы. 8 класс: 9 класс. Методическое пособие. Цифровые ресурсы. Лабораторный журнал. Учебная книга Задачник. Автор: Жилин ...Использование химии в медицине
Содержание. Помощь химии В наши дни Успехи Фармацевтика Типы лекарств неорганические препараты органические препараты Классификация Фармакологическая ...Анализ ЕГЭ по химии 2011
Уровни выполнения экзаменационной работы. неудовлетворительный – 0–31 / 0–12, удовлетворительный –32–56 / 13–35, хороший – 57–77 / 36–56, отличный ...Викторина по химии
1.Газ, который применили во время первой мировой войны в качестве химического оружия. 2. Единственный жидкий металл. 3.Русский учёный - энциклопедист. ...Конспекты
Материалы для индивидуальной работы по химии
Предмет: химия. Учитель: Пестова Татьяна Михайловна. Класс: 8. Материалы для индивидуальной работы по химии. Индивидуальные задания разнообразны ...методическая разработка урока по химии
Муниципальное бюджетное общеобразовательное учреждение. « Средняя общеобразовательная школа села Алексеевка ». Базарно – Карабулакского района Саратовской ...Обобщающее повторение по неорганической химии
Обобщающее повторение по неорганической химии за курс 8 класса. Разработан Савич Еленой Николаевной учителем биологии, химии Донецкой СШ с. Донецкое, ...Лабораторные опыты по неорганической химии (свойства кислот, оснований, солей)
III. . . . Технологическая карта урока. ЭТАПЫ УРОКА. ДЕЯТЕЛЬНОСТЬ УЧИТЕЛЯ. . ДЕЯТЕЛЬНОСТЬ УЧЕНИКА. . 1.Организационный. . момент. ...Развитие познавательной самостоятельности на уроках химии через составление химических задач
Развитие познавательной самостоятельности на уроках химии через составление химических задач. «Не мыслям надо учить, а мыслить…». . И.Кант. ...Развитие интеллекта и творческих способностей учащихся на уроках химии
Перед современной школой стоит задача воспитания грамотного, продуктивно мыслящего человека, адаптированного к условиям жизни в обществе. Проблема ...Решение экспериментальных задач по органической химии
Конспект открытого урока . Практическая работа №4 «Решение экспериментальных задач по органической химии». Класс:10. УМК: Рудзитис Г.Е., ФельдманФ.Г. ...Использование опорных схем на уроках химии
Муниципальное образовательное автономное учреждение средняя общеобразовательная школа с углубленным изучением отдельных предметов №1 г. Белогорск, ...Задачи по теме «Галогены
Задачи по теме «Галогены». №1. Сколько миллилитров раствора с массовой долей соляной кислоты 36 % (пл. 1,2 г/мл) необходимо для взаимодействия 0,1 ...Обобщение знаний по классам неорганических соединений
Тема урока. . Обобщение знаний по классам неорганических соединений. ( урок для учащихся 8 классов по неорганической химии, изучаемый в разделе « ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:24 ноября 2018
Категория:Химия
Классы:
Содержит:16 слайд(ов)
Поделись с друзьями:
Скачать презентацию