Презентация "Углеводороды" по химии – проект, доклад
Презентацию на тему "Углеводороды" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 33 слайд(ов).
Слайды презентации
Список похожих презентаций
Углеводороды ряда этилена
Этилен. Углеводороды ряда этилена Цель урока. Повторить строение молекулы этилена, виды изомерии и номенклатуру алкенов, химические свойства этилена. ...Углеводороды в вопросах ЕГЭ
Силу ума придают упражнения, а не покой. Учащиеся должны. Знать классы углеводородов и их общие формулы Уметь составлять формулы углеводородов Уметь ...Углеводороды и их природные источники. Прородный газ
Углеводороды-это класс органических соединений,молекулы которых состоят только из углерода и водорода. Наиболее распространенными природными источниками ...Углеводороды алкены
Учебная цель:. изучить способы получения, химические свойства и применение алкенов на примере непредельного углеводорода - этилена. Эпиграф к уроку. ...Углеводороды ароматического ряда
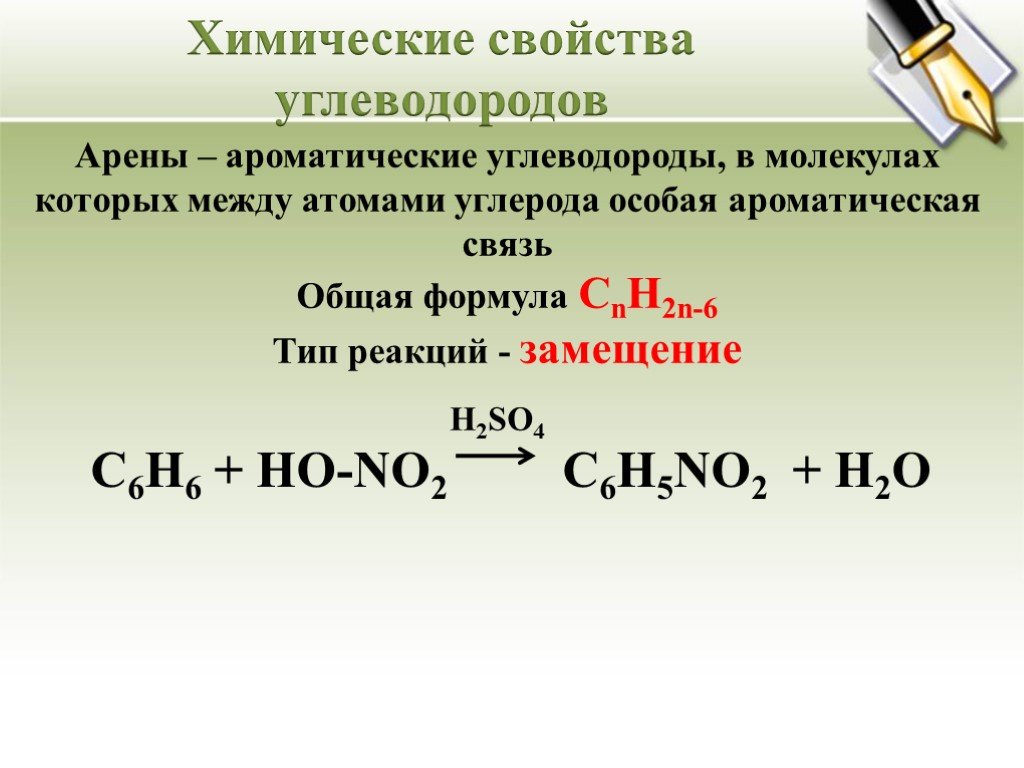
Какие углеводороды называются ароматическими? Ароматические углеводороды (арены) – это углеводороды с общей формулой СnH2n-6, в молекулах которых ...Углеводороды
Предельные (насыщенные). Непредельные Алканы Циклоалканы Алкены Алкадиены Алкины. Алканы (парафины). К алканам (парафинам) относятся соединения с ...Углеводороды
Задачи урока: 1. проверить качество усвоения материала 2. Стимулировать познавательную активность учащихся 3. Развивать смекалку, эрудицию, быстро ...Углеводороды
1. Гомологическому ряду алканов соответствует общая формула: а) СпН2п+2; б) СпН2п; в) СпН2п-2; г) СпНп+2 2. Название углеводорода СН3 – СН – СН3 а) ...Углеводороды
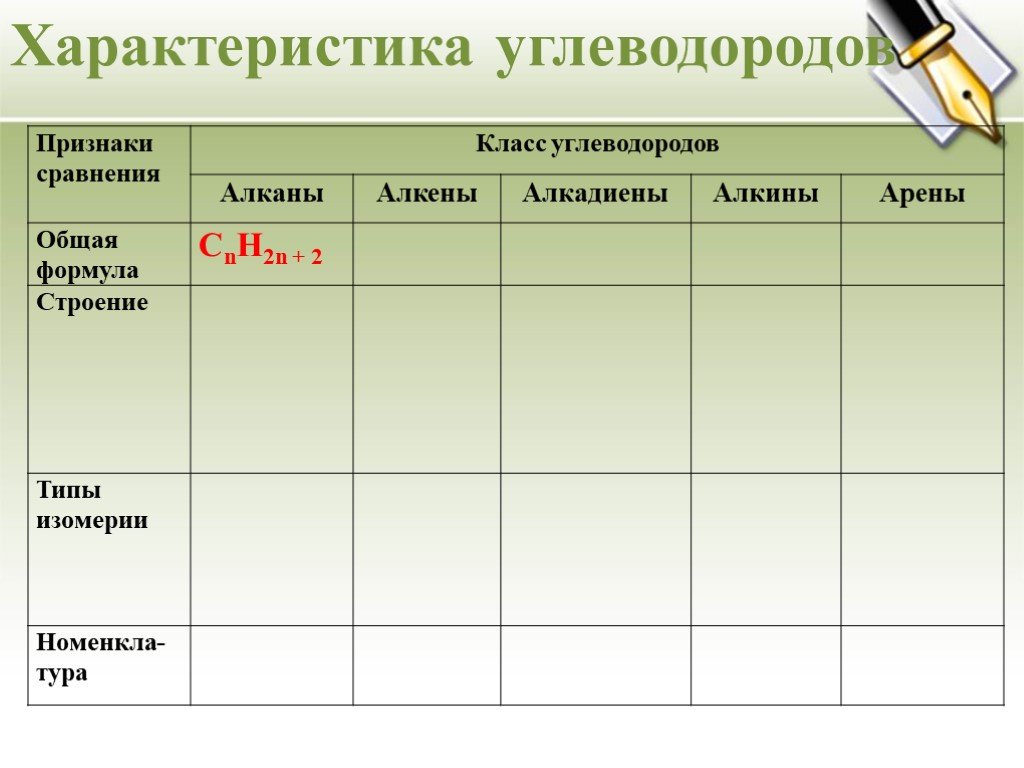
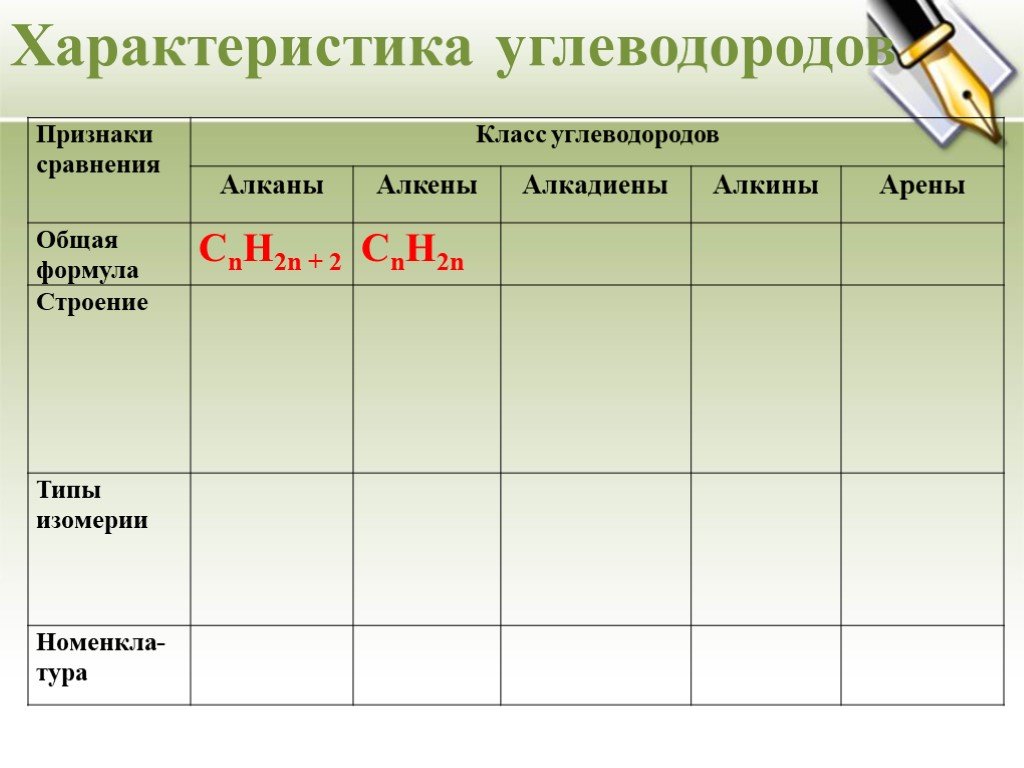
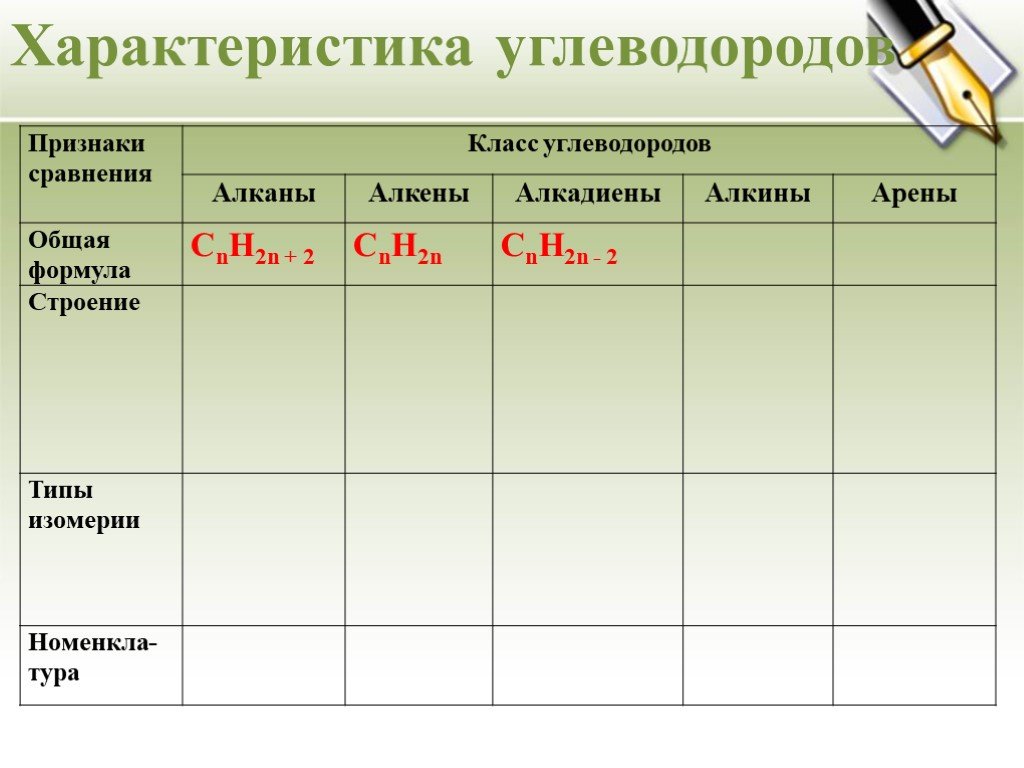
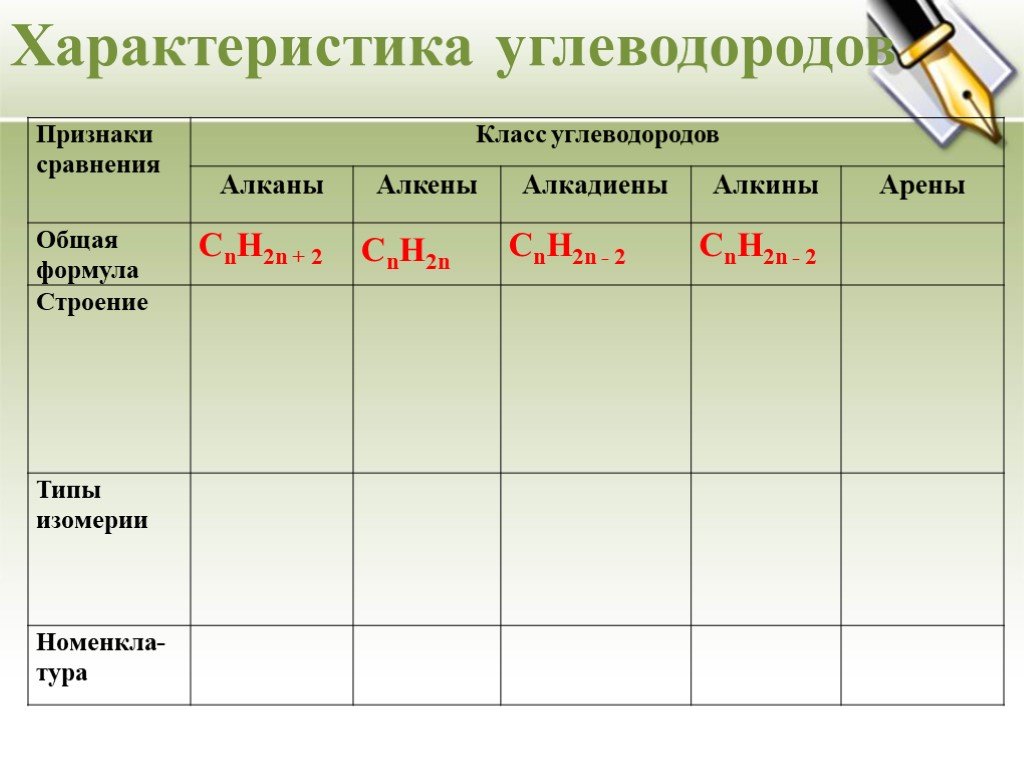
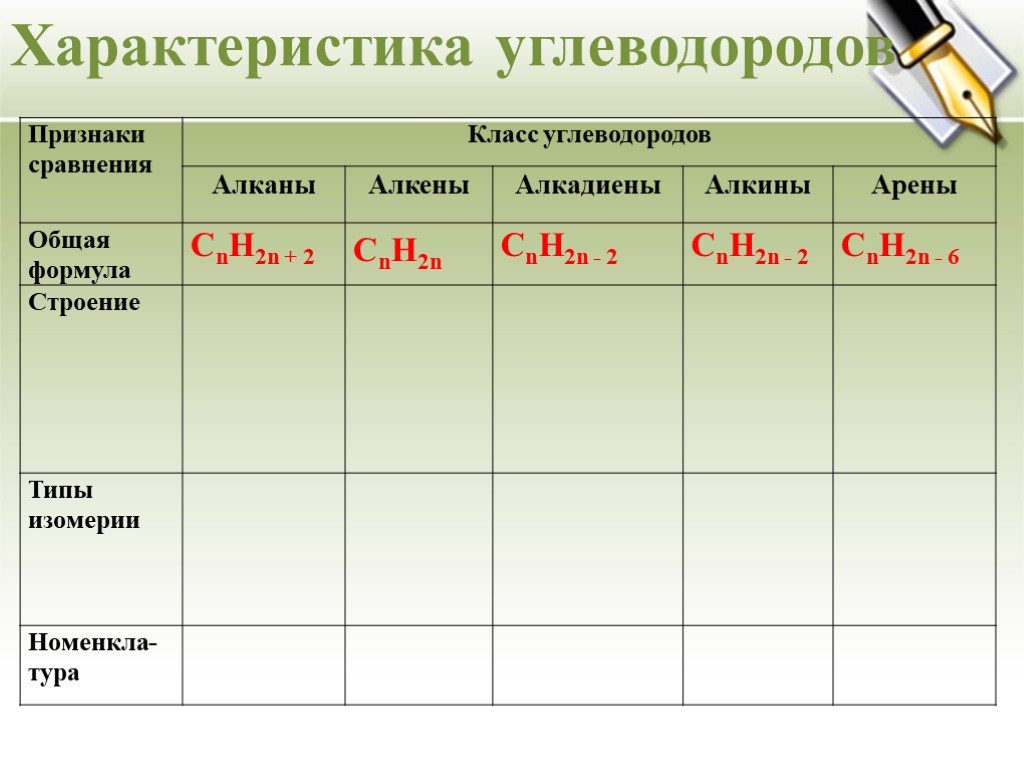
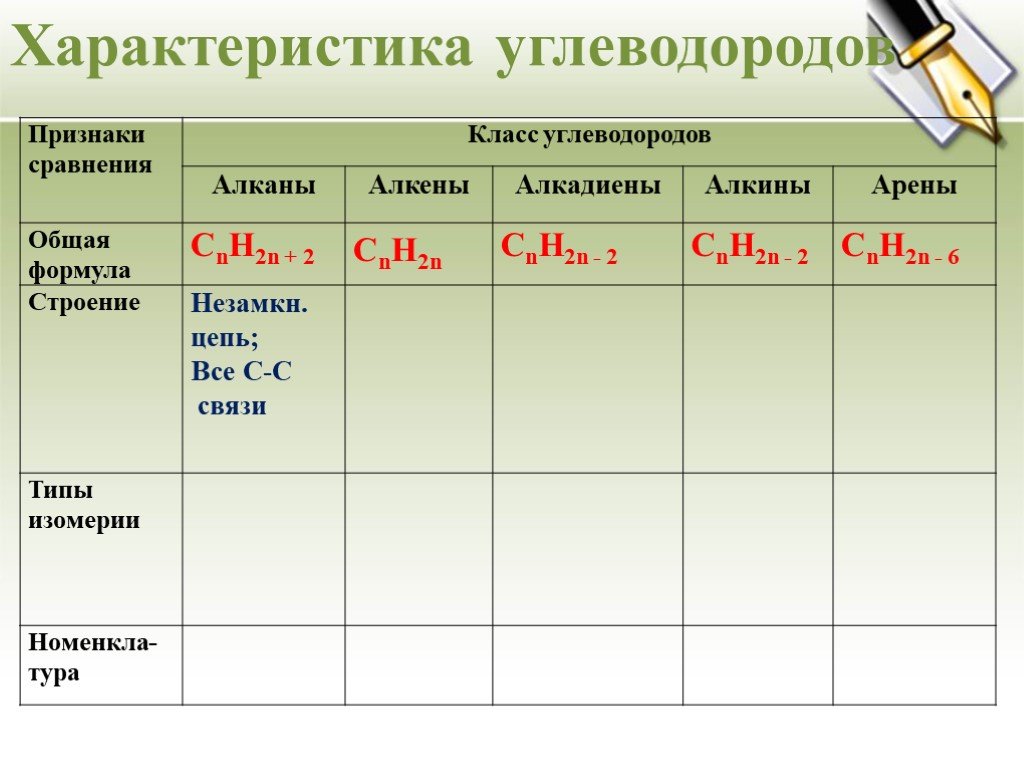
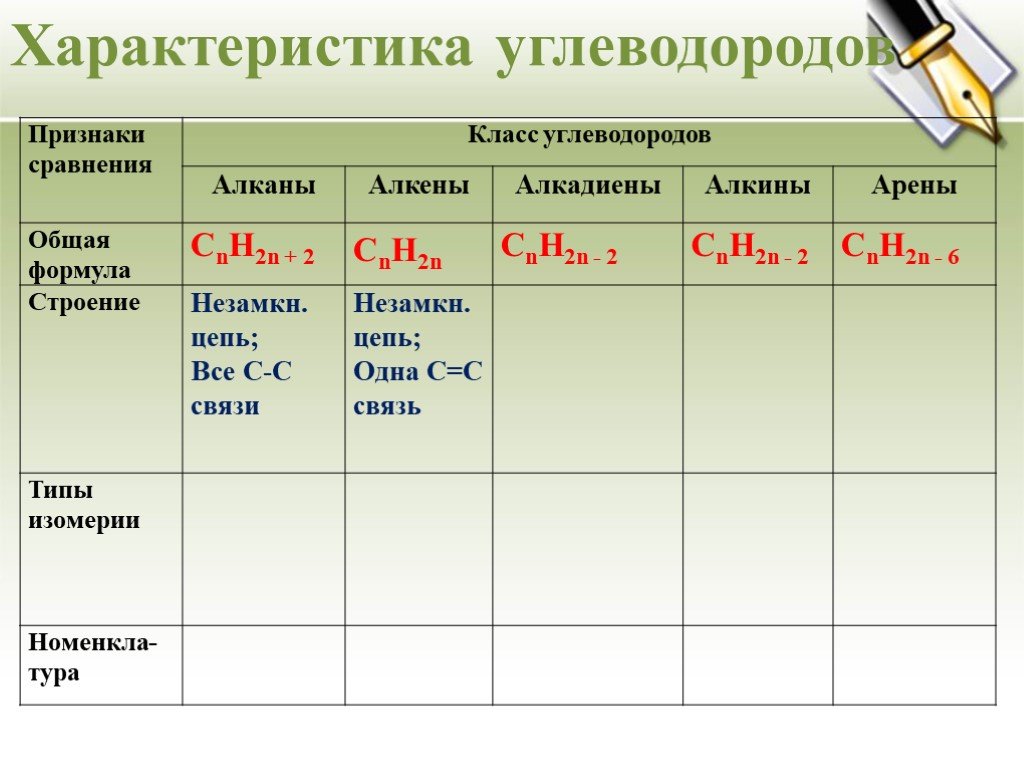
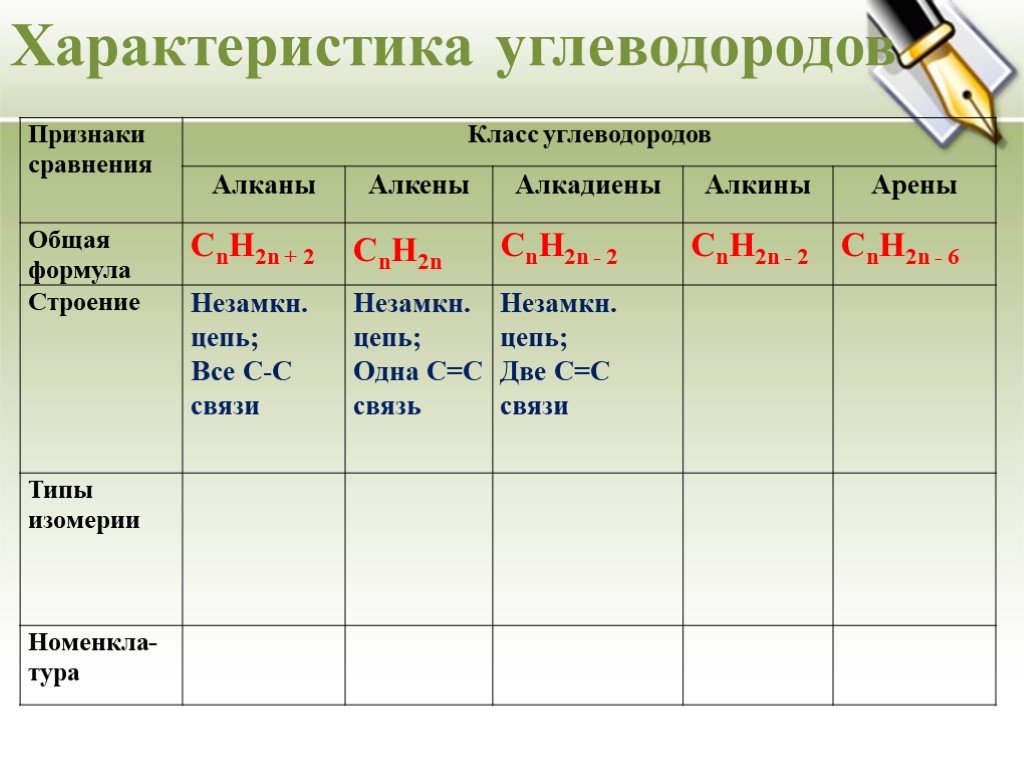
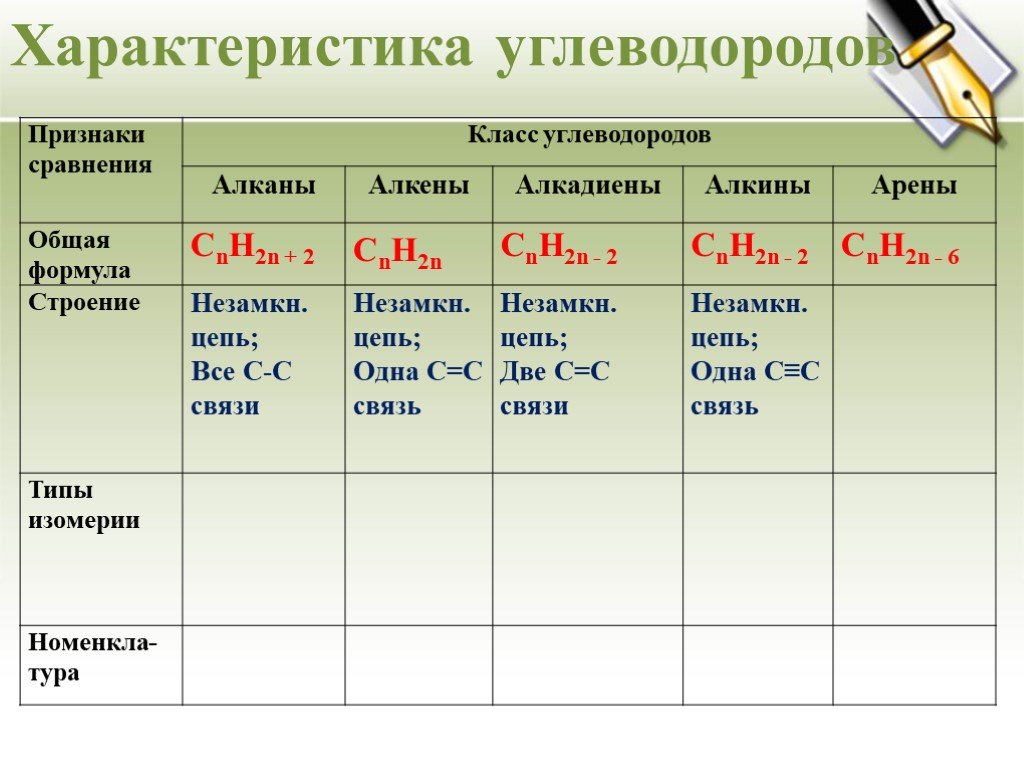
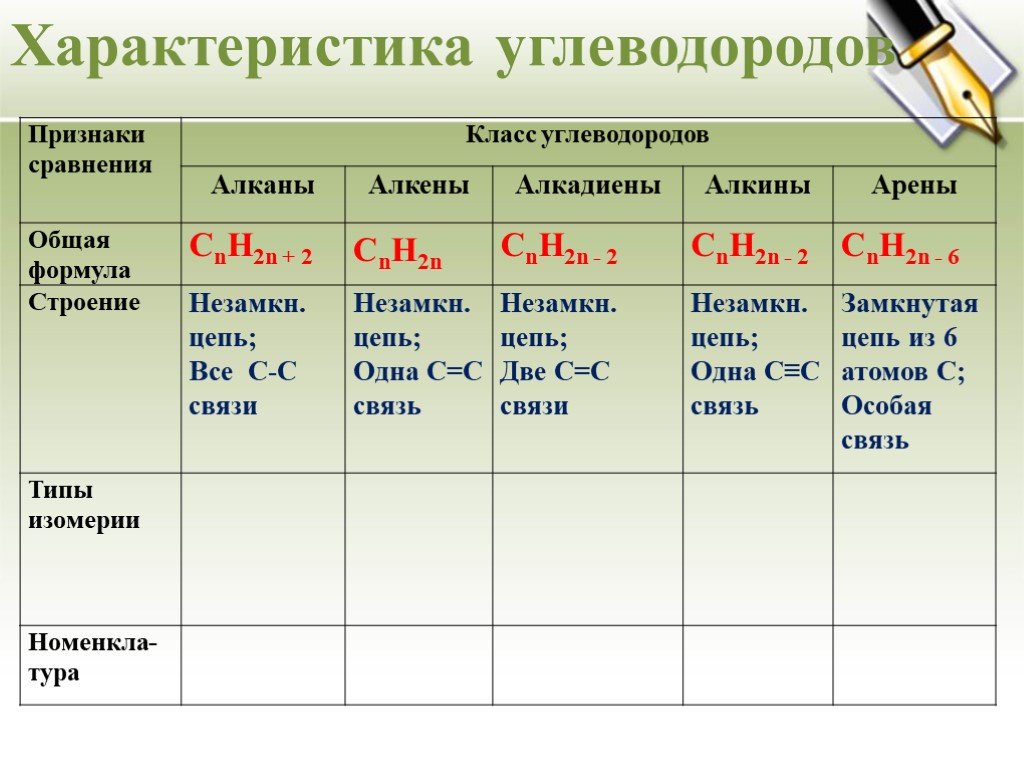
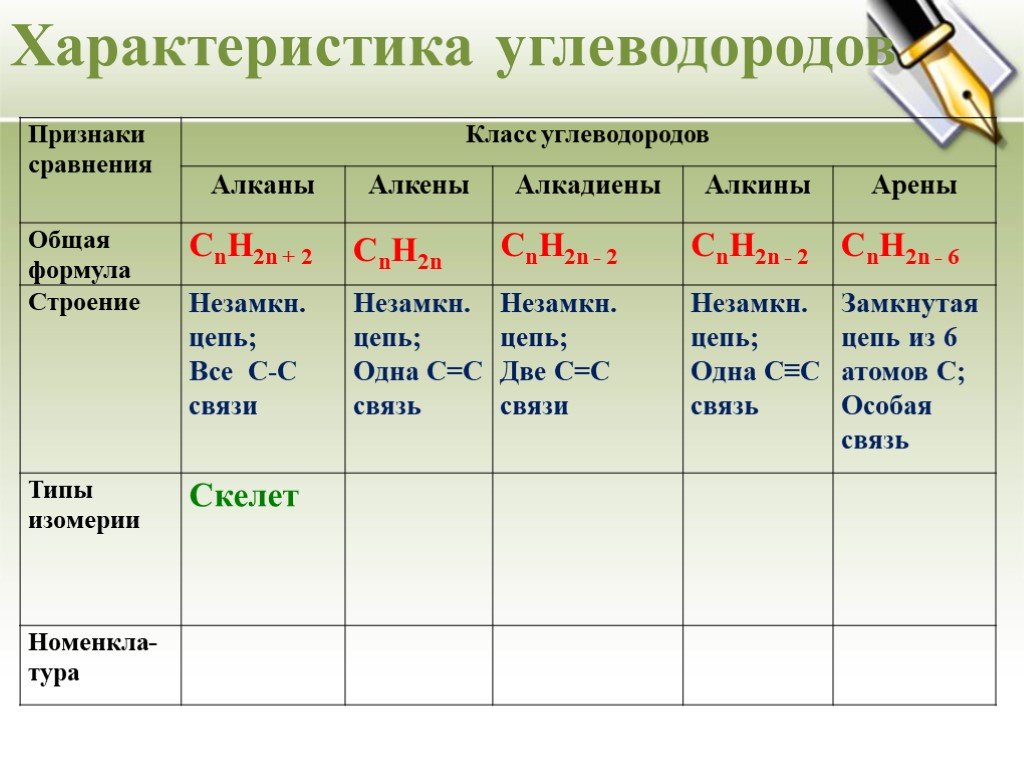
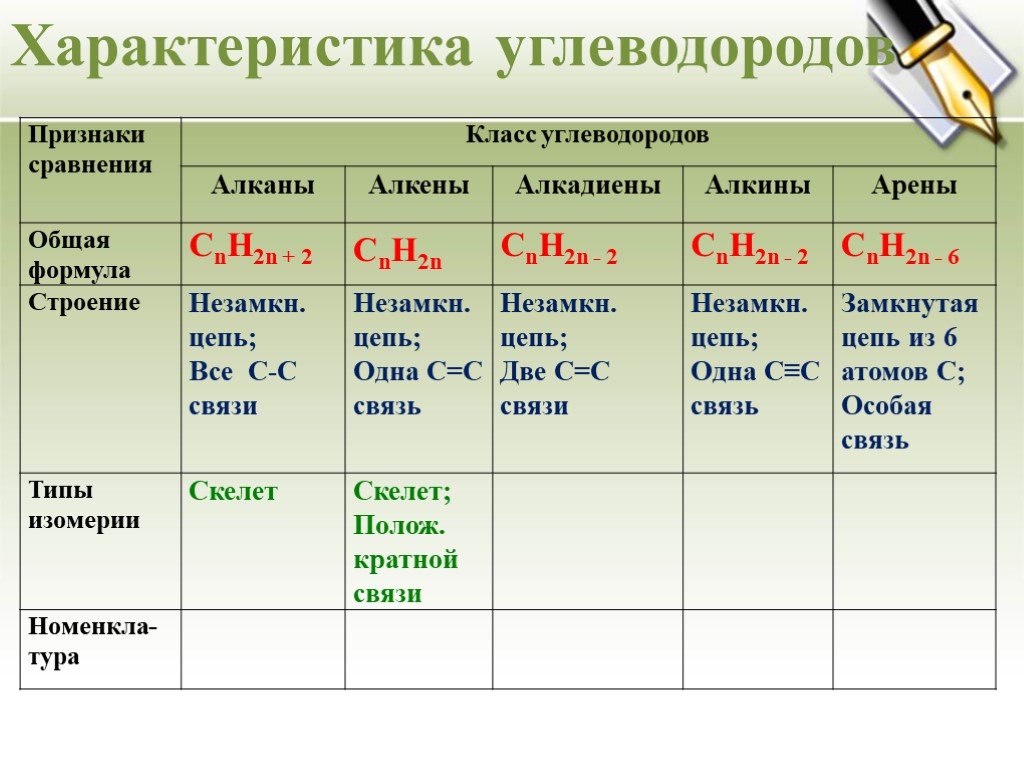
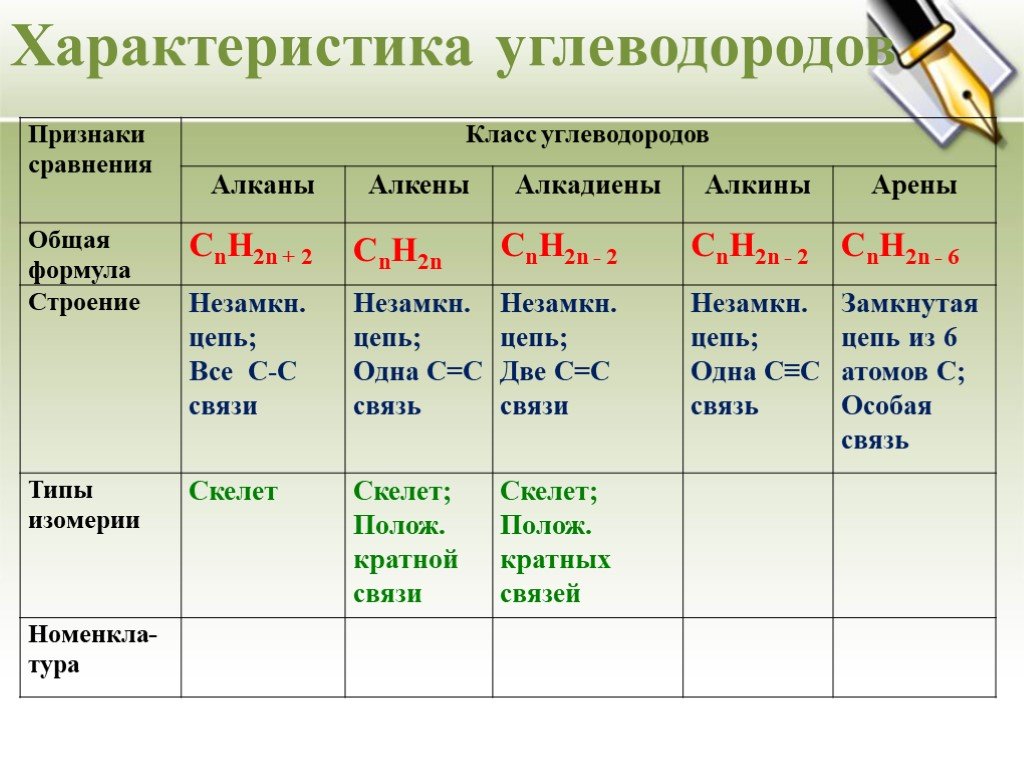
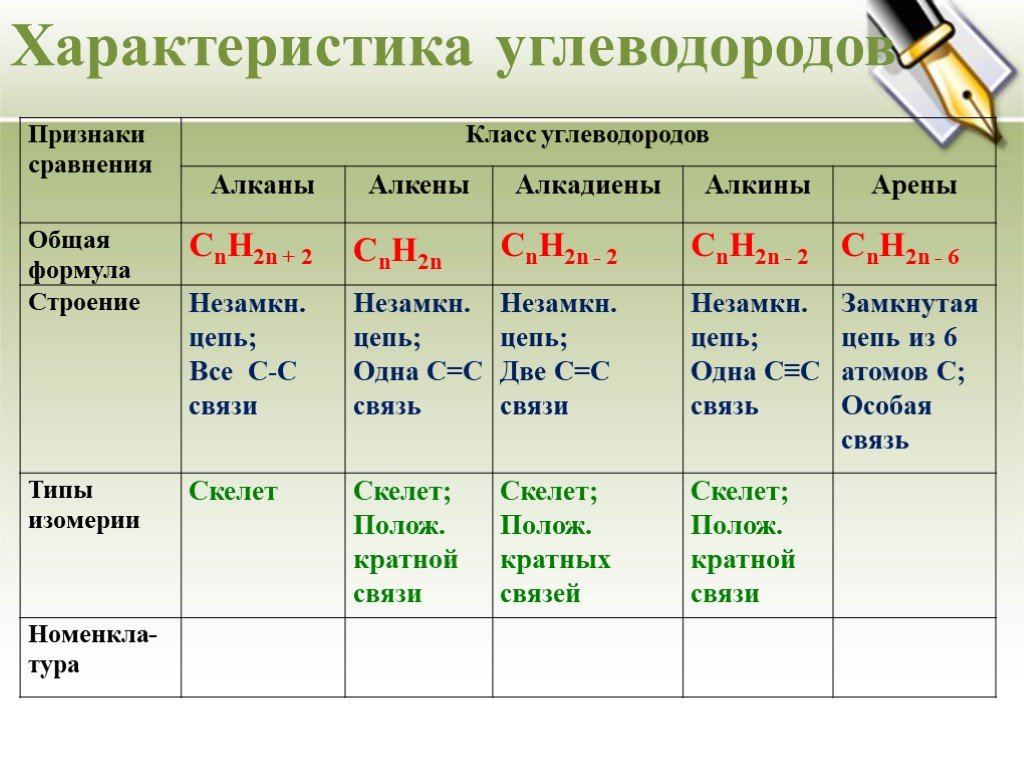
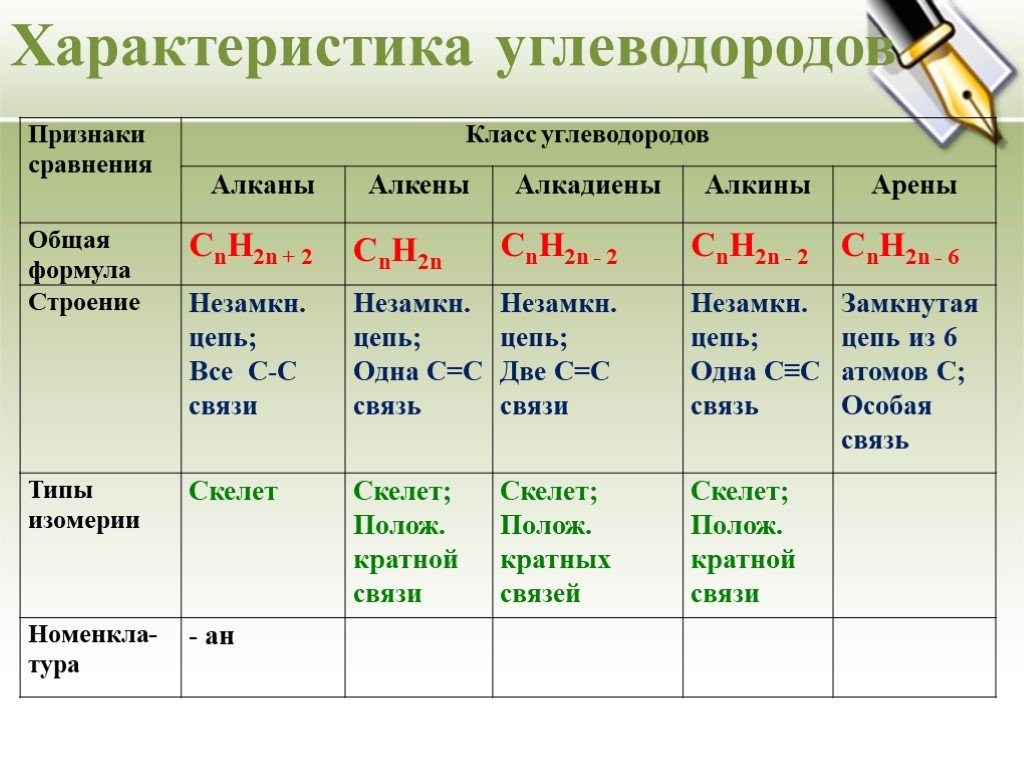
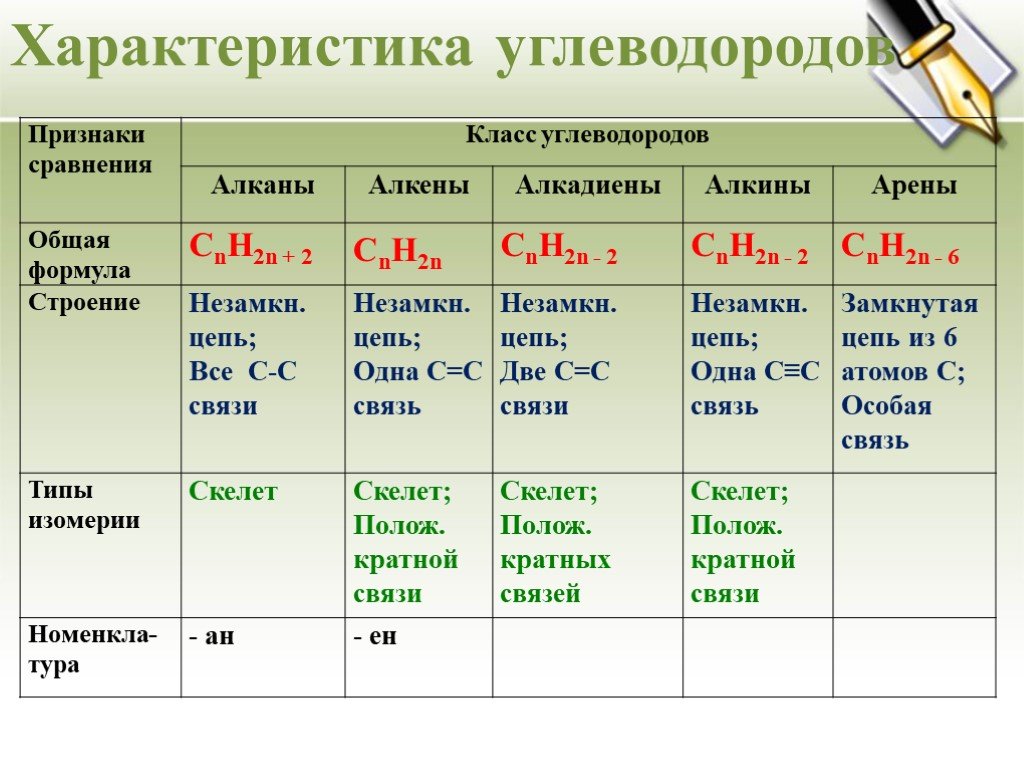
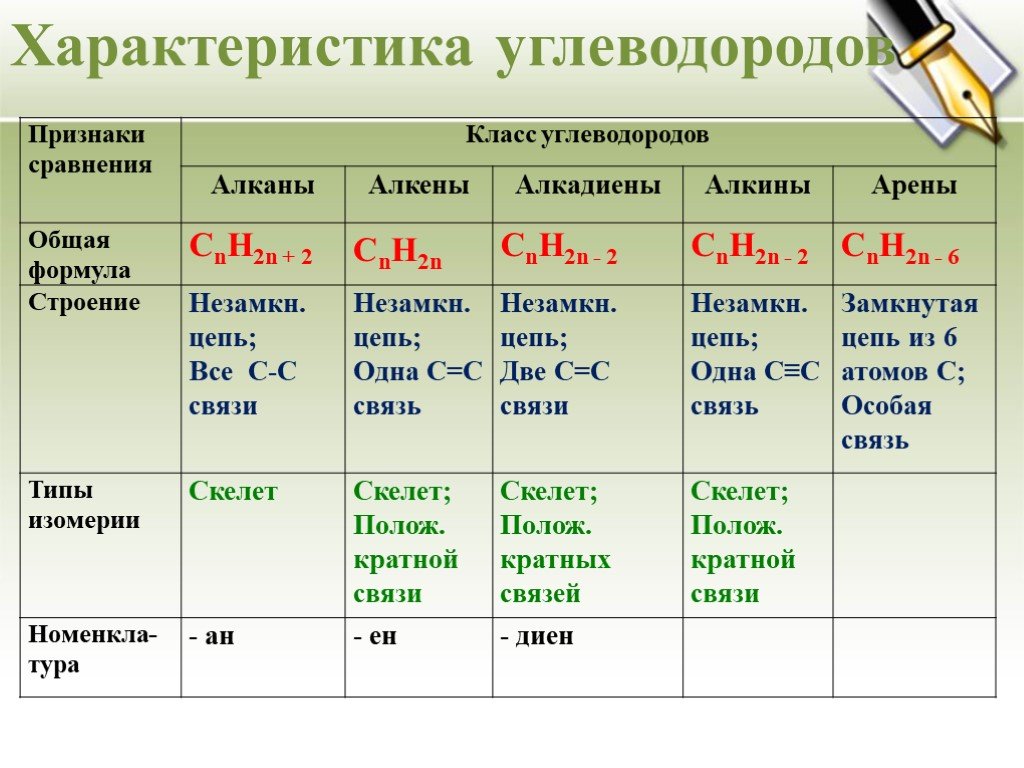
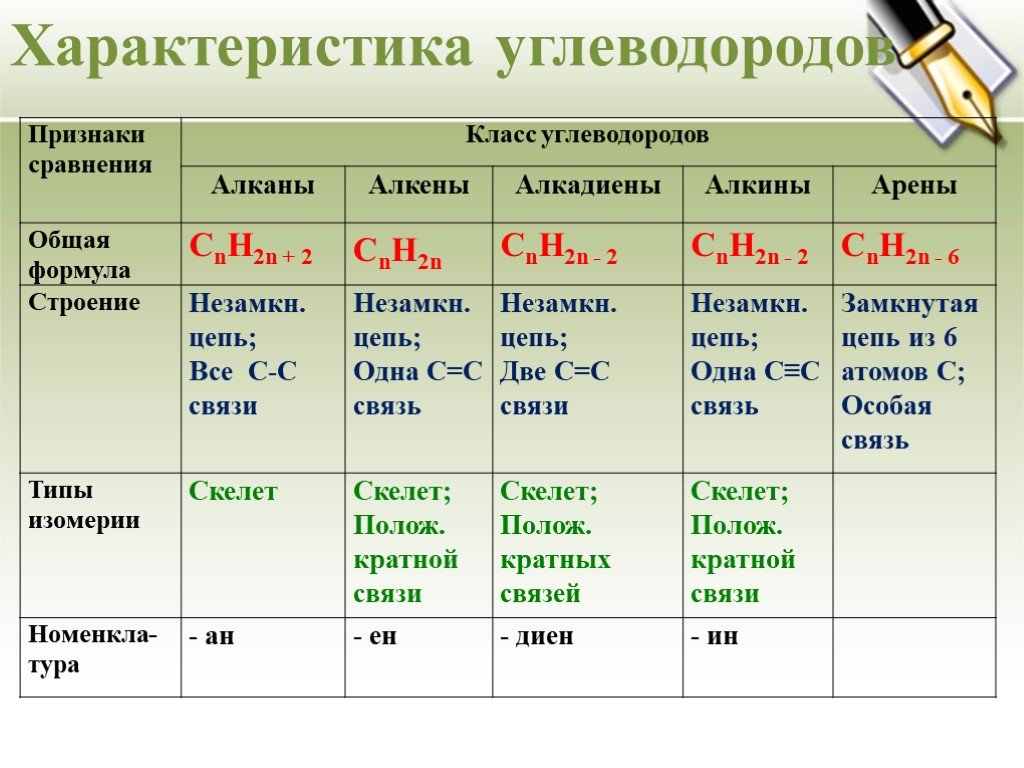
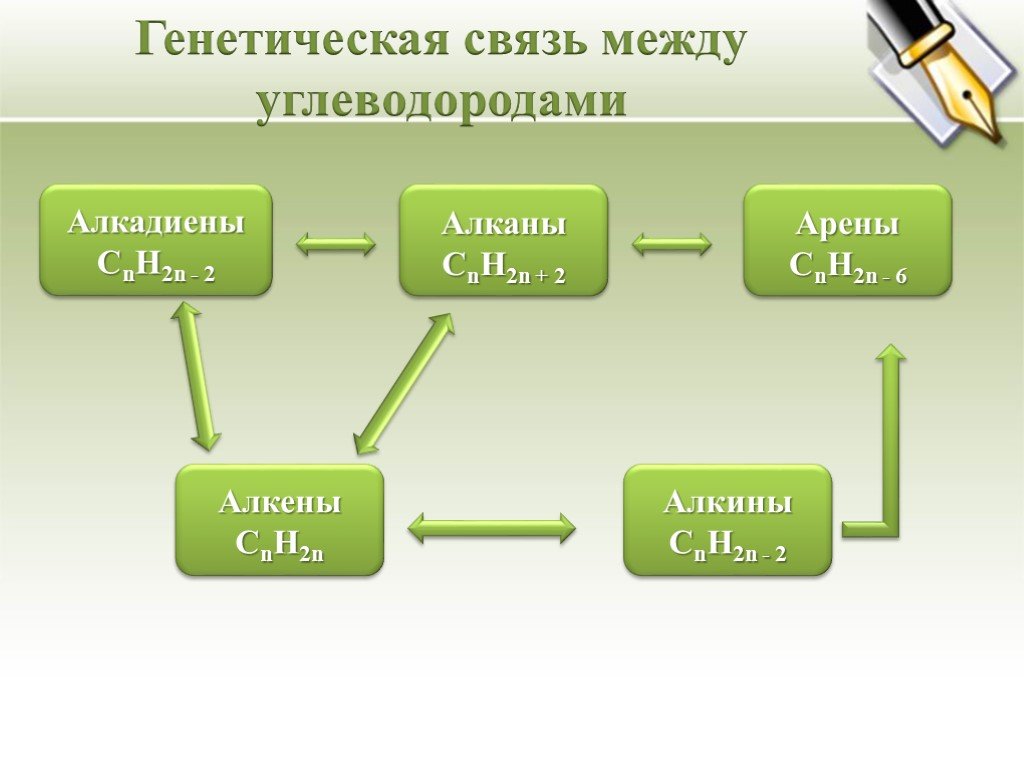
Урок - обобщение по теме "Углеводороды". Углеводороды: алканы алкены алкины алкадиены циклоалканы арены СnH2n+2 СnH2n СnH2n-2 СnH2n-6. Составьте молекулярные ...Углеводороды
Цель урока: обобщить сведения об углеводородах. УЭ1 Обобщить знания по составу и классификации углеводородов, особенностях строения их молекул. Что ...Предельные углеводороды химия
Органическая химия – это раздел химической науки, в котором изучаются соединения углерода и их превращения. В наши дни к органическим веществам относятся ...Предельные углеводороды
Определение. Предельные углеводороды - это органические вещества, состоящие только из углерода и водорода, соответствующие общей формуле Сn Н2n +2. ...Предельные углеводороды
План урока. Понятие о углеводородах. 2.Предельные углеводороды. 3.Природные источники углеводородов. 4. Вопросы. Д/З § 33, В.3, 4. 1. Понятие о углеводородах. ...Предельные углеводороды
Классификация органических веществ. УГЛЕВОДОРОДЫ – это вещества, состоящие только из углерода и водорода. Определение предельных углеводородов (ПУВ). ...Предельные углеводороды (алканы, или парафины)
Алканы – название предельных углеводородов по международной номенклатуре Междунаро́дный сою́з теорети́ческой и прикладно́й хи́мии (ИЮПАК, International ...Обобщение: предельные и непредельные углеводороды
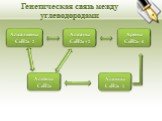
Цели урока:. повторить, обобщить и закрепить полученные знания и умения по темам «Предельные и непредельные углеводороды» изучить генетическую связь ...Предельные углеводороды
Цели урока: Научить учащихся выводить формулу вещества по его относительной плотности и массовым долям элементов, выводить формулу вещества по его ...Насыщенные углеводороды
Определение. Алканы- это углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле CnH2n+2. Строение. ...Непредельные углеводороды
Непредельные УГЛЕВОДОРОДЫ. Алкены Алкадиены Алкины. Цель викторины:. Повторить, закрепить и проверить материал по теме: «Непредельные углеводороды», ...Ароматические углеводороды – арены. Бензол как представитель ароматических углеводородов
Бензол как представитель ароматических углеводородов. Задачи урока:. на примере бензола познакомиться с углеводородами, которые имеют замкнутые цепи ...Конспекты
Углеводороды
Пояснительная записка. Шаповалова Ирина Анатольевна. Учитель химии. МОУ «СОШ№11 с углубленным изучением иностранных языков». г.Ноябрьск, ЯНАО. ...Углеводороды
. МИНИСТЕРСТВО ОБРАЗОВАНИЯ ОМСКОЙ ОБЛАСТИ. Бюджетное образовательное учреждение. . начального профессионального образования. . «Профессиональное ...Углеводороды
Технологическая карта урока. Тема раздела:. Углеводороды. СМК раздела. Основные классы УВ: алканы, алкены, алкины, алкадиены, циклоалканы, ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:27 октября 2018
Категория:Химия
Содержит:33 слайд(ов)
Поделись с друзьями:
Скачать презентацию




































![СН2=СН2+[O]+H2O → СН2OH - СН2OH СН2=СН2+[O]+H2O → СН2OH - СН2OH](https://prezentacii.org/upload/cloud/18/10/92112/images/thumbs/screen24.jpg)