Слайд 1Презентация по теме «Металлы» «Уран»
Работа Садковского Ивана 9 «В»
Слайд 2Уран-(устаревший вариант ураний)-
химический элемент с атомным номером 92 в периодической системе, атомная масса 238,029; обозначается символом U (лат. Uranium), относится к семейству актиноидов. Физические свойства:Уран — очень тяжёлый, серебристо-белый глянцеватый металл. В чистом виде он немного мягче стали, ковкий, гибкий, обладает небольшими парамагнитными свойствам Степени окисления урана-6,5,4 и 3.

Слайд 3Химические свойства урана
Уран может проявлять степени окисления от +III до +VI. Соединения урана(III) образуют неустойчивые растворы красного цвета и являются сильными восстановителями: 4UCl3 + 2H2O → 3UCl4 + UO2 + H2↑ Соединения урана(IV) являются наиболее устойчивыми и образуют водные растворы зелёного цвета. Соединения урана(V) неустойчивы и легко диспропорционируют в водном растворе: 2UO2Cl → UO2Cl2 + UO2 Химически уран очень активный металл. Быстро окисляясь на воздухе, он покрывается радужной пленкой оксида. Мелкий порошок урана самовоспламеняется на воздухе, он зажигается при температуре 150—175 °C, образуя U3O8. При 1000 °C уран соединяется с азотом, образуя желтый нитрид урана. Вода способна разъедать металл, медленно при низкой температуре, и быстро при высокой, а также при мелком измельчении порошка урана. Уран растворяется в соляной, азотной и других кислотах, образуя четырёхвалентные соли, зато не взаимодействует с щелочами. Уран вытесняет водород из неорганических кислот и солевых растворов таких металлов, как ртуть, серебро, медь, олово, платина и золото. При сильном встряхивании металлические частицы урана начинают светиться. Уран имеет четыре степени окисления — III—VI. Шестивалентные соединения включают в себя триокись урана (окись уранила) UO3 и уранилхлорид урана UO2Cl2. Тетрахлорид урана UCl4 и диоксид урана UO2 — примеры четырёхвалентного урана. Вещества, содержащие четырёхвалентный уран, обычно нестабильны и обращаются в шестивалентные при длительном пребывании на воздухе. Ураниловые соли, такие как уранилхлорид, распадаются в присутствии яркого света или органики.

Слайд 4История
Ещё в древнейшие времена (I век до нашей эры) природная окись урана использовалась для изготовления жёлтой глазури для керамики. Исследования урана развивались, подобно порождаемой им цепной реакции. Вначале сведения о его свойствах, как и первые импульсы цепной реакции, поступали с большими перерывами, от случая к случаю. Первая важная дата в истории урана — 1789 год, когда немецкий натурфилософ и химик Мартин Генрих Клапрот восстановил извлечённую из саксонской смоляной руды золотисто-жёлтую «землю» до чёрного металлоподобного вещества. В честь самой далёкой из известных тогда планет (открытой Гершелем восемью годами раньше) Клапрот, считая новое вещество элементом, назвал его ураном. Пятьдесят лет уран Клапрота числился металлом. Только в 1841 г. Эжен Мелькиор Пелиго [(Eugene-Melchior Péligot) — французский химик (1811—1890) доказал, что, несмотря на характерный металлический блеск, уран Клапрота не элемент, а окисел UO2. В 1840 г. Пелиго удалось получить настоящий уран — тяжёлый металл серо-стального цвета и определить его атомный вес.

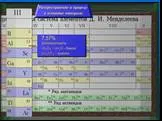
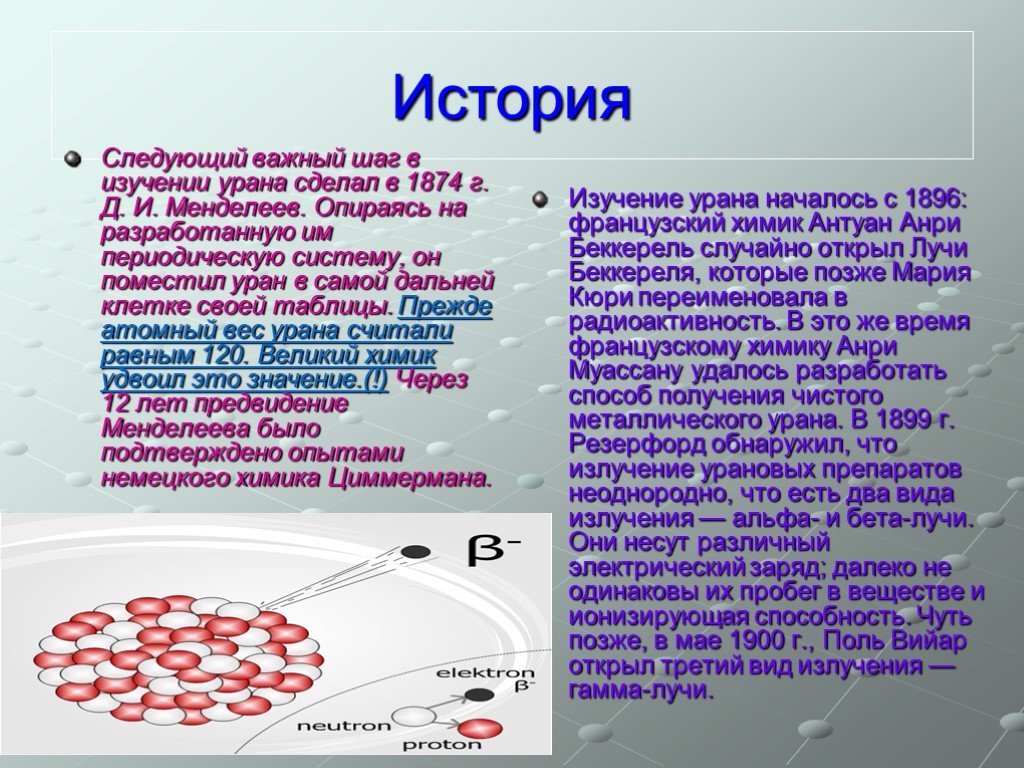
Слайд 5Следующий важный шаг в изучении урана сделал в 1874 г. Д. И. Менделеев. Опираясь на разработанную им периодическую систему, он поместил уран в самой дальней клетке своей таблицы. Прежде атомный вес урана считали равным 120. Великий химик удвоил это значение.(!) Через 12 лет предвидение Менделеева было подтверждено опытами немецкого химика Циммермана.
Изучение урана началось с 1896: французский химик Антуан Анри Беккерель случайно открыл Лучи Беккереля, которые позже Мария Кюри переименовала в радиоактивность. В это же время французскому химику Анри Муассану удалось разработать способ получения чистого металлического урана. В 1899 г. Резерфорд обнаружил, что излучение урановых препаратов неоднородно, что есть два вида излучения — альфа- и бета-лучи. Они несут различный электрический заряд; далеко не одинаковы их пробег в веществе и ионизирующая способность. Чуть позже, в мае 1900 г., Поль Вийар открыл третий вид излучения — гамма-лучи.
![Эрнест Резерфорд провёл в 1907 г. первые опыты по определению возраста минералов при изучении радиоактивных урана и тория [4] на основе созданной им совместно с Фредериком Содди (Soddy, Frederick, 1877—1956; Нобелевская премия по химии, 1921) теории радиоактивности. В 1913 г. Ф. Содди ввёл понятие о Эрнест Резерфорд провёл в 1907 г. первые опыты по определению возраста минералов при изучении радиоактивных урана и тория [4] на основе созданной им совместно с Фредериком Содди (Soddy, Frederick, 1877—1956; Нобелевская премия по химии, 1921) теории радиоактивности. В 1913 г. Ф. Содди ввёл понятие о](https://prezentacii.org/upload/cloud/18/10/84658/images/thumbs/screen6.jpg)
Слайд 6Эрнест Резерфорд провёл в 1907 г. первые опыты по определению возраста минералов при изучении радиоактивных урана и тория [4] на основе созданной им совместно с Фредериком Содди (Soddy, Frederick, 1877—1956; Нобелевская премия по химии, 1921) теории радиоактивности. В 1913 г. Ф. Содди ввёл понятие об изотопах (от греч. ισος — «равный», «одинаковый», и τόπος — «место»), а в 1920 г.предсказал, что изотопы можно использовать для определения геологического возраста горных пород. В 1928 г. Ниггот реализовал, а в 1939 г. A.O.К.Нир (Nier,Alfred Otto Carl,1911 — 1994) создал первые уравнения для расчёта возраста и применил масс-спектрометр для разделения изотопов. В 1938 немецкие физики Отто Ган и Фриц Штрассман открыли непредсказанное явление, происходящем с ядром урана при облучении его нейтронами. Захватывая свободный нейтрон, ядро изотопа урана 235U делится, при этом выделяется (в расчете на одно ядро урана) достаточно большая энергия, в основном, за счёт кинетической энергии осколков и излучения. Позднее теория этого явления была обоснована Лизой Мейтнер и Отто Фришем. Данное открытие явилось истоком как мирного, так и военного использования внутриатомной энергии. В 1939—1940 гг. Ю. Б. Харитон и Я. Б. Зельдович впервые теоретически показали, что при небольшом обогащении природного урана ураном-235 можно создать условия для непрерывного деления атомных ядер, то есть придать процессу цепной характер.

Слайд 7Изотопы
Изото́пы (от греч. ισος — «равный», «одинаковый», и τόπος — «место») — разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре. Название связано с тем, что изотопы находятся в одном и том же месте (в одной клетке) таблицы Менделеева. Химические свойства атома зависят практически только от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z (то есть количеством протонов в нём) и почти не зависит от его массового числа A (то есть суммарного числа протонов Z и нейтронов N). Все изотопы одного элемента имеют одинаковый заряд ядра, отличаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число (например, 12C, 222Rn). Можно также написать название элемента с добавлением через дефис массового числа (например, углерод-12, радон-222). Некоторые изотопы имеют традиционные собственные названия (например, дейтерий, актинон).

Слайд 8Нахождение в природе
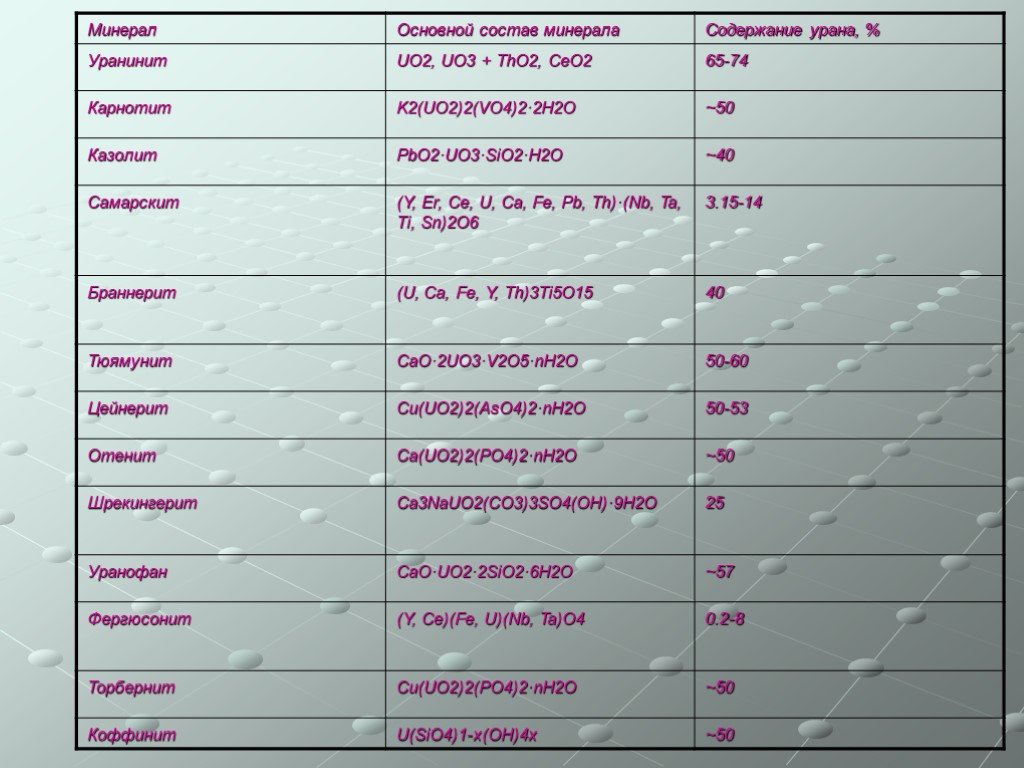
Уран широко распространён в природе. Количество урана в слое литосферы толщиной 20 км оценивается в 1,3·1014 т. Основная масса урана находится в кислых породах с высоким содержанием кремния. Значительная масса урана сконцентрирована в осадочных породах, особенно обогащённых органикой. В больших количествах как примесь уран присутствует в ториевых и редкоземельных минералах (ортит, сфен CaTiO3[SiO4], монацит (La,Ce}PO4, циркон ZrSiO4, ксенотим YPO4 и др.). Важнейшими урановыми рудами являются настуран (урановая смолка), уранинит и карнотит. Основными минералами — спутниками урана являются молибденит MoS2, галенит PbS, кварц SiO2, кальцит CaCO3, гидромусковит и др.

Слайд 10Содержание урана в земной коре составляет 0,003 %, он встречается в поверхностном слое земли в виде четырех видов отложений. Во-первых, это жилы уранинита, или урановой смолки (диоксид урана UO2), очень богатые ураном, но редко встречающиеся. Им сопутствуют отложения радия, так как радий является прямым продуктом изотопного распада урана. Такие жилы встречаются в Заире, Канаде (Большое Медвежье озеро), Чехии и Франции. Вторым источником урана являются конгломераты ториевой и урановой руды совместно с рудами других важных минералов. Конгломераты обычно содержат достаточные для извлечения количества золота и серебра, а сопутствующими элементами становятся уран и торий. Большие месторождения этих руд находятся в Канаде, ЮАР, России и Австралии. Третьим источником урана являются осадочные породы и песчаники, богатые минералом карнотитом (уранил-ванадат калия), который содержит, кроме урана, значительное количество ванадия и других элементов. Такие руды встречаются в западных штатах США. Железоурановые сланцы и фосфатные руды составляют четвертый источник отложений. Богатые отложения обнаружены в глинистых сланцах Швеции. Некоторые фосфатные руды Марокко и США содержат значительные количества урана, а фосфатные залежи в Анголе и Центральноафриканской Республике еще более богаты ураном. Большинство лигнитов и некоторые угли обычно содержат примеси урана. Богатые ураном отложения лигнитов обнаружены в Северной и Южной Дакоте (США) и битумных углях Испании и Чехии [3].

Слайд 11Физиологическое действие
В микроколичествах (10−5—10−8 %) обнаруживается в тканях растений, животных и человека. В наибольшей степени накапливается некоторыми грибами и водорослями. Соединения урана всасываются в желудочно-кишечном тракте (около 1 %), в легких — 50 %. Основные депо в организме: селезёнка, почки, скелет, печень, лёгкие и бронхо-лёгочные лимфатические узлы. Содержание в органах и тканях человека и животных не превышает 10−7г. Уран и его соединения токсичны. Особенно опасны аэрозоли урана и его соединений. Для аэрозолей растворимых в воде соединений урана ПДК в воздухе 0,015 мг/м³, для нерастворимых форм урана ПДК 0,075 мг/м³. При попадании в организм уран действует на все органы, являясь общеклеточным ядом. Уран практически необратимо, как и многие другие тяжелые металлы, связывается с белками, прежде всего, с сульфидными группами аминокислот, нарушая их функцию. Молекулярный механизм действия урана связан с его способностью подавлять активность ферментов. В первую очередь поражаются почки (появляются белок и сахар в моче, олигурия). При хронической интоксикации возможны нарушения кроветворения и нервной системы.

Слайд 12Получение урана
Самая первая стадия уранового производства — концентрирование. Породу дробят и смешивают с водой. Тяжёлые компоненты взвеси осаждаются быстрее. Если порода содержит первичные минералы урана, то они осаждаются быстро: это тяжёлые минералы. Вторичные минералы урана легче, в этом случае раньше оседает тяжёлая пустая порода. (Впрочем, далеко не всегда она действительно пустая; в ней могут быть многие полезные элементы, в том числе и уран). Следующая стадия — выщелачивание концентратов, перевод урана в раствор. Применяют кислотное и щелочное выщелачивание. Первое — дешевле, поскольку для извлечения урана используют серную кислоту. Но если в исходном сырье, как, например, в урановой смолке, уран находится в четырёхвалентном состоянии, то этот способ неприменим: четырёхвалентный уран в серной кислоте практически не растворяется. В этом случае нужно либо прибегнуть к щелочному выщелачиванию, либо предварительно окислять уран до шестивалентного состояния. Не применяют кислотное выщелачивание и в тех случаях, если урановый концентрат содержит доломит или магнезит, реагирующие с серной кислотой. В этих случаях пользуются едким натром (гидроксидом натрия). Проблему выщелачивания урана из руд решает кислородная продувка. В нагретую до 150 °C смесь урановой руды с сульфидными минералами подают поток кислорода. При этом из сернистых минералов образуется серная кислота, которая и вымывает уран.

Слайд 13На следующем этапе из полученного раствора нужно избирательно выделить уран. Современные методы — экстракция и ионный обмен — позволяют решить эту проблему. Раствор содержит не только уран, но и другие катионы. Некоторые из них в определённых условиях ведут себя так же, как уран: экстрагируются теми же органическими растворителями, оседают на тех же ионообменных смолах, выпадают в осадок при тех же условиях. Поэтому для селективного выделения урана приходится использовать многие окислительно-восстановительные реакции, чтобы на каждой стадии избавляться от того или иного нежелательного попутчика. На современных ионообменных смолах уран выделяется весьма селективно. Методы ионного обмена и экстракции хороши ещё и тем, что позволяют достаточно полно извлекать уран из бедных растворов (содержание урана — десятые доли грамма на литр

Слайд 14После этих операций уран переводят в твёрдое состояние — в один из оксидов или в тетрафторид UF4. Но этот уран ещё надо очистить от примесей с большим сечением захвата тепловых нейтронов — бора, кадмия, гафния. Их содержание в конечном продукте не должно превышать стотысячных и миллионных долей процента. Для удаления этих примесей технически чистое соединение урана растворяют в азотной кислоте. При этом образуется уранилнитрат UO2(NO3)2, который при экстракции трибутил-фосфатом и некоторыми другими веществами дополнительно очищается до нужных кондиций. Затем это вещество кристаллизуют (или осаждают пероксид UO4·2H2O) и начинают осторожно прокаливать. В результате этой операции образуется трёхокись урана UO3, которую восстанавливают водородом до UO2. На диоксид урана UO2 при температуре от 430 до 600 °C воздействуют сухим фтористым водородом для получения тетрафторида UF4. Из этого соединения восстанавливают металлический уран с помощью кальция или магния.
Слайд 15Применение урана
Ядерное топливо Геология Ядерное оружие
Слайд 16Ядерное топливо
Изотоп U238 способен делиться под влиянием бомбардировки высокоэнергетическими нейтронами, эту его особенность используют для увеличения мощности термоядерного оружия (используются нейтроны, порождённые термоядерной реакцией). В результате захвата нейтрона с последующим β-распадом 238U может превращаться в 239Pu, который затем используется как ядерное топливо. Уран-233, искусственно получаемый в реакторах из тория (торий-232 захватывает нейтрон и превращается в торий-233, который распадается в протактиний-233 и затем в уран-233), может в будущем стать распространённым ядерным топливом для атомных электростанций (уже сейчас существуют реакторы, использующие этот нуклид в качестве топлива, например KAMINI в Индии) и производства атомных бомб (критическая масса около 16 кг). Уран-233 также является наиболее перспективным топливом для газофазных ядерных ракетных двигателей.

Слайд 17Геология
Основная отрасль использования урана — определение возраста минералов и горных пород с целью выяснения последовательности протекания геологических процессов. Этим занимаются Геохронология и Теоретическая геохронология. Существенное значение имеет также решение задачи о смешении и источниках веществВ связи с тем, что горные породы содержат различные концентрации урана, они обладают различной радиоактивностью. Это свойство используется при выделении горных пород геофизическими методами. Наиболее широко этот метод применяется в нефтяной геологии при геофизических исследованиях скважин, в этот комплекс входит, в частности, γ — каротаж или нейтронный гамма-каротаж, гамма-гамма-каротаж и т. д.

Слайд 18Ядерное оружие
Урановая бомба: Для того, чтобы реакция могла поддерживать сама себя, необходимо соответствующее «топливо», в качестве которого на первых этапах использовался изотоп урана. Уран в природе встречается в виде двух изотопов — уран-235 и уран-238. При поглощении ураном-235 нейтрона в процессе распада выделяется от одного до трёх нейтронов. Уран-238, напротив, при поглощении нейтронов умеренных энергий не выделяет новые, препятствуя ядерной реакции. Он превращается в уран-239, затем в нептуний-239, и наконец, в относительно стабильный плутоний-239. Для обеспечения работоспособности ядерной бомбы содержание урана-235 в ядерном топливе должно быть не ниже 80 %, иначе уран-238 быстро погасит цепную ядерную реакцию. Природный же уран почти весь (около 99,3 %) состоит из урана-238. Поэтому при производстве ядерного топлива применяют сложный и многоступенчатый процесс обогащения урана, в результате которого доля урана-235 повышается. Бомба на основе урана стала первым ядерным оружием, использованным человеком в боевых условиях (бомба «Малыш», сброшенная на Хиросиму).

Слайд 19Обеднённый уран
После извлечения 235U и 234U из природного урана, оставшийся материал (уран-238) носит название «обеднённый уран», так как он обеднён 235-м изотопом. Обеднённый уран в два раза менее радиоактивен, чем природный уран, в основном за счёт удаления из него 234U. Из-за того, что основное использование урана — производство энергии, обеднённый уран — малополезный продукт с низкой экономической ценностью. В основном его использование связано с большой плотностью урана и относительно низкой его стоимостью. Обеднённый уран используется для радиационной защиты (как это ни странно) и как балластная масса в аэрокосмических применениях, таких как рулевые поверхности летательных аппаратов. В каждом самолёте «Боинг-747» содержится 1500 кг обеднённого урана для этих целей. Ещё этот материал применяется в высокоскоростных роторах гироскопов, больших маховиках, как балласт в космических спускаемых аппаратах и гоночных яхтах, при бурении нефтяных скважин.

Слайд 20Сердечники бронебойных снарядов
Самое известное применение обеднённого урана — в качестве сердечников для бронебойных снарядов. При сплавлении с 2 % Mo или 0,75 % Ti и термической обработке (быстрая закалка разогретого до 850 °C металла в воде или масле, дальнейшее выдерживание при 450 °C 5 часов) металлический уран становится твёрже и прочнее стали (прочность на разрыв больше 1600 МПа, при том, что у чистого урана она равна 450 МПа). В сочетании с большой плотностью, это делает закалённую урановую болванку чрезвычайно эффективным средством для пробивания брони, аналогичным по эффективности более дорогому вольфраму. Тяжёлый урановый наконечник также изменяет распределение масс в снаряде, улучшая его аэродинамическую устойчивость. Подобные сплавы типа «Стабилла» применяются в стреловидных оперенных снарядах танковых и противотанковых артиллерийских орудий. Процесс разрушения брони сопровождается измельчением в пыль урановой болванки и воспламенением её на воздухе с другой стороны брони Около 300 тонн обеднённого урана остались на поле боя во время операции «Буря в Пустыне» (по большей части это остатки снарядов 30-мм пушки GAU-8 штурмовых самолётов A-10, каждый снаряд содержит 272 г уранового сплава). Такие снаряды были использованы войсками НАТО в боевых действиях на территории Югославии[12]. После их применения обсуждалась экологическая проблема радиационного загрязнения территории страны. Впервые уран в качестве сердечника для снарядов был применен в Третьем рейхе. Обеднённый уран используется в современной танковой броне, например, танка M-1 «Абрамс».
![Другие сферы применения. Небольшая добавка урана придаёт красивую жёлто-зелёную флуоресценцию стеклуУранат натрия Na2U2O7 использовался как жёлтый пигмент в живописи.[11] Соединения урана применялись как краски для живописи по фарфору и для керамических глазурей и эмалей (окрашивают в цвета: жёлтый, Другие сферы применения. Небольшая добавка урана придаёт красивую жёлто-зелёную флуоресценцию стеклуУранат натрия Na2U2O7 использовался как жёлтый пигмент в живописи.[11] Соединения урана применялись как краски для живописи по фарфору и для керамических глазурей и эмалей (окрашивают в цвета: жёлтый,](https://prezentacii.org/upload/cloud/18/10/84658/images/thumbs/screen21.jpg)
Слайд 21Другие сферы применения
Небольшая добавка урана придаёт красивую жёлто-зелёную флуоресценцию стеклуУранат натрия Na2U2O7 использовался как жёлтый пигмент в живописи.[11] Соединения урана применялись как краски для живописи по фарфору и для керамических глазурей и эмалей (окрашивают в цвета: жёлтый, бурый, зелёный и чёрный, в зависимости от степени окисления).[11] Некоторые соединения урана светочувствительны.[11] В начале XX века уранилнитрат широко применялся для усиления негативов и окрашивания (тонирования) позитивов (фотографических отпечатков) в бурый цвет.[11] Карбид урана-235 в сплаве с карбидом ниобия и карбидом циркония применяется в качестве топлива для ядерных реактивных двигателей (рабочее тело — водород + гексан). Сплавы железа и обеднённого урана (уран-238) применяются как мощные магнитострикционные материалы.

























![Эрнест Резерфорд провёл в 1907 г. первые опыты по определению возраста минералов при изучении радиоактивных урана и тория [4] на основе созданной им совместно с Фредериком Содди (Soddy, Frederick, 1877—1956; Нобелевская премия по химии, 1921) теории радиоактивности. В 1913 г. Ф. Содди ввёл понятие о Эрнест Резерфорд провёл в 1907 г. первые опыты по определению возраста минералов при изучении радиоактивных урана и тория [4] на основе созданной им совместно с Фредериком Содди (Soddy, Frederick, 1877—1956; Нобелевская премия по химии, 1921) теории радиоактивности. В 1913 г. Ф. Содди ввёл понятие о](https://prezentacii.org/upload/cloud/18/10/84658/images/thumbs/screen6.jpg)













![Другие сферы применения. Небольшая добавка урана придаёт красивую жёлто-зелёную флуоресценцию стеклуУранат натрия Na2U2O7 использовался как жёлтый пигмент в живописи.[11] Соединения урана применялись как краски для живописи по фарфору и для керамических глазурей и эмалей (окрашивают в цвета: жёлтый, Другие сферы применения. Небольшая добавка урана придаёт красивую жёлто-зелёную флуоресценцию стеклуУранат натрия Na2U2O7 использовался как жёлтый пигмент в живописи.[11] Соединения урана применялись как краски для живописи по фарфору и для керамических глазурей и эмалей (окрашивают в цвета: жёлтый,](https://prezentacii.org/upload/cloud/18/10/84658/images/thumbs/screen21.jpg)